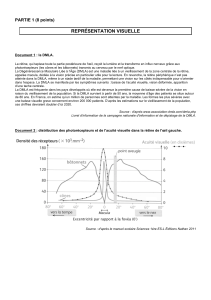
Prévention de la dégénérescence maculaire liée a` l`âge

Pre
´vention de la de
´ge
´ne
´rescence maculaire lie
´ea
`l’a
ˆge
Prevention of age-related macular degeneration
DELPHINE COUASNON, ELSA COBAST, AUDE HERVE, EMILIE LE HAZIF, ALAIN B. LEGRAND
Faculté des sciences pharmaceutiques et biologiques, Université de Rennes 1, 2, avenue du professeur Léon Bernard, 35043 Rennes cedex
Re
´sume
´.
La de
´ge
´ne
´rescence maculaire lie
´ea
`l’a
ˆge (DMLA) est une maladie de
´ge
´ne
´rative de la re
´tine qui touche une
partie importante de la population a
ˆge
´e (> 25 % apre
`s 75 ans). Elle affecte principalement la vision centrale et pre
´cise
et repre
´sente un handicap de la vie quotidienne. L’influence du stress oxydant dans l’e
´tiologie et l’e
´volution de la
maladie est clairement e
´tablie. Nous de
´crivons les me
´canismes de de
´fenses contre l’apparition et l’e
´volution de la
DMLA ainsi que quelques supple
´mentations alimentaires pouvant les renforcer, notamment les vitamines C et E, les
oligoe
´le
´ments Zn, Se, Cu, la lute
´ine, et les Acides Gras Polyinsature
´sa
`Longue Chaine (AGPLC) de la se
´rie des
ome
´ga-3. Quelques essais cliniques acheve
´s ou en cours sont de
´crits.
Mots cle
´s:
de
´ge
´ne
´rescence maculaire lie
´ea
`l’a
ˆge, re
´tinopathie, stress oxydant, antioxydants, lute
´ine, acides gras
ome
´ga 3 polyinsature
´sa
`longue chaı
ˆne, supple
´mentation alimentaire
Abstract.
The age-related macular degeneration (AMD) is a degenerative disease of retina concerning an important
number of elderly (>25% over 75 years old). AMD mainly affects the central and precise view, and it is an everyday
handicap and disability. The role of oxidizing stress on the etiology and evolution of this disease is clearly established.
We describe defense mechanisms against the development of AMD and some food supplementations reinforcing such
defenses, like vitamins (C & E), oligo-elements (Zn, Se, Cu), lutein, and omega 3 polyunsaturated long chain fatty
acids. Some completed or ongoing clinical trials are described.
Key words:
age-related macular degeneration, retinal disease, oxidizing stress, antioxidants, lutein, omega 3 long chain
polyunsaturated fatty acids, food supplementation
Introduction
La DMLA ou dégénérescence maculaire liée à l’âge, est
selon l’OMS une maladie oculaire prioritaire, et qui tou-
che la vue de la personne âgée.
La DMLA est la 3
e
cause mondiale de déficience visuelle
(première cause dans les pays industrialisés) et représente
8,7 % des causes de cécité au monde.
La DMLA est la première cause de handicap visuel chez les
personnes de plus de 50 ans dans les pays développés.
Le risque de survenue de la maladie augmente avec l’âge
et dépasse 25 % de la population après 75 ans.
Elle touche 2 millions de personnes en France, majoritaire-
ment atteintes d’une forme peu sévère. Les formes sévères
concernent près de 150 000 à 200 000 Français.
Le principal facteur de risque en est donc l’âge. D’autres fac-
teurs de risque adjuvant sont incriminés, comme le taba-
gisme, l’influence génétique, le degré de pigmentation
(risqueplusimportantencasd’iris clair), l’hypertension arté-
rielle, les ultraviolets et un déséquilibre alimentaire.
L’œil a une place prépondérante dans la pathologie liée à
l’oxygène : il est exposé non seulement à des réactions
inflammatoires, mais également aux méfaits du soleil et
de la pollution atmosphérique.
Notre problématique est d’évaluer, au regard des propriétés
étiologiques de la DMLA, si des traitements de supplémenta-
tion peuvent garantir une prévention de la survenue de la
pathologie. Pour y répondre, nous allons étudier le rôle des
antioxydants, puis de la lutéine et enfin des oméga-3.
Premie
`re partie :
Physiopathologie de la DMLA
(de
´ge
´ne
´rescence maculaire lie
´ea
`l’a
ˆge)
Anatomie et physiologie de l’œil humain
L’œil humain est l’organe de la vision de l’homme. Il capte
la lumière puis interagit avec elle, ce qui nous permet de
distinguer les formes et les couleurs (figure 1).
L’organisation de l’appareil de la vision [1]
L’œil est constitué d’un globe oculaire, formé de 3 envelop-
pes ou tuniques : les tuniques externe, moyenne et interne.
Tunique externe
–la sclérotique (= blanc de l’œil), la plus résistante des
tuniques de l’œil. C’est la membrane de protection de
SYNTHE
`SE
J Pharm Clin 2010 ; 29 (2) : 61-87
doi: 10.1684/jpc.2010.0139
*Correspondance et tire
´sa
`part : A. Legrand
J Pharm Clin, vol. 29, n
o
2, avril-mai-juin 2010 61
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

l’œil, peu vascularisée, riche en collagène. Elle devient
transparente en avant pour donner la cornée ;
–la cornée principale lentille de l’œil. Elle assure la fonc-
tion de protection de l’œil contre les micro-organismes.
Tunique moyenne : l’uvée (membrane vasculaire,
nourricière)
–la choroïde est une membrane vascularisée disposée au-
tour de la rétine, assurant sa nutrition. Les cellules de cette
tunique renferment un pigment, la mélanine, qui lui donne
une couleur brun foncé, afin que les rayons ne pénètrent
que par la pupille ;
–l’iris donne la couleur de l’œil. Constituant le dia-
phragme de l’œil, jouant sur la quantité de lumière
entrant ;
–le corps ciliaire sécrète l’humeur aqueuse (figure 2).
Tunique interne ou membrane nerveuse (figure 3)
–La rétine ;
–La tache jaune ou macula ;
–Le point aveugle : point de sortie, où les fibres nerveuses
se réunissent pour former le nerf optique. Il ne comporte
pas de cellule photosensible.
Nous allons étudier plus en détail la rétine, siège de la
pathologie.
La re
´tine [1-4]
La rétine est la membrane la plus interne de l’œil, elle
tapisse entièrement l’œil y compris la face interne de
l’iris. Elle comporte deux régions particulières, la région
maculaire et l’ora serrata (zone située à l’intérieur du
globe oculaire, à proximité de l’iris et plus précisément
du bord ciliaire).
Organisation de la rétine
La rétine est essentiellement constituée de deux parties :
–l’épithélium pigmentaire reposant sur la membrane de
Bruch, et le neuroépithélium ;
–le neuroépithélium quant à lui, est constitué de 3 groupes
d’éléments suivants :
1. une chaîne de 3 neurones : cônes et bâtonnets, les
cellules bipolaires et les cellules ganglionnaires ;
2. des neurones d’association ;
3. les cellules gliales de soutien (tels que les astrocytes,
la glie paravasculaire, la microglie, et surtout les cellules
de Müller).
La stratification de ces trois groupes d’éléments réalise une
organisation en dix couches, détaillées sur la figure 4.
La choroïde
Le premier niveau est constitué par la choroïde.
Celle-ci comprend 2 structures :
–la lame choriocapillaire qui constitue la vascularisation
de l’ensemble de la rétine, permet l’apport des nutri-
ments ;
–la membrane de Bruch :ellenourritetoxygènel’ensemble
de la rétine. En effet, il existe des échanges métaboliques
très importants à travers cette membrane ; échanges avec la
rétine externe, l’épithélium pigmentaire et la choriocapil-
laire(étantlaprincipalesourcedenutriments).
La membrane de Bruch, constituée de phospholipides,
forme une barrière de filtration semi-perméable à travers
laquelle les nutriments passent de la choriocapillaire vers
les photorécepteurs, et les produits de dégradation cellu-
laire (déchets issus des réactions photochimiques) passent
dans la direction opposée. Cette membrane s’épaissit
naturellement avec l’âge. La membrane de Bruch semble
par ce phénomène contribuer à l’étiologie de la dégéné-
rescence maculaire liée à l’âge (DMLA).
La rétine et ses 10 couches successives
–(1) L’épithélium pigmentaire rétinien (EPR) : monocouche
de cellules rétiniennes (ayant des propriétés de cellules
Cornée
Cristallin
Iris
Conjonctive Rétine
Macula
Nerf optique
Figure 1. Physiologie de l’œil. Source : http://www710.univ-
lyon1.fr/~fdenis/club_EEA/images/oeil.jpg.
Corps
ciliares
Iris
Choroïde
Figure 2. Tunique moyenne. Source : http://tecfa.unige.ch/
staf/staf-g/glaus/staf14/ex8/images/oeil4.jpg.
Cristallin
Iris
Rétine
Sclère
Fovéa
Macula
Choroïde
Nerf
optique
Cornée
Rétine
Figure 3. Tunique interne. Source : http://www.vetopsy.fr/
sens/visu/images/oeil_ret.gif.
D. Couasnon, et al.
J Pharm Clin, vol. 29, n
o
2, avril-mai-juin 2010
62
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

épithéliales) et de granules pigmentaires (mélanine et
lipofuscine). Chaque cellule de cet épithélium sera en
contact avec au moins 25 bâtonnets ou cônes.
Il possède plusieurs rôles :
–l’absorption des rayons UV ;
–le maintien de la BHR (barrière hémato-rétinienne) ;
–la participation au cycle visuel (absorbe tous les photons
qui n’ont pas été captés par les photorécepteurs) ;
–la phagocytose des segments externes des photorécep-
teurs ;
–les apports de nutriments et métabolites à la rétine neu-
rosensorielle.
Cet épithélium a un rôle essentiel à la fois fonctionnel et
métabolique. Il a un rôle de transport, d’interface entre la
choroïde et le reste de la rétine par transports actif ou pas-
sif. Le transfert des métabolites tels que les acides gras
existe de la choroïde vers les photorécepteurs et inverse-
ment. L’EPR est l’élément essentiel à l’apport de nutriments
aux photorécepteurs. S’il se produit une défaillance au
sein de cet épithélium, telle qu’une rupture ou lésion, il y
aura un déficit dans ce mécanisme d’apport et de rejet au
niveau rétinien.
L’épithélium pigmentaire rétinien et les acides gras : l’épi-
thélium aurait la faculté de s’enrichir en DHA et de pro-
Choroïde
Lame
choriocapillaire
Lame de Bruch
Rétine
pigmentaire
1. Epithélium
pigmentaire
2. Photorécepteurs
3. Limitante externe
Bâtonnet
4. Noyaux ou
grains externes
5. Plexiforme
externe
Cellule horizontale
Cellule bipolaire
6. Noyaux ou
grains internes
Cellule amacrine
7. Plexiforme
interne
Cellule
ganglionnaire
8. Cellules
ganglionnaires
9. Fibres nerveuses
(nerf optique)
10. Limitante interne
Capillaire
rétinien
Cellule
de Müller
Astrocyte
100
µm
0 µm
200
µm
Cône
R
é
t
i
n
e
N
e
u
r
o
-
E
p
i
t
h
é
l
i
u
m
Couche
ganglionnaire
du nerf optique (II)
Couche
neuroépithéliale
Couche
ganglionnaire
de la rétine
L
U
M
I
E
R
E
Figure 4. Les différentes couches rétiniennes. Source : http://www.vetopsy.fr/sens/visu/images/ret_dessin.gif.
Pre
´vention de la de
´ge
´ne
´rescence maculaire lie
´ea
`l’a
ˆge
J Pharm Clin, vol. 29, n
o
2, avril-mai-juin 2010 63
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

duire des métabolites neuroprotecteurs. Il agirait comme
une « plaque tournante » du métabolisme des acides
gras pour la rétine et pourrait constituer une cible à privi-
légier dans le cadre d’une prévention nutritionnelle desti-
née à prévenir les pathologies oculaires liées au
vieillissement.
–(2) Les photorécepteurs (ou cellules visuelles) : ils servent
à décomposer les informations lumineuses en signaux
électriques, qui seront envoyés au nerf optique.
Il existe deux types de photorécepteurs : les cônes et les
bâtonnets (figure 5).
–Les cônes : environ 6 millions de cellules dans la rétine,
la plus grande concentration est dans la macula. Il existe
3 types différents de cônes servant à décomposer la lu-
mière en couleurs. On parle de 3 pigments rétiniens : io-
dopsine S pour le bleu, iodopsine M pour le vert et iodo-
psine L pour le rouge. Ils permettent une vision centrale
détaillée et la perception de la couleur.
–Les bâtonnets : environ 125 millions de cellules dans la
rétine. Ils sont responsables de la vision périphérique et de
la vision nocturne. Ils sont constitués d’un unique pigment
rétinien : la rhodopsine.
Les photorécepteurs requièrent une quantité importante
d’oxygène afin de transmettre les signaux au cerveau. En
métabolisant l’oxygène, les cellules produisent beaucoup
de déchets qui doivent être rejetés de manière efficace afin
que les cellules puissent fonctionner normalement. La livrai-
son d’oxygène et le rejet des déchets sont le travail de
l’épithélium pigmentaire rétinien, de la membrane de
Bruch et de la choroïde qui fonctionnent ensemble
comme une « unité sanitaire ».
–(4) La couche des grains externes : elle correspond aux
noyaux des cellules visuelles.
–(6) La couche des grains internes : elle est formée par les
corps cellulaires des cellules bipolaires, amacrines, hori-
zontales et de Müller.
–(5 et 7) Les couches plexiformes : constituent des synap-
ses entre les différentes cellules.
Vascularisation de la rétine
Cette vascularisation, artérielle et veineuse, est située dans
la couche des fibres ganglionnaires sous la limitante
interne.
Au niveau de la macula, il y existe une zone avasculaire
(la fovéa). Cette zone est entourée par un capillaire
continu ; par conséquent, dans cette partie avasculaire,
les échanges se font par l’intermédiaire de la choriocapil-
laire.
La région maculaire [5]
Dans cette région les cellules pigmentées sont les plus hau-
tes et les plus denses.
–La macula, située dans la rétine centrale est respon-
sable de la vision fine, nous permettant de lire, écrire, et
réaliser toutes les activités manuelles de détail. En effet,
elle est uniquement composée de cônes, assurant une mo-
tilité visuelle maximale. Par conséquent, dans la DMLA
seule la vision centrale est altérée ; la vision périphérique
étant conservée, du fait que les bâtonnets ne sont pas at-
teints.Les berges sont plus épaisses car elles comprennent,
en plus de la structure rétinienne normale, les éléments
d’association et de transmission qui manquent à la fovéa.
La plexiforme externe des berges est étirée oblique, nom-
mée « couche de Henlé ». C’est dans cette couche que se
collectent les œdèmes maculaires.
La lutéine est un pigment caroténoïde qui est concentré
dans la macula, donnant ainsi sa couleur jaune.
–La fovea, le centre de la macula, est constituée unique-
ment de cônes, et l’acuité visuelle y est donc maximale.
De
´ge
´ne
´rescence maculaire lie
´ea
`l’a
ˆge :
La physiopathologie
De
´finition [6-8]
La dégénérescence maculaire liée à l’âge (DMLA) est une
maladie dégénérative de la rétine d’évolution chronique
qui débute après l’âge de 50 ans (son diagnostic est sou-
vent fait 10 à 15 ans plus tard). Cette maladie correspond
à des lésions de la macula. Ces lésions sont : dégénérati-
ves, non inflammatoires, acquises, survenant sur un œil
auparavant normal, entraînant une altération de la vision
centrale. La vision périphérique ou latérale ne sont pas
atteintes.
Les de
´faillances physiopathologiques
a
`l’origine d’une DMLA [5, 9]
Avec le vieillissement, les cellules de l’épithélium pigmen-
taire rétinien se détériorent, causant un maillon faible dans
le processus « sanitaire rétinien ». Les cellules photorécep-
trices sont en manque d’oxygène, et ne peuvent plus
envoyer de signaux visuels au cerveau. Il y aura une dimi-
nution de la destruction des déchets qui vont s’accumuler
au niveau de l’œil. Cette accumulation de déchets
entraîne le dépôt de Drusen, précurseurs de la DMLA.
Une autre théorie suggère que les vaisseaux sanguins
sous-jacents, qui fournissent les nutriments et rejettent les
déchets de l’épithélium pigmentaire rétinien et des photo-
récepteurs, ne fonctionnent pas correctement. Par consé-
quent, il y aura un manque d’oxygène et accumulation
des déchets. Ce manque d’oxygène entraîne une hypoxie,
qui va induire la libération du VEGF (vascular endothelial
growth factor). Ce facteur de croissance vasculaire va
quant à lui induire la mise en place d’un mécanisme de
compensation par la formation de nouveaux vaisseaux
sanguins anormaux, on parle de néovascularisation cho-
roïdienne.
Aujourd’hui les mécanismes expliquant la formation de
ces néovaisseaux ne sont pas encore tous connus. En
A
Disques
Espace cytoplasmique
Segment
externe
Segment
externe Membrane
plasmique
Segment
interne
Segment
interne
Terminaison
synaptique
Terminaison
synaptique
Cône
Noyaux
Mitochondrie
Cils
Bâtonnet
Figure 5. Les photorécepteurs. Source : http://www.physio.
chups.jussieu.fr/vision1.pdf.
D. Couasnon, et al.
J Pharm Clin, vol. 29, n
o
2, avril-mai-juin 2010
64
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

revanche, le rôle du facteur de croissance VEGF dans le
développement de ces néovaisseaux est bien identifié.
Ces néovaisseaux sont à l’origine de décollements pig-
mentaires et d’hémorragies au niveau de la macula, qui
vont gêner la vision.
Les radicaux libres sont produits en grande quantité par la
macula, et neutralisés par les antioxydants. Malheureuse-
ment, l’organisme lorsqu’il est exposé à des facteurs
influençant, va produire un taux de radicaux libres supé-
rieur à ses besoins. Ces radicaux libres réagissent avec les
cônes des photorécepteurs dans la macula et produisent
une quantité anormale de déchets, qui s’accumulent et
entraînent un dysfonctionnement au niveau des cellules
photoréceptrices.
Les facteurs de risques [7, 10]
Les facteurs de risque les mieux identifiés de la DMLA sont
l’âge et le tabac.
–l’âge (personne de plus de 50 ans) est un facteur de
risque essentiel, contre lequel on ne peut évidemment
pas agir. La prévalence de l’apparition de la DMLA chez
les plus de 80 ans est de 30 % ;
–le deuxième facteur de risque reconnu est le tabac. Une
étude a montré l’augmentation de la fréquence de la
DMLA chez les fumeurs ; ce risque persiste jusqu’à
20 ans après l’arrêt du tabac. Les sujets fumant plus de
20 cigarettes par jour ont un risque de DMLA multiplié
par 2,5. Le tabagisme pourrait favoriser l’apparition de
néovaisseaux choroïdiens. Cependant des personnes
n’ayant jamais fumé de leur vie peuvent être atteintes de
DMLA ;
–l’hérédité intervient dans la survenue de la DMLA, même
si la probabilité de transmission aux descendants n’est
pas encore prouvée, au moins 3 gènes seraient impliqués.
La présence d’un seul allèle favorisant multiplie par 2 à
5 le risque d’être atteint. Le risque est supérieur à 80 %
avec 3 allèles favorisants ;
–l’alimentation est le facteur de risque que nous allons
étudier. Les patients atteints de DMLA seraient aussi ceux
ayant un régime faible en vitamines, minéraux et oligoélé-
ments ;
–la lumière : on a cru longtemps que les rétinopathies
étaient dues à une élévation de la température provoquée
par l’observation directe du soleil (notamment au cours
d’éclipse). On admet aujourd’hui que les effets solaires
rétiniens sont de nature photochimique et qu’ils ont pour
siège les photorécepteurs et l’épithélium pigmentaire de la
rétine. En effet, les photons de haute énergie détruisent
l’article externe des photorécepteurs. Ainsi, la rétine du
sujet âgé, protégée par un cristallin opacifié, devient dan-
gereusement exposée après chirurgie de la cataracte (les
cristallins artificiels présentent de mauvaises qualités
d’absorption des UV et de la lumière bleue). La différence
entre les pigments de l’épithélium pigmentaire rétinien que
sont la mélanine et la lipofushine, réside dans leurs taux.
La mélanine est un piège à radicaux libre alors que la
lipofushine ne l’est pas ; lors de la vieillesse la lipofushine
augmente, par conséquent on observe une forte concen-
tration de l’oxygène dans épithélium pigmentaire.
D’autres facteurs de risque tels que la couleur des yeux,
l’hypertension artérielle et l’obésité ont été évoqués, mais
àl’heure actuelle, ils ne sont pas confirmés.
Les formes cliniques [6-8, 11]
E
´tiologie de la DMLA
Dans le DMLA, la région maculaire présente deux anoma-
lies caractéristiques :
–apparition de Drusen : taches blanches dues à l’accu-
mulation de déchets lipidoprotéiques sous la rétine (figu-
res 6 et 7). Les Drusen sont des dépôts localisés de lipides
et lipoprotéines, secondaires à une accumulation de
déchets métaboliques dus à la destruction de cellules pho-
toréceptrices ;
–l’altérationde l’épithélium pigmentaire : les cellules épi-
théliales et photoréceptrices disparaissent et laissent la
placeàdesplagescicatriciellesauniveaudelarétine.
Lorsque ces plages cicatricielles vont se rejoindre, on parle
A
`retenir : les sympto
ˆmes qui doivent alerter
Une baisse de la sensibilité aux contrastes.
Une baisse d’acuité visuelle.
Une vision déformée ou gondolée.
Une apparition d’une tache centrale : un scotome.
fovea optic
nerve
Human retina
Figure 6. Rétine normale. Source : http://www.jordanseyes.
com/userimages/normal-retina.jpg.
DRUSEN
Figure 7. Drusen du pôle postérieur. Source : http://www.snof.
org/maladies/dmla.html.
Pre
´vention de la de
´ge
´ne
´rescence maculaire lie
´ea
`l’a
ˆge
J Pharm Clin, vol. 29, n
o
2, avril-mai-juin 2010 65
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
1
/
27
100%