Endocrinologie pédiatrique - saem: société algérienne d

Le must de l’ESPE
Paris 10-12 Septembre 2016
55° congrès de la société Européenne d ’endocrinologie pédiatrique
M.Bensalah,S.Ould-Kablia
Service d’endocrinologie
Hôpital central de l’armée

La thyroïde

Gènes impliqués dans la dysgénésie thyroïdienne
Pr Michel Polak.Paris
Thyroïde
NKX1
NKX2
Pax 8
Gènes impliqués dans la
DT peu nombreux
Formes monogéniques
<5%
FOX1-GLIS3

Borealine
Molécule impliquée dans
l’adhésion et la migration
cellulaire

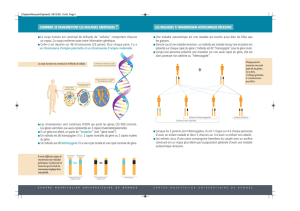
Boréaline et dysgénésie thyroïdienne
Buts Recherche de mutation
de la boréaline dans la
DT
Méthode
Séquençage des gènes d’une famille
consanguine avec HC puis chez une
cohorte de 136 avec DT
Résultats
Mutation faux sens homozygote p.S148F
(sœur avec ectopie T et une autre avec
hémi agénésie)
Mutation hétérozygote p.R114W (ectopie
thyroïdienne) et p.L177W(athyréose)
Pas d’altération des
mitoses des cellules
thyroïdiennes
Mais une diminution
significative de la
migration et de
l’adhésion des cellules
thyroïdiennes
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
1
/
44
100%