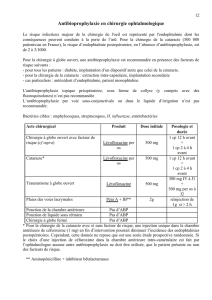
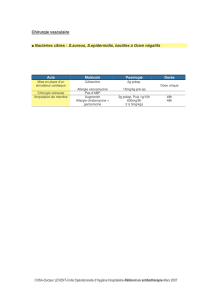
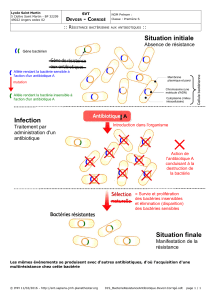
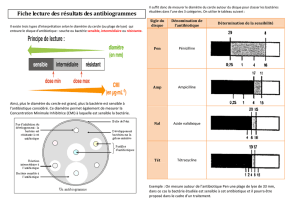
Antibioprophylaxie chirurgicale

Antibioprophylaxie
chirurgicale : quoi de neuf en 2010 ?
Joseph HAJJAR
Service d’hygiène et d’épidémiologie
Valence

Rappel
•Burke, 1961
–Démonstration sur modèle animal de l’efficacité de l’ABP si
débutée avant l'intervention
•Vachon, 1984
–L’ABP a pour objectif de « Participer à la réduction en
fréquence et en gravité d'un risque d'infection
hypothétique mais précis, lié à une intervention
chirurgicale donnée »
2

1. Justification de l’ATP
•L’infection, un risque permanent en chirurgie
–Contamination du site opératoire par des bactéries
•Flore propre du patient et sources exogènes
•Dans 90 % des plaies opératoires lors de la fermeture
•Quels que soient la technique et l’environnement
•Différents facteurs favorisant la prolifération
3

1. Justification de l’ATP
•L’infection, la complication postopératoire la plus
fréquente
–Toutes chirurgies confondues, taux brut d’ISO estimé à 2%,
à rapporter aux 7 millions annuels d’opérés et pour un coût
moyen par infection de 3000 €(France)
4

1. Justification de l’ATP
•L’antibioprophylaxie, technique validée
–S’oppose àla prolifération bactérienne
–Fait partie des mesures préventives, mais…à condition de
respecter
•Ses indications
ET
•Ses règles de prescription
ET
•Les autres mesures préventives
5
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
1
/
23
100%