2. Les pathologies infectieuses – Dr Legout

RISQUEINFECTIEUXET
ENVIRONNEMENT
LLEGOUT,
SERVICEDEMALADIESINFECTIEUSES
CHALPES‐LÉMAN

AUCUN CONFLIT D’INTERETS AVEC LA PRÉSENTATION

RISQUE INFECTIEUX ET ENVIRONNEMENT
• Environnement = air; eau non traitée (réseau), eau traitée (soins spécifiques),
surfaces, dispositifs médicaux, linge, aliments, déchets
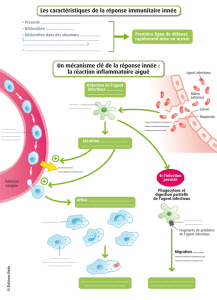
• Risque infectieux environnemental:
• Microorganismes présents variés: bacteries, virus, levures, champignons,
parasites
• Certaines sources environnementales peuvent être à l’origine d’épidémie ex:
aspergillose, légionellose
=> La maitrise de l’environnement hospitalier est indispensable pour protéger les
patients et le personnel.

RISQUE INFECTIEUX ET ENVIRONNEMENT
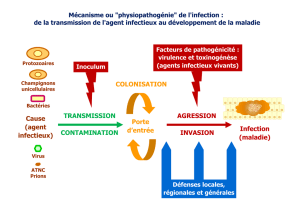
•Déclaration de l’infection:
• Dépend de la virulence du germe (ex:
streptocoque du groupe A toxinogene), de sa
quantité (shigelle…)
• Mode de contamination (hydrique, aérienne,
par contact)
• Réceptivité de l’hôte
• Etat immunitaire : maladie hémato, ttt
immunosuppresseur, corticothérapie,
chimiothérapie, cancer actif…
• Co-morbidités actives; age, dénutrition
• Contexte de réanimation, chirurgie ( multiples
KT, ventilation, dialyse, denutrition….)
• Arbre respiratoire malade soit lors d’une
agression aigue comme la grippe, soit lors
d’une agression chronique comme le tabac…

QUELS MICROORGANISMES ?
•Bactéries
• Origine humaine: staphylocoque doré, enterobacteries, enterocoque
• Dont certaines résistantes: staphylocoque doré methi-R, enterobacteries BLSE,
enterocoque resistant à l’ampicilline
• Origine environnementale: bacille à gram négatif et mycobacterie atypique (xenopi
• Dont Pseudomonas, Acinetobacter baumanii, Stenotrophomonas maltophilia, legionnella
• Existence de multi-résistance
•Champignons:
• Aspergillus bien adapté à la survie et à la multiplication dans l’environnement
• Cryptocoque (fiente de pigeons…)
•Virus:
• Rotavirus , VRS, grippe
• Peuvent contaminer l’environnement à partir du réservoir humain
• VRS survit 6h, rotavirus 10j
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
1
/
35
100%