Injection intravitréenne : complications et réalisation

Littérature
Images en Ophtalmologie
•
Vol. II
•
n° 1
•
janvier-février-mars 2008
29
Coup d’œil
Injection intravitréenne : complications et réalisation
V. Sarda, C. Rohart, G. Chaine
(Service d’ophtalmologie, hôpital Avicenne, Bobigny)
Depuis la première injection intravitréenne au début du
siècle dernier, cette intervention n’a fait que croître
en nombre et en diversité. Plus récemment, il s’agis-
sait d’injections d’antiviraux dans le cadre de rétinites chez
les patients immunodéprimés. Cette voie d’administration
a permis d’augmenter la concentration locale par injection
directe tout en réduisant les effets indésirables systémiques
sévères de ces traitements.
Le vieillissement de la population est responsable d’une
augmentation considérable des pathologies dégénératives,
comme la dégénérescence maculaire liée à l’âge (DMLA), et,
à un moindre degré, des pathologies vasculaires rétiniennes
(maculopathie diabétique, occlusion veineuse). De nombreuses
approches thérapeutiques ont été proposées dans ces maladies
du segment postérieur, parmi lesquelles l’injection intravi-
tréenne.
Les complications sont rares après injection intravitréenne mais
doivent être connues en raison de leur gravité. Une technique
de réalisation et une asepsie rigoureuses sont nécessaires pour
prévenir ces complications potentiellement cécitantes.
Historique
Au début du XXe siècle, on injectait de l’air en intravitréen pour
réaliser un tamponnement interne, puis apparurent les antibio-
tiques pour le traitement des endophtalmies et les antiviraux
pour les rétinites virales des sujets immunodéprimés. Dans
ces deux dernières indications, la voie intravitréenne a fait la
preuve d’une efcacité remarquable. Les indications pour le
traitement des lymphomes et des hémorragies maculaires
sont plus anecdotiques.
Dans cet article, nous développerons les complications liées à
ces injections et les recommandations autour du geste d’injec-
tion de triamcinolone et d’anti-VEGF dans des indications plus
récentes.
Complications graves
liées à l’injection intravitréenne
L’endophtalmie
Il s’agit de la complication la plus grave en ophtalmologie.
Elle est rare mais potentiellement cécitante. Après injection
intravitréenne, sa fréquence varie de 0,1 % à 0,3 % selon les
études
(1-3)
. Ce taux est comparable à celui des endophtalmies
✔
après chirurgie de la cataracte
(4)
. Le risque d’endophtalmie
est diminué par un geste en asepsie dans le respect des bonnes
pratiques. Un non-respect des protocoles d’asepsie explique-
rait 67 % des endophtalmies
(5)
.
Par ailleurs, des facteurs de risque d’endophtalmies ont été
identiés : patients présentant une infection ou une inam-
mation locale pendant le geste, porteurs de lentilles, sujets
immunodéprimés, diabétiques ou atteints d’infections respi-
ratoires. Cependant, il est important de rappeler que cette
complication peut survenir chez tous les patients
(6)
.
L’endophtalmie semble plus fréquente dans les cas d’injection
intravitréenne de triamcinolone
(7)
. Une étude regroupant les
effets indésirables après injections intravitréennes de 1966
à 2004 a montré une prévalence de l’endophtalmie de 0,3 %
toutes injections confondues, de 0,1 % pour les injections d’anti-
viraux, et de 0,6 % pour les injections de triamcinolone après
exclusion des pseudo-endophtalmies
(2)
.
Les germes retrouvés sur les prélèvements bactériologiques au
cours des endophtalmies sont le plus souvent des germes de
la ore conjonctivale normale ou des annexes (staphylocoque
coagulase-négative, streptocoque). Ils sont inoculés en intra-
vitréen au cours de l’injection ou en postopératoire précoce.
Une désinfection du site d’injection avant le geste doit être
réalisée avec soin. La polividone iodée est la seule molécule
ayant montré son efcacité pour réduire le taux d’endophtal-
mies
(8, 9)
.
Les prélèvements bactériologiques effectués lors du diagnostic
d’endophtalmie sont positifs dans 60 % des cas et permettent,
si le germe est identié, la mise en route d’une antibiothérapie
adaptée.
La pseudo-endophtalmie
La pseudo-endophtalmie est spéciquement liée à l’injection de
triamcinolone et complique 0,3 % des injections intravitréennes
de triamcinolone
(2)
. Elle apparaît dans les 3 premiers jours
suivant l’intervention. La pseudo-endophtalmie se distingue
cliniquement de l’endophtalmie par un œil peu rouge et non
douloureux. L’inflammation intraoculaire est sévère, avec
souvent un hypopion. Il s’agit d’une inammation stérile. Son
évolution est favorable, avec une résolution complète en moins
de deux semaines. Ces pseudo-endophtalmies se présentent
plus fréquemment sur des yeux ayant des antécédents de
chirurgie intraoculaire (œil vitrectomisé, pseudophake ou
aphake). La distinction clinique entre une endophtalmie et
une pseudo-endophtalmie n’est pas toujours facile. Un facteur
✔
IO-NN1-0108.indd 29 19/03/08 11:15:10

Littérature
Images en Ophtalmologie
•
Vol. II
•
n° 1
•
janvier-février-mars 2008
30
Coup d’œil
déterminant pour le diagnostic différentiel est le délai d’ap-
parition, qui est habituellement inférieur à 3 jours pour les
pseudo-endophtalmies
(1, 10-12)
.
Les infections virales
Récemment, des cas isolés de rétinites virales après injection
de triamcinolone ont été recensés. Dans la littérature, quatre
cas de rétinites à cytomégalovirus (CMV) ont été diagnostiqués
dans les mois suivant une injection intravitréenne de triam-
cinolone associée à une vitrectomie
(13-15)
. Ces patients ne
présentaient aucune immunodépression, ni signes systémiques
d’infection à CMV. Ces cas sont documentés par des prélève-
ments biologiques sans co-infection virale (les patients étaient
négatifs pour les autres virus). Dans tous ces cas rapportés, le
traitement général et local par ganciclovir a été actif.
De plus, un cas de nécrose rétinienne herpétique suivant
une injection intravitréenne de triamcinolone en dehors d’un
contexte d’immunosuppression a été publié
(16)
.
L’hémorragie intravitréenne, l’hémorragie rétinienne et
hyphéma
L’hémorragie intravitréenne peut survenir de façon occasion-
nelle après injection intravitréenne. Sa fréquence est de 0,2 %
à 1,3 %
(2)
. Elle apparaît immédiatement après l’injection et
se résorbe habituellement spontanément dans les semaines
ou mois suivants. Une vitrectomie peut être proposée dans les
cas où l’hémorragie ne disparaît pas dans des délais raison-
nables. Elle survient plus fréquemment après injection de TPA
ou de hyaluronidase
(17, 18)
. Une hémorragie rétinienne et
un hyphéma peuvent également se déclarer après injection
intravitréenne.
Le décollement de rétine
Après injection intravitréenne, il est exceptionnel. Sa fréquence
varie de 0,04 % à 0,9 % selon les études
(2, 19)
. Il survient dans
un contexte pathologique particulier. Il est retrouvé après des
injections intravitréennes d’antiviraux sur rétinites à CMV
avec nécrose rétinienne ou en présence d’une rétinopathie
diabétique proliférante avec traction.
L’uvéite
L’uvéite postinjection intravitréenne a également été décrite.
Sa fréquence est de 0,14 %
(19)
toutes injections confondues.
Cette fréquence augmente après des injections de cidofovir,
fomivirsen et hyaluronidase (6,3 %
[2]
). Elle atteint 26,9 % des
injections intravitréennes de cidofovir pour rétinite à CMV
et 38,2 % pour le fomivirsen
(2)
.
L’hypertension oculaire
Après injection de triamcinolone, elle varie de 21 % à
52 %
(2, 20)
selon le seuil de pression intraoculaire xé dans
les études.
L’hypertension oculaire peut suivre rapidement l’injection. Le
mécanisme peut être directement lié à la triamcinolone, ou indi-
rectement par un dépôt obstructif sur le trabéculum
(21, 22)
.
✔
✔
✔
✔
✔
La répétition des injections ne favorise pas l’hypertension
oculaire, mais les patients ayant présenté une augmentation
signicative de la pression oculaire après la première injection
sont plus exposés aux risques de récidives d’une hypertonie
lors d’injections ultérieures.
Les patients ayant des facteurs de risque de développer
une hypertension intraoculaire après triamcinolone sont les
patients glaucomateux (avec une incidence de 66 % d’aug-
mentation de la pression oculaire supérieure à 21 mmHg
[23]
)
et les sujets jeunes. Ce facteur de risque reste cependant
discuté.
Les collyres hypotonisants sont le plus souvent sufsants pour
assurer un bon contrôle tensionnel. Les hypertensions sévères
nécessitant une chirurgie ltrante (ou une vitrectomie pour
ablation de la triamcinolone) ne concernent que 1 % de ces
patients
(23)
.
Par ailleurs, l’hypertension oculaire après injection intravi-
tréenne entraîne un risque non négligeable d’occlusion vascu-
laire rétinienne.
L’occlusion de l’artère centrale de rétine
Elle est exceptionnelle (entre 1 et 3 cas dans certaines
études
[2, 3, 19]
), mais potentiellement grave pour l’acuité
visuelle nale. Il est important de s’assurer de la présence
d’une perception lumineuse immédiatement après l’injec-
tion. L’occlusion survient par un mécanisme de compression
locale. Lorsque l’on injecte un volume de liquide dans un œil
non expansif, la pression augmente et peut comprimer l’artère
centrale de la rétine. Un dépistage précoce de l’occlusion est
effectué par la recherche d’une perception lumineuse juste
après l’injection. En son absence, une ponction de la chambre
antérieure doit être réalisée en urgence.
Des occlusions ou hémi-occlusions de la veine centrale de la
rétine ont également été décrites [2].
La cataracte
Elle peut être liée soit à l’injection (complication post-trau-
matique due à la technique), soit au principe actif (triamci-
nolone). Secondaire au geste, elle survient après contact
direct de l’aiguille avec le cristallin lors de l’injection et est
exceptionnelle (0,01 %
[19]
). De façon plus courante, une cata-
racte peut apparaître ou progresser par toxicité directe de
la triamcinolone, en particulier en cas d’injections multiples
(cataracte cortisonique). La fréquence de cette cataracte est
de 9,9 % après injection de triamcinolone et de 1,8 % toutes
molécules confondues
(2)
.
Les réactions d’hypersensibilité et d’anaphylaxie
Elles sont dues au produit injecté (
rash
cutané, œdème de
Quincke, bronchospasme, choc). L’interrogatoire préinjection
doit toujours éliminer une allergie connue au principe actif
ou à ses conservateurs. Une courte surveillance générale du
patient après injection et la présence, en salle, de matériel
d’urgence d’injection intravitréenne permettent d’intervenir
en cas de détresse vitale imminente.
✔
✔
✔
IO-NN1-0108.indd 30 19/03/08 11:15:11

Littérature
Images en Ophtalmologie
•
Vol. II
•
n° 1
•
janvier-février-mars 2008
31
Coup d’œil
Les risques cardiovasculaires
Les risques cardiovasculaires des anti-VEGF intravitréens
doivent être pris en considération, d’autant plus que les injec-
tions sont itératives sur une période plus ou moins prolongée,
et qu’il s’agit en général de patients âgés, souvent atteints
de pathologies cardiovasculaires. Bien que les doses d’anti-
VEGF injectées en intravitréen soient plus faibles que les
doses injectées en intraveineux, et qu’il y ait une séquestration
partielle dans l’œil, la demi-vie de ces molécules (à l’exception
du ranibizumab) est longue. Les concentrations sériques de
pégaptanib et de ranibizumab sont inférieures à celles esti-
mées par la FDA (Food and Drug Administration) pour inhiber
l’activité du VEGF de 50 % (11-27 ng/ml). Cependant, la concen-
tration sérique du bévacizumab est sensiblement supérieure
à ce seuil.
Dans tous les cas, les concentrations sériques de ces trois
agents après injection sont inférieures au taux physiologique
du VEGF chez l’homme.
Les données de la littérature n’ont pas mis en évidence de
différence signicative en termes d’accidents cardiovascu-
laires entre les patients ayant reçu une injection et les groupes
contrôles, malgré l’augmentation marginale mais non signi-
cative chez les sujets traités par ranibizumab.
Une étude de 2005 regroupant les effets systémiques après
injection d’Avastin® a retrouvé des cas d’hypertension arté-
rielle, de thrombose veineuse, d’accident vasculaire cérébral
transitoire ou constitué et d’infarctus du myocarde. Ces événe-
ments n’étaient pas statistiquement signicatifs
(19)
.
Autres complications liées à l’injection
intravitréenne
D’autres effets indésirables plus bénins mais aussi plus
fréquents peuvent survenir lors d’injections intravitréennes.
On retrouve des hémorragies sous-conjonctivales (0,03 %
[19]
),
des ulcérations de cornée (0,15 %
[19]
), des douleurs oculaires,
des corps ottants vitréens, une sensation de corps étranger,
des troubles visuels, une hyperhémie oculaire, une réaction
au point d’injection, un prurit et une conjonctivite. Les patients
doivent être informés de ces effets.
Molécules injectées
Les premières molécules injectées en intravitréen ont été les
antibiotiques. C’est le début du traitement de l’endophtalmie
par antibiotique directement injecté au site d’infection. Après
les antibiotiques, les antiviraux, injectés en intravitréen, ont
été utilisés pour le traitement des rétinites à CMV. D’autres
molécules comme le TPA et la hyaluronidase ont été injectées
de la même façon dans le cadre de pathologies spéciques du
segment postérieur.
✔
La triamcinolone en intravitréen connaît un grand essor
dans les années 1990. Elle présente de bons résultats dans
les maculopathies œdémateuses. Elle s’injecte sous la forme
de Kénacort® avec du carboxyméthylcellulose et de l’alcool
benzylique en conservateur. Sa demi-vie est de 18,6 jours
dans un œil non vitrectomisé et de 3,2 jours si l’œil est
vitrectomisé. Elle s’utilise fréquemment pour les œdèmes
maculaires liés au diabète, à une occlusion veineuse centrale
de la rétine, à une uvéite ou pour les œdèmes maculaires
idiopathiques
(24-26)
.
Plus récemment, des inhibiteurs de l’angiogenèse ont été déve-
loppés autour de la DMLA
(27-29)
.
Le pégaptanib (Macugen®) a obtenu l’AMM européenne en
janvier 2006 dans le traitement de la forme néovasculaire de
la DMLA. C’est un aptamère qui se xe et bloque le VEGF. Il est
sélectif pour l’isoforme A 165 (étude VISION).
Le ranibizumab (Lucentis®) est indiqué dans le traitement
de la forme néovasculaire de la DMLA. C’est un fragment
d’anticorps monoclonal humanisé recombinant dirigé contre
le facteur de croissance de l’endothélium vasculaire humain de
type A de haute afnité pour l’isoforme VEGF A 165 et l’isoforme
VEGF A 121 (étude MARINA).
Le bévacizumab (Avastin
®
) n’a pas d’AMM en ophtalmologie.
Initialement, c’est un traitement utilisé dans le cancer colo-
rectal. C’est un anticorps monoclonal bloquant le VEGF.
Depuis leur indication dans le traitement de la DMLA, les
inhibiteurs de l’angiogenèse ont montré leur efcacité dans
d’autres pathologies néovasculaires. Dans la littérature et en
pratique, on retrouve des régressions de rubéoses iriennes
d’origine diabétique, d’occlusions veineuses ou de rétinopathies
d’irradiations.
Ces injections ouvrent la voie à de nouvelles thérapies curatives
en ophtalmologie dans des pathologies auparavant sans pers-
pective d’amélioration. Cependant, à ce jour, les effets indé-
sirables locaux et systémiques à long terme de ces nouvelles
molécules injectées à répétition chez l’homme ne sont pas
connus.
Recommandations autour du geste d’injection
Face à l’essor de la pratique des injections intravitréennes et
en raison des complications qui peuvent être sévères et céci-
tantes, de bonnes pratiques ont été instituées pour encadrer
leur réalisation.
Après le Comité de lutte contre les infections nosocomiales
(Clin), l’Agence française de sécurité sanitaire des produits de
santé (Afssaps) a émis des recommandations pour diminuer le
taux de complications des injections intravitréennes.
•
•
•
•
IO-NN1-0108.indd 31 19/03/08 11:15:11

Littérature
Images en Ophtalmologie
•
Vol. II
•
n° 1
•
janvier-février-mars 2008
32
Coup d’œil
Ces recommandations concernent :
Le lieu de l’acte : il faut une salle dédiée à l’injection intravi-
tréenne, peu encombrée, bien éclairée, aux murs et sols lisses.
Le dépoussiérage doit être humide et régulier ; les fenêtres et
la porte doivent rester fermées, sans ventilation, pour éviter les
turbulences. Un matériel d’urgence doit toujours être acces-
sible. Un système de lavage des mains, bien entretenu, doit
être présent.
Les contre-indications doivent être recherchées et élimi-
nées avant les injections intravitréennes. En cas d’infection
oculaire ou des annexes, le geste est contre-indiqué, sauf en
cas d’injection intravitréenne pour endophtalmie (prélève-
ments, injection d’antibiothérapies). Le glaucome et l’hyper-
tonie oculaire ne sont pas des contre-indications à l’injection
intravitréenne (même en cas d’injections de triamcinolone)
mais doivent être traités et équilibrés. Le fond d’œil avec
•
•
examen de la périphérie est réalisé an de dépister et de traiter
les lésions périphériques à risque de décollement de rétine
avant l’injection. L’interrogatoire à la recherche d’allergies est
indispensable avant toute prescription médicamenteuse. La
prise d’anticoagulants et d’antiagrégants plaquettaires n’est
pas une contre-indication. Cependant, si le patient présente
un INR supérieur à 5 (index surveillant les patients sous anti-
coagulants), l’injection intravitréenne est déconseillée, car il
y a un risque hémorragique important.
L’information et le consentement libre et éclairé du patient
sont indispensables. Il est nécessaire d’expliquer les risques
et les bénéces liés à l’injection et à son produit. Une che
explicative de la Société française d’ophtalmologie
(encadré)
et le consentement signé doivent être remis avant la pratique
du geste. Le patient doit être prévenu du risque de vision oue
temporaire après l’injection. Par conséquent, il ne doit pas
conduire tant que sa vision n’est pas redevenue normale, et il
•
Encadré. Fiche d’information n° 65 (Sfo-Snof) relative à l’injection intravitréenne.
Madame, mademoiselle, monsieur,
Vous présentez une pathologie oculaire
pour laquelle votre ophtalmologiste vous
propose une injection de substance(s)
médicamenteuse(s) à l’intérieur de votre œil.
Cette fiche contient des informations sur
l’intervention qui vous est proposée.
Pourquoi réaliser cette injection ?
L’injection de substances médicamenteuses
directement à l’intérieur de l’œil permet dans
certains cas une action très efficace sur la
maladie oculaire à traiter, tout en minimisant
les eets indésirables généraux.
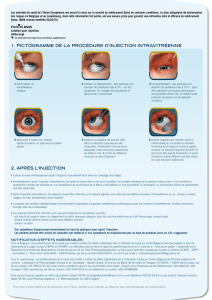
Description de l’intervention
Elle est réalisée en position allongée sur le dos
ou demi-assise.
– Anesthésie : l’œil est insensibilisé par l’ins-
tillation de collyre anesthésiant.
– Désinfection : les paupières et la surface
oculaire sont désinfectées avec un produit anti-
septique pour diminuer le risque d’infection.
– Installation : le visage est recouvert par un
champ opératoire stérile, et un écarteur à
paupières stérile est mis en place.
– Injection intravitréenne : l’injection ne dure
que quelques secondes. On utilise une aiguille
très ne introduite à travers la sclère (blanc de
l’œil), à un endroit précis où l’on peut péné-
✓
✓
trer dans l’œil sans danger pour les structures
oculaires.
– Après l’injection : une instillation de collyre
antibiotique est réalisée.
Évolution postopératoire habituelle
– L’œil traité reste indolore dans la très grande
majorité des cas.
– Selon le produit injecté, il peut arriver de
voir quelques taches dans le champ visuel,
pendant quelques heures à quelques jours,
correspondant à la présence du produit dans
le vitré (le gel transparent qui remplit l’œil
derrière le cristallin). Les taches se résorbent
habituellement en quelques jours ou quel-
ques semaines, mais peuvent persister.
– L’efficacité du médicament injecté sera
évaluée ultérieurement par votre ophtalmo-
logiste.
Complications
Des complications peuvent survenir et être
transitoires ou dénitives. Elles peuvent néces-
siter un traitement médical ou chirurgical.
La complication la plus fréquente est sans
conséquence. Il s’agit de l’hémorragie sous-
conjonctivale (le blanc de l’œil devient rouge
au niveau de l’injection), qui se résorbe spon-
tanément en quelques jours.
✓
✓
Les autres complications sont très rares, et
peuvent survenir malgré les précautions rigou-
reuses prises par le médecin. Exceptionnelle-
ment, et comme pour toute chirurgie oculaire,
elles peuvent prendre un caractère de gravité
pouvant conduire à une perte de la vision, et,
dans les cas les plus rares, à la perte de l’œil :
– infection qui se manifesterait par une baisse
de la vision, des douleurs et une rougeur de
l’œil. Si vous perceviez ces symptômes dans
les heures ou les jours qui suivent l’injection,
contactez immédiatement votre ophtalmo-
logiste ou le centre hospitalier le plus proche
pour être pris en charge sans retard ;
– élévation de la pression intraoculaire, néces-
sitant un traitement médical ou chirurgical ;
– lésion du cristallin à l’origine d’une cata-
racte ;
– hémorragie intravitréenne ;
– décollement de rétine.
Votre ophtalmologiste est disposé à répondre
à toute question complémentaire que vous
souhaiteriez lui poser.
Les dispositions réglementaires font obli-
gation au médecin de prouver qu’il a fourni
l’information au patient. Aussi vous demande-
t-on de signer ce document, dont le double
est conservé par votre médecin.
Je soussigné ................................................................................................. reconnais que la nature de l’injection, ses bénéces ainsi que ses
risques m’ont été expliqués en termes que j’ai compris, et qu’il a été répondu de façon satisfaisante à toutes les questions que j’ai
posées.
J’ai disposé d’un délai de réexion susant et :
❏ donne mon accord pour la réalisation de l’acte qui m’est proposé.
❏ ne donne pas mon accord
Date et signature
IO-NN1-0108.indd 32 19/03/08 11:15:12

Littérature
Images en Ophtalmologie
•
Vol. II
•
n° 1
•
janvier-février-mars 2008
33
Coup d’œil
est préférable qu’il soit accompagné. Des conseils pour réduire
le risque infectieux doivent être donnés, comme celui de ne pas
porter de lentilles la semaine précédant l’injection, de ne pas
se maquiller, de prendre une douche et de se laver les cheveux
avant l’intervention.
Le patient : il porte masque, charlotte, blouse à usage
unique, surchaussures ; il doit être installé confortablement
en décubitus dorsal.
L’opérateur : il est expérimenté, porte charlotte, masque,
surchaussures, blouse à usage unique ; il procède à une
désinfection chirurgicale des mains (solution hydro-alcoolisée)
et s’équipe de gants stériles.
Le matériel : sa traçabilité est assurée, il est à usage unique,
sa préparation doit être stérile et réalisée sur la table avec
asepsie, champ stérile, compas, pince à griffe, blépharostat,
coton-tige, compresses stériles, cupules. La seringue du médi-
cament est stérile, possédant une aiguille de 27 ou 30 gauges.
Le geste : il s’effectue sous anesthésie locale, après désin-
fection à la povidone iodée ophtalmologique périorbitaire, des
paupières, des cils, du cul-de-sac oculaire et du site d’injection.
Il n’y a pas de massage oculaire. L’injection se fait (un seul œil
à la fois) entre 3,5 et 4 mm du limbe, en décalant la conjonctive
du point d’entrée scléral, perpendiculairement à l’entrée puis
en direction du centre du globe. Le retrait doit être lent ; s’ensuit
l’application d’un coton-tige quelques secondes pour diminuer
le reux.
Une antibiothérapie locale postinjection immédiate et
les 3 jours suivants est recommandée. En revanche, en ce
qui concerne les précautions à observer avant l’injection,
seul un antiseptique local les 3 jours précédant le geste est
recommandé. Les antibiotiques préopératoires diminuant
les bactéries de la ore conjonctivale (retrouvées dans les
endophtalmies) sont fréquemment prescrits, mais ils restent
controversés. L’association de povidone iodée à un antibiotique
local permettrait une stérilisation locale de 83 %, contre 40 %
pour la povidone iodée seule et 31 % pour l’antibothérapie
seule
(30)
.
La surveillance postinjection est immédiate et consiste à
vérier la présence d’une perception lumineuse. Il existe en
effet un risque rare mais grave d’occlusion de l’artère centrale
de la rétine par hyperpression locale nécessitant une ponction
de la chambre antérieure si elle persiste quelques minutes. Par
ailleurs, une surveillance générale immédiate est requise pour
éliminer une réaction anaphylactique au produit injecté. Une
surveillance ophtalmologique à une semaine (acuité visuelle,
tension oculaire et fond d’œil pour éliminer les complications)
et à 4 semaines (pour évaluer l’effet thérapeutique) est néces-
saire. Dans les suites précoces du geste, un contact télépho-
nique avec le patient peut sufre si ce dernier est prévenu des
signes d’alarme des complications.
•
•
•
•
•
•
Le respect des bonnes pratiques encadrant la procédure
d’injection et la prescription médicamenteuse diminue la
fréquence des complications survenant dans les suites d’une
injection intravitréenne.
II
Références bibliographiques
1.
JonasJB,SpandauUH,RenschF,vonBaltzS,SchlichtenbredeF.Infec-
tiousandnoninfectiousendophthalmitisafterintravitrealbevacizumab.JOcul
PharmacolTher2007;23(3):240-2.
2.
JagerRD,AielloLP,PatelSC,CunninghamETJr.Risksofintravitreous
injection:acomprehensivereview.Retina2004;24(5):676-98.
3.
BaathJ,EllsAL,CrichtonA,KheraniA,WilliamsRG.Safetyproleofintra-
vitrealtriamcinoloneacetonide.JOculPharmacolTher2007;23(3):304-10.
4.
SandvigKU,DannevigL.Postoperativeendophthalmitis:establishment
andresultsofanationalregistry.JCataractRefractSurg2003;29(7):1273-80.
5.
GragoudasES,AdamisAP,CunninghamETJr,FeinsodM,GuyerDR;
VEGF InhibitionStudy inOcular Neovascularization Clinical Trial Group.
Pegaptanibforneovascularage-relatedmaculardegeneration.NEnglJMed
2004;351(27):2805-16.
6.
ScottIU,FlynnHWJr.Reducingtheriskofendophthalmitisfollowingintra-
vitrealinjections.Retina2007;27(1):10-2.
7.
MoshfeghiDM,KaiserPK,ScottIUetal.Acuteendophthalmitisfollowingintra-
vitrealtriamcinoloneacetonideinjection.AmJOphthalmol2003;136(5):791-6.
8.
TaCN.Minimizingtheriskofendophthalmitisfollowingintravitreousinjec-
tions.Retina2004;24(5):699-705.
9.
SpeakerMG,MenikoffJA.Prophylaxisofendophthalmitiswithtopicalpovi-
done-iodine.Ophthalmology1991;98(12):1769-75.
10.
RothDB,ChiehJ,SpirnMJ,GreenSN,YarianDL,ChaudhryNA.Nonin-
fectiousendophthalmitisassociatedwithintravitrealtriamcinoloneinjection.
ArchOphthalmol2003;121(9):1279-82.
11.
SutterFK,GilliesMC.Pseudo-endophthalmitisafterintravitrealinjection
oftriamcinolone.BrJOphthalmol2003;87(8):972-4.
12.
NelsonML,TennantMT,SivalingamA,RegilloCD,BelmontJB,MartidisA.
Infectiousandpresumednoninfectiousendophthalmitisafterintravitreal
triamcinoloneacetonideinjection.Retina2003;23(5):686-91.
13.
FurukawaM,KumagaiK,OginoN,OkinamiS,UemuraA,LarsonE.Cytome-
galovirusretinitisafterintravitreoustriamcinolonetreatmentofavitrectomized
eyeinanimmunocompetentpatient.RetinalCasesandBriefReports2007.
14.
HsuJ,ChenE,VanderJF.Cytomegalovirusretinitisaftertreatmentwith
intravitrealtriamcinoloneacetonideinanimmunocompetentpatient.Retinal
CasesandBriefReports2007.
15.
SaidelMA,BerreenJ,MargolisTP.Cytomegalovirusretinitisafterintra-
vitreoustriamcinoloneinanimmunocompetentpatient.AmJOphthalmol
2005;140(6):1141-3.
16.
SiskRA,HutchinsRK.Necrotizingherpeticretinopathyafterintravitreal
triamcinoloneacetonideinjection.RetinalCasesandBriefReports2007.
17.
HattenbachLO,KlaisC,KochFH,GumbelHO.Intravitreousinjectionof
tissueplasminogenactivatorandgasinthetreatmentofsubmacularhemor-
rhageundervariousconditions.Ophthalmology2001;108(8):1485-92.
18.
LaheyJM,FongDS,KearneyJ.Intravitrealtissueplasminogenactivatorfor
acutecentralretinalveinocclusion.OphthalmicSurgLasers1999;30(6):427-34.
19.
FungAE,RosenfeldPJ,ReichelE.TheInternationalIntravitrealBeva-
cizumabSafetySurvey:usingtheinternettoassessdrugsafetyworldwide.
BrJOphthalmol2006;90(11):1344-9.
20.
DemolsP.Intravitrealinjectionsofcorticoids.BullSocBelgeOphthalmol
2007;(304):117-23.
21.
RheeDJ,PeckRE,BelmontJetal.Intraocularpressurealterationsfollowing
intravitrealtriamcinoloneacetonide.BrJOphthalmol2006;90(8):999-1003.
22.
BakriSJ,BeerPM.Theeffectofintravitrealtriamcinoloneacetonideon
intraocularpressure.OphthalmicSurgLasersImaging2003;34(5):386-90.
IO-NN1-0108.indd 33 19/03/08 11:15:12
 6
6
1
/
6
100%