Fusion et hémifusion induites par les protéines d`enveloppe sauvages

cas-image
Fusion et hémifusion induites
par les protéines d’enveloppe sauvages (WT)
et mutantes (W596M) du VIH
S. Bär
M. Alizon
Département de biologie cellulaire, Institut
Cochin, Inserm U567, CNRS UMR8104,
75014 Paris
Les glycoprotéines d’enveloppe gp120 et gp41 du virus de l’immunodéficience
humaine (VIH) permettent l’entrée du virus dans la cellule cible par fusion de
l’enveloppe virale et de la membrane cible. Des mutations dans la gp41 peuvent
entraîner une perte de fonctionnalité à différents niveaux de cette chaîne d’évé-
nements, permettant la pénétration de la capside virale dans la cellule. En effet,
celle-ci comprend une étape de mise en continuité des bicouches lipidiques virale
et cellulaire (hémifusion) puis des étapes d’ouverture et de dilatation du pore de
fusion qui, toutes, sont susceptibles d’être affectées [1].
Afin de mettre en évidence l’étape touchée, l’on peut suivre
la migration de marqueurs fluorescents lors de la fusion de
cellules effectrices exprimant les protéines d’enveloppe
virales et de cellules cibles. On considère que cette fusion
cellule-cellule mime correctement la fusion virus-cellule.
Sur la figure 1, des cellules effectrices marquées avec un
analogue de lipides émettant de la fluorescence dans le vert
(DiO, Molecular Probes) sont mises au contact de cellules
cibles marquées avec un analogue de lipides émettant de la
fluorescence dans le rouge (DiI, Molecular Probes). Ces
composés vont d’abord marquer la membrane plasmique
des cellules, puis, au cours du temps, le recyclage membra-
naire va entraîner un marquage des vésicules cytoplasmi-
ques. Ces vésicules émettant de la fluorescence peuvent
alors servir de marquage cytoplasmique. À l’issue de la
coculture, les cellules sont fixées et observées au micros-
cope confocal.
La capacité de telles mutations à permettre la mise en place
de l’hémifusion tout en bloquant la suite du processus de
fusion amène à penser que la gp41 est directement impli-
quée dans les étapes de formation et de dilatation du pore de
fusion [3].
Remerciements. Ce travail a été financé par une bourse de
l’Agence nationale de recherches sur le sida.
Références
1. Blumenthal R, Clague MJ, Durell SR, Epand RM. Membrane fusion.
Chem Rev 2003 ; 103 : 53-69.
2. Cao J, Bergeron L, Helseth E, Thali M, Repke H, Sodroski J. Effects of
amino acid changes in the extracellular domain of the human immunode-
ficiency virus type 1 gp41 envelope glycoprotein. JVirol1993 ; 67 :
2747-55.
3. Bar S, Alizon M. Role of the ectodomain of the gp41 transmembrane
envelope protein of human immunodeficiency virus type 1 in late steps of
the membrane fusion process. J Virol 2004 ; 78 : 811-20.
Virologie 2005, 9 : 326-7
Virologie, Vol. 9, n° 4, juillet-août 2005
326
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

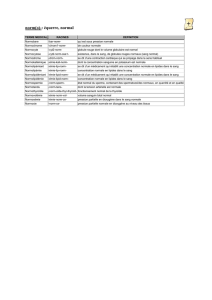
Neg A B CWT
WT
W596M
10µm
10µm
10µm
10µm
Figure 1. A) Témoin négatif (Neg) : les cellules effectrices n’expriment pas de protéines d’enveloppe. Les marqueurs ne migrent pas. B)
WT : les cellules effectrices expriment les protéines d’enveloppe sauvages. La fusion a lieu et suite à la mise en continuité des bicouches
lipidiques et à la formation puis à la dilatation du pore de fusion, lipides membranaires et vésicules cytoplasmiques peuvent diffuser. C)
W596M : les cellules effectrices expriment des protéines d’enveloppe mutées dans la gp41 en position 596 [2]. Seuls les marqueurs
membranaires peuvent diffuser. On atteint le stade d’hémifusion consistant en une diffusion de lipides membranaires. L’absence de
passage des vésicules cytoplasmiques marquées indique que le pore de fusion, s’il est formé, n’atteint pas une taille suffisante au mélange
des contenus cytoplasmiques.
cas-image
Virologie, Vol. 9, n° 4, juillet-août 2005
327
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.
1
/
2
100%