Erythroenzymopathies : modèle d`études - iPubli

SYNTHÈSE
Raonde Rosa
à
à
ATP A
2,3
à
L

1

1
/
( 1
7
vol.


of
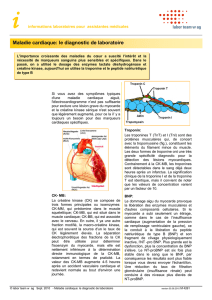
Rappos entre le système GSH et le des pentoses phos
phates.
 6
6
 7
7
 8
8
 9
9
 10
10
1
/
10
100%