Le syndrome inflammatoire de reconstitution immunitaire : plusieurs

Journal Identification = MET Article Identification = 0469 Date: March 9, 2015 Time: 8:40 am
Mise au point
mt 2015 ; 21 (1) : 8-18
Le syndrome inflammatoire
de reconstitution
immunitaire :
plusieurs visages
pour le même syndrome
Silvia Sovaila1, Claire Rivoisy2, Anne Bourgarit3,4,5
1Service de médecine interne, hôpital Saint-Louis, 75010 Paris, France
2Service de médecine interne, hôpital de Bicêtre, université Paris-Sud, 94270 Paris Le
Kremlin Bicêtre, France
3Service de médecine interne, diabète et pathologies métaboliques, hôpitaux universitaires
de Strasbourg, université de Strasbourg, 67091 Strasbourg France
4Inserm UMRS 945, Pitié-Salpêtrière, UPMC, 75651 Paris France
5Service de médecine interne, CHU Jean Verdier, APHP, université Paris 13, 93140 Bondy,
France
<anne.bourgaritdurand@jvr.aphp.fr>
Le syndrome inflammatoire de reconstitution immune (IRIS) est défini par l’aggravation sous
forme inflammatoire d’une pathologie infectieuse, lors de la reconstitution immunitaire après
une immunodépression «réversible ». Connu au cours des tuberculoses ganglionnaires, ce
syndrome a été clairement caractérisé et identifié plus récemment au cours de l’infection par
le VIH au cours de la puissante reconstitution immune induite par les trithérapies antivirales.
Depuis, les conditions de survenue de ce syndrome ne cessent de s’étendre et peuvent compli-
quer toutes les immunodépressions réversibles : greffe de moelle, transplantation d’organe,
chimiothérapie, biothérapies anti-inflammatoires, anticorps monoclonaux et grossesse. Par
ailleurs, initialement décrit au décours de pathologies infectieuses, il peut aussi compliquer
d’autres affections : auto-immunes, tumorales, etc. Son diagnostic est souvent un diagnostic
d’élimination. Son caractère très inflammatoire et aigu peut, parfois, engager le pronostic
fonctionnel et vital mais il est le plus souvent transitoire et de bon pronostic. Savoir recon-
naitre ce syndrome permet une prise en charge adaptée, anti-inflammatoires, modulation de la
reconstitution immunitaire, et surtout de ne pas remettre en question l’efficacité du traitement
anti-infectieux associé.
Mots clés : reconstitution immune, immunodépression réversible, syndrome de reconstitution
immunitaire
Le syndrome inflammatoire de
reconstitution immune (IRIS) est
défini par l’aggravation sous forme
inflammatoire d’une pathologie,
lors de la reconstitution immuni-
taire après une immunodépression
«réversible ». Connu au cours des
tuberculoses ganglionnaires, ce syn-
drome a été clairement caractérisé
et identifié plus récemment au cours
de l’infection par le VIH lors de
la puissante reconstitution immune
induite par les trithérapies antivirales.
Depuis, les conditions de surve-
nue de ce syndrome ne cessent
de s’étendre et peuvent compli-
quer toutes les immunodépressions
réversibles : greffe de moelle, trans-
plantation d’organe, chimiothérapie,
biothérapies anti-inflammatoires et
grossesse. Par ailleurs, initialement
décrit principalement sous la forme
d’aggravations de pathologies infec-
tieuses, il peut aussi compliquer
d’autres affections : auto-immunes,
tumorales, etc.
Nous présentons ici ses diffé-
rentes manifestations à l’occasion de
quatre cas cliniques illustratifs per-
mettant d’apprendre à le reconnaître
sous toutes ses formes.
Observation 1. Un patient de
32 ans, ivoirien, est hospitalisé pour
doi:10.1684/met.2015.0469
Tirés à part : A. Bourgarit
8
Pour citer cet article : Sovaila S, Rivoisy C, Bourgarit A. Le syndrome inflammatoire de reconstitution immunitaire : plusieurs visages pour le même syndrome.
mt 2015 ; 21 (1) : 8-18 doi:10.1684/met.2015.0469
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

Journal Identification = MET Article Identification = 0469 Date: March 9, 2015 Time: 8:40 am
asthénie, fièvre et toux. Un diagnostic de tuber-
culose disséminée avec atteinte pleuro-pulmo-
naire, ganglionnaire et hépatosplénique est retenu et
confirmé bactériologiquement : mise en évidence de
M. tuberculosis multisensible dans les crachats et le
liquide pleural. On lui découvre une infection par le VIH
(charge virale à 150 000 copies/mL), il est sévèrement
immunodéprimé (lymphocytes TCD4+ à 105/mm3). Trois
semaines de quadrithérapie antituberculeuse permettent
une amélioration clinique et radiologique avec un retour à
l’apyrexie, une stérilisation des crachats et une disparition
de l’épanchement pleural. Un traitement antirétroviral
efficace (HAART) par zidovudine, lamivudine et éfavirenz
est alors débuté. Soixante-douze heures après le début
de ce traitement, le patient signale la réapparition de
la fièvre avec syndrome pleural, réaugmentation du
syndrome inflammatoire biologique. La nouvelle enquête
microbiologique, incluant la recherche de BAAR dans
les crachats et le LBA reste négative éliminant une
autre infection ou la résistance au traitement. Il n’y a
pas d’argument pour un effet toxique des traitements.
Parallèlement, une réponse immunovirologique au trai-
tement antirétroviral est confirmée par la diminution de
la charge virale à 400 copies/mm3et l’augmentation
des lymphocytes T CD4+ à 178/mm2. Le diagnostic de
syndrome inflammatoire de reconstitution immunitaire
de la tuberculose associé aux antirétroviraux a ainsi été
retenu. L’adjonction d’une corticothérapie générale a
permis l’amélioration rapide des symptômes.
Historique
Les aggravations paradoxales de tuberculoses sous trai-
tement antituberculeux bien conduit sont décrites depuis
l’utilisation de la rifampicine en 1955 [1]. Toutefois, ce
syndrome a été clairement identifié, caractérisé et défini
depuis l’utilisation d’antiprotéases dans le traitement de
l’infection par le VIH en 1996. On le connaît depuis sous
le nom d’Immune Reconstitution Inflammatory Syndrome
(IRIS) [2].
L’IRIS ou SRI (syndrome de reconstitution immunitaire)
est donc la manifestation clinique d’une réponse immu-
nitaire disproportionnée inflammatoire dans un contexte
de reconstitution immune après une immunosuppression
réversible.
Épidémiologie
L’arrivée de la trithérapie antirétrovirale amène à la
publication d’un premier cas d’IRIS chez un patient traité
pour une rétinite à CMV en 1997 [3]. Un an plus tard, en
1998, les mycobactéries et le cryptocoque ont été imputés
comme pathogènes d’IRIS dans trois autres cas cliniques
[4-6]. En 2012, 20 ans plus tard, le mot clé «immune
reconstitution syndrome »réunit 1 151 publications dans
PubMed.
Les données épidémiologiques existent seulement
dans le cadre du contexte de l’infection par le VIH. Dans
une récente méta-analyse, Muller et al. estiment que l’IRIS
complique l’introduction d’une trithérapie antirétrovirale
dans 16 % de cas [7] variant3à63%selon la localisa-
tion, l’agent pathogène et les moyens diagnostiques mis
en œuvre [8-10].
En dehors de l’infection par le VIH, les incidences sont
mal connues et reposent sur des séries rétrospectives [11] :
10 à 30 % dans les tuberculoses simples, 7 % sous anti-
TNF [12].
Physiopathologie
La physiopathologie de l’IRIS n’a elle aussi été étudiée
que dans le contexte de la restauration immunitaire
sous HAART des patients infectés par le VIH. Il a été
démontré que l’IRIS était associé à la restauration d’une
réponse immune très inflammatoire dirigée contre l’agent
pathogène-infectieux présent [13, 14] (tableau 1). Cette
réponse spécifique implique, selon le type d’agent patho-
gène, des lymphocytes T CD4 ou CD8 et/ou d’autres
acteurs de la réponse immune (Cf. tableau 2) [15]. Cette
réponse intense est associée à un «syndrome inflamma-
toire »ou «orage cytokinique »[16-19]. Elle implique
aussi la réponse immune innée : cellules NK, lympho-
cytes T ␥␦, complément [20], macrophages [21, 22]
probablement par des dysfonctions de la présentation
antigénique, et du contrôle de la réponse spécifique.
Ces dysfonctions semblent être le lit d’une susceptibilité
génétique.
Ces éléments de physiopathologie ne permettent pas
à ce jour d’avoir un test diagnostic positif d’IRIS mais la
réapparition d’une IDR phlycténulaire, d’un granulome
histologique et d’un test Quantiféron positif au cours d’une
tuberculose traitée, et contemporaine d’une reconstitution
quantitative, seront des arguments.
Formes et présentations cliniques
Les premiers critères diagnostiques d’IRIS ont été éta-
blis par Martyn French en 2004 (tableau 3) puis confirmés
par un consortium international (ISNIH).
On décrit deux formes d’IRIS sous HAART selon leur
chronologie :
–l’IRIS paradoxal correspond à la ré-détérioration
clinique lors de la restauration immunitaire d’une patho-
logie déjà connue et traitée, paradoxale car survenant
malgré un traitement efficace de l’infection illustré par le
l’observation no1 [23, 24] ;
mt, vol. 21, n◦1, janvier-février 2015 9
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

Journal Identification = MET Article Identification = 0469 Date: March 9, 2015 Time: 8:40 am
Mise au point
Tableau 1. Agents infectieux impliqués dans l’IRIS.
Agent pathogène Manifestations cliniques
IRIS
Délai d’apparition
IRIS
Mécanismes
impliqués dans l’IRIS
Bactéries
Mycobacterium
tuberculosis, M. BCG,
M. Avium complex,
M. Leprae
Fièvre, adénopathies,
pneumonie, pleurésie,
tuberculomes, méningites
[36, 37]
[3j, 4-12 sem.] [38]
selon type
immunodépression
CD4, macrophages,
NK, LT ␥␦, cytokines
Th1 et inflammatoires,
réaction
granulomateuse
Bartonella henselae Granulomatose splénique Réaction
granulomateuse
Chlamydia trachomatis Syndrome fébrile, urétrites,
arthrites [39]
6 mois (1 cas)
Tropheryma whipplei Syndrome fébrile, arthrites,
pleurésie, érythème
noueuse, syndrome
hypothalamique et
perforation digestive [40]
Granulomatose
digestive
Champignons
Cryptococcus
neoformans
Adénopathies, méningite
aseptique, maladie
disséminée,
pneumopathie, décès [41]
Cellules NK inactives,
macrophages inactifs
par défaut de TNF-␣,
CD4 Th1 helper
Histoplasma
capsulatum
Abcès hépatique,
lymphangite, uvéite et
arthrites [42]
Th1
Parasites
Pneumocystis Carini Pneumopathie interstitielle
atypique [43]
Modèle souris
Leishmania Donovani Uvéites/lésions cutanées
[44]
[2 sem.-8 mois] Anomalies de réponse
Th1 helper, aug
cytokines Th2 et
TNF-alpha
Schistosoma mansoni Hépatosplénomégalie,
douleurs abdominales [45]
[2 sem.-1 mois]
Criptosporidia Syndrome fébrile, douleurs
abdominales [45]
1 mois (n=1)
Strongyloides
stercorales
Troubles digestifs,
syndrome fébrile,
hyper-éosinophilie,
cytolyse, sepsis à BGN
associé [45]
[3 sem.-4 mois]
Toxoplasma gondii Céphalées, convulsion
[45, 46]
3 sem. (n=4)
Cysticercis Neurocysticercose [47]
10 mt, vol. 21, n◦1, janvier-février 2015
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

Journal Identification = MET Article Identification = 0469 Date: March 9, 2015 Time: 8:40 am
Tableau 1. (Suite)
Agent pathogène Manifestations cliniques
IRIS
Délai d’apparition
IRIS
Mécanismes
impliqués dans l’IRIS
Virus
CMV Rétinites/uvéites [48] CD8, NK
HVB Hépatite aiguë, flairs CD4 cytotoxique
HVC Hépatite aiguë, flairs CD4 cytotoxique
HHV8 Aggravation de sarcome
de Kaposi
VZV Lésions cutanées [49],
méningo-encéphalites [50]
[1 sem.-6 mois] IL-6, TNF-alpha
HSV Ulcérations,
méningo-encéphalites
4 mois
JC virus Aggravation de LEMP [51] Moy. 6 [1-14] sem. CD8 et CD4 anti-JC
virus
M. contagiosum virus Aggravation des lésions
cutanées [52]
Tableau 2. IRIS non infectieux.
Mécanisme Exemple
Tumoral Sarcome de Kaposi (HHV8) [45, 46]
Granulomateux Sarcoïdose [47-49]
Inflammatoire
Syndrome de Still [50]
Syndrome de Sweet [51]
Goutte [52]
Auto-immun
LES [53]
Thyroïdite Hashimoto [54, 55]
Thyroïdite de Grave-Basedow [56, 57]
Purpura trombocytopénique [58, 59]
Syndrome Guillain Barre [59, 60]
Leuco-encéphalopathie [61]
Résistance à l’insuline type B [62]
Hépatite auto-immune [63]
Syndrome néphrotique [64]
Autres Choc cardiogénique [65]
Thrombose cérébrale [66]
–l’IRIS démasquant illustré par le cas de Mme A.
(observation 2).
Observation 2. Mme A., 34 ans, dont l’infection
par le VIH est connue depuis sa grossesse huit années
auparavant, jusque-là non traitée, atteint les critères
d’introduction d’un traitement antirétroviral avec une
charge virale à 1 000 000 copies/mL et un taux de lym-
phocytes T CD4 à 270/mm3(<350/mm3). Huit jours après
le début d’une trithérapie efficace (éfavirenz, tenofovir et
emtricitabine), elle est hospitalisée pour toux et dyspnée
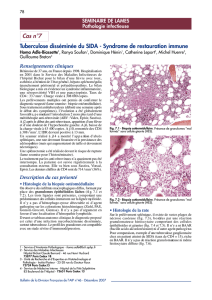
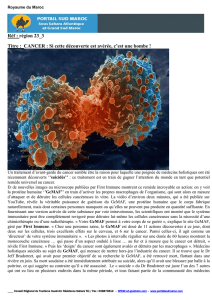
fébrile. Les examens cliniques et paracliniques mettent
en évidence une pneumopathie interstitielle bilatérale (cf.
figure 1). Le lavage broncho-alvéolaire est lymphocytaire,
stérile et ne montre pas, à l’examen direct, de Pneu-
mocystis jiroveci, de mycobactéries, de champignons ni
d’inclusions virales. À ce moment le taux de lympho-
cytes TCD4+ est à 510/mm3et la charge virale diminuée à
5 322 copies/mL, témoignant d’une réponse immunoviro-
logique excellente aux antirétroviraux. Devant la détresse
respiratoire, la patiente est prise en charge en réanima-
tion où l’introduction probabiliste de cotrimoxazole et
corticoïdes (1 mg/kg/j), et l’interruption du traitement anti-
rétroviral dans l’hypothèse d’un IRIS démasquant une
pneumopathie à P. jiroveci permettent une amélioration
rapide. Ce diagnostic est secondairement confirmé par la
positivité de la PCR pour P. jirovenci et la mise en évidence
de quelques kystes parasitaires dans le LBA après relecture
attentive des lames de l’examen direct [25].
La révélation lors de la restauration immunitaire d’un
tableau clinique jusqu’alors complètement inapparent
définit «l’IRIS démasquant »[26, 27]. Les manifestations
cliniques sont le plus souvent atypiques car très inflam-
matoires et exacerbées. Dans le cas de la tuberculose,
on différencie en plus «la tuberculose survenant sous
HAART »de «l’IRIS démasquant »celui-ci définit par
l’apparition de symptômes inflammatoires intenses dans
les trois premiers mois après le début des antirétroviraux
dans le cas de ce dernier [26-28]. L’existence d’un syn-
drome inflammatoire (CRP) lors de l’introduction des ARV
serait un facteur de risque d’IRIS démasquant [29].
La complexité de ces formes réside dans la caractéri-
sation et le diagnostic de l’infection ou de la pathologie
sous-jacente dont la symptomatologie peut être trompeuse
mt, vol. 21, n◦1, janvier-février 2015 11
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

Journal Identification = MET Article Identification = 0469 Date: March 9, 2015 Time: 8:40 am
Mise au point
Tableau 3. Critères diagnostiques d’IRIS (French, M.A., P. Price, and S.F. Stone, Immune restoration disease after antiretroviral
therapy. AIDS, 2004. 18(12): p. 1615-27). (D’après [2]).
Critères majeurs
A. Présentation atypique d’infections opportunistes ou néoplasies, chez les patients répondeurs au traitement antirétroviral
- Maladie localisée, ex. lymphatique, splénique, hépatique
- Réaction inflammatoire exagérée, ex. syndrome fébrile sévère, après exclusion d’autres étiologies, lésions douloureuses
- Réponse inflammatoire atypique dans le tissu atteint, ex. granulome, suppuration, nécrose, infiltrat inflammatoire lymphocytaire
périvasculaire
- Aggravation ou augmentation de la taille des lésions après évolution initiale clairement favorable sous traitement spécifique contre
le pathogène, avant de débuter le traitement antirétroviral, après avoir éliminé une toxicité médicamenteuse ou autre diagnostic, ex. :
•apparition ou augmentation des lésions cérébrales après le traitement pour cryptococcose ou toxoplasmose cérébrale ;
•progression de la pneumonie ou apparition d’une pneumonie après traitement d’une tuberculose ou pneumocystose pulmonaire ;
•nouvelle apparition ou aggravation d’une uvéite/rétinite après résolution d’une rétinite CMV ;
•fièvre et cytopénie après traitement pour une infection disséminée a mycobactéries atypiques ;
•augmentation des lésions de sarcome de Kaposi et rémissions dans un deuxième temps, complète ou partielle, sans traitement
spécifique ;
B. Diminution de niveaux de RNA HIV de 1 log10 copies/mL
Critères mineurs
A. Augmentation de taux de lymphocyte CD4 après début du traitement antirétroviral
B. Augmentation de la réponse antigène spécifique, ex. :
- réponse aux antigènes mycobactériens
C. Résolution spontanée de la maladie sans traitement spécifique antimicrobien ou de chimiothérapie, après poursuite du traitement
antirétroviral
Figure 1. TDM thoracique. Nodules centro-lobulaires ramifiés et opacités en verre dépoli avec images réticulées lobulaires.
12 mt, vol. 21, n◦1, janvier-février 2015
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
1
/
11
100%