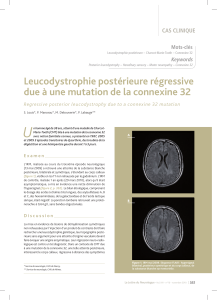
immunoglobulines iv - OMEDIT Poitou

Observatoire du Médicament des Dispositifs médicaux stériles et de l’Innovation Thérapeutique
Juin 2013
Version 01
FICHE PRATIQUE D’UTILISATION DES MEDICAMENTS
A L’INTENTION DES MEDECINS, PHARMACIENS et IDE
IMMUNOGLOBULINES INTRAVEINEUSES
CLASSE MEDICAMENTEUSE
Médicaments dérivés du sang
Immunoglobulines humaines polyvalentes intraveineuses
INDICATIONS
Déficits immunitaires primitifs
Traitements immunomodulateurs
Allogreffe de moelle osseuse
POSOLOGIE
Indication
Dose
Fréquence des injections
Traitement substitutif dans les déficits
immunitaires primitifs
Dose de charge : 0,4 à
0,8 g/kg
Dose d'entretien : 0,2
à 0,8 g/kg
Toutes les 2 à 4 semaines pour obtenir un
taux résiduel d'IgG d'au moins 4 à 6 g/l
Traitement substitutif dans les déficits
immunitaires secondaires
0,2 à 0,4 g/kg
Toutes les 3 à 4 semaines pour obtenir un
taux résiduel d'IgG d'au moins 4 à 6 g/l
Enfants infectés par le VIH
0,2 à 0,4 g/kg
Toutes les 3 à 4 semaines
Traitement immunomodulateur :
Purpura thrombopénique idiopathique
0,8 à 1 g/kg
A J1, éventuellement répété dans les 3 jours
0,4 g/kg/j
Pendant 2 à 5 jours
Syndrome de Guillain-Barré
0,4 g/kg/j
Pendant 3-7 jours
Maladie de Kawasaki
1,6 à 2 g/kg
En plusieurs doses réparties sur 2 à 5 jours en
association avec l'acide acétylsalicylique ou
en une dose unique en association avec
l'acide acétylsalicylique
Allogreffe de moelle osseuse :
Traitement des infections et prévention de la
maladie du greffon contre l'hôte
0,5 g/kg
Chaque semaine à partir du jour J-7 avant la
greffe jusqu'à 3 mois après la greffe
Défaut persistant de production d'anticorps
0,5 g/kg
Chaque mois jusqu'au retour à la normale du
taux d'anticorps

Observatoire du Médicament des Dispositifs médicaux stériles et de l’Innovation Thérapeutique
Juin 2013
Version 01
FICHE PRATIQUE D’UTILISATION DES MEDICAMENTS
A L’INTENTION DES MEDECINS, PHARMACIENS et IDE
IMMUNOGLOBULINES INTRAVEINEUSES
MODALITES D’ADMINISTRATION
Respecter les règles d’asepsie habituelle lors de la reconstitution
Après reconstitution (TEGELINE), agiter modérément par un mouvement de rotation doux, pour
éviter la formation de mousse, jusqu'à dissolution complète de la poudre en moins de 30 minutes
Les spécialités (CLAIRYG, PRIVIGEN, OCTAGAM) sont prêtes à l’emploi
Administrer les Immunoglobulines à l'aide d'une tubulure séparée, ne pas administrer avec d'autres
produits et/ou médicaments
Perfuser lentement pendant la première ½ heure (0,5-1 ml/kg/h) puis augmentation progressive du débit
La vitesse de perfusion doit être rigoureusement contrôlée et adaptée en fonction de la tolérance clinique :
Début de
perfusion
Si bonne tolérance
1ère ½ heure
ensuite
Ne pas dépasser
IMMUNOGLOBULINES
0,5 à 1 ml /kg /h
progressive jusqu’à 2 à 3 ml/kg/h
4 ml/kg/h
Surveillance des patients pendant la perfusion et pendant au moins 20 minutes après la perfusion, une heure
en cas de première perfusion d’IgIV.
HAD :
o Le patient doit bénéficier d’un abord veineux facile,
o La présence à domicile d’une tierce personne adulte et éduquée à l’arrêt de la perfusion est
obligatoire pendant toute la durée des perfusions,
o Avoir une ligne téléphonique fonctionnelle et pouvoir communiquer à distance,
o Les perfusions sont réalisées uniquement les jours de la semaine,
o Le patient est informé par l’infirmière des différents incidents possibles comme l’inflammation au
point de ponction, la diffusion de la perfusion, les effets secondaires éventuels et doit savoir
arrêter la pompe au moindre doute et/ou alerter,
o L’IDE s’assure que le patient dispose du numéro de téléphone de l’HAD.
SURVEILLANCE - PRECAUTIONS D’EMPLOI
Surveiller le patient pendant toute la durée la perfusion. Noter les paramètres de surveillance sur la fiche
de suivi (ANNEXE)
Chez les patients à risque (insuffisance rénale préexistante, diabète, âge supérieur 65 ans, obésité,
hypovolémie, sous médicaments néphrotoxiques), l’administration d’IgIV impose :
o une hydratation correcte avant administration IV,
o une surveillance de la diurèse,
o une surveillance de la créatinémie
o d’éviter si possible, l’association à des médicaments néphrotoxiques (ex : diurétiques de l’anse,
AINS, antibiotiques néphrotoxiques…..)
o habituellement, administrer 1 ml/Kg/h ; ne pas dépasser 2 ml/kg/h

Observatoire du Médicament des Dispositifs médicaux stériles et de l’Innovation Thérapeutique
Juin 2013
Version 01
FICHE PRATIQUE D’UTILISATION DES MEDICAMENTS
A L’INTENTION DES MEDECINS, PHARMACIENS et IDE
IMMUNOGLOBULINES INTRAVEINEUSES
En cas d’insuffisance rénale préexistante, une IgIV sans saccharose (CLAIRYG, PRIVIGEN, OCTAGAM) doit
être privilégiée
A la fin de l’administration et/ou en cas de non administration, partielle ou complète, retourner les unités
à la pharmacie avec le volet de traçabilité
Certains effets indésirables graves peuvent être liés au débit de perfusion. Respecter les débits de
perfusion recommandés
PRINCIPAUX EFFETS INDESIRABLES
Fièvre
Frisson
Augmentation réversible de la créatinine sérique
Certains effets indésirables peuvent survenir plus fréquemment :
o en cas de débit de perfusion élevé
o chez les patients présentant une hypo ou agammaglobulinémie avec ou sans déficit en IgA et lors
de la première administration d’Ig ou si le traitement a été interrompu depuis longtemps
STATUT
Médicament soumis à prescription hospitalière.
Inscrit sur la liste de rétrocession avec prise en charge à 100%
Inscrit sur la liste des spécialités prises en charge en sus des GHS
Il s’agit de médicaments dérivés du plasma (MDS) dont :
- la traçabilité patient-lot est obligatoire
- la déclaration de tous les effets indésirables doit être faite au Centre Régional de Pharmacovigilance dans les 24h.
1
/
3
100%