Dosages de thyroxine - John Libbey Eurotext

Dosages de thyroxine (T4) et tri-iodothyronine
(T3) : techniques
et place dans le bilan thyroïdien fonctionnel
R. Sapin
1
J.-L. Schlienger
2
1
Unité d’analyses endocriniennes,
Laboratoire universitaire de biophysique,
CNRS/ULP UMR 7004,
Faculté de médecine, Strasbourg
2
Service de médecine interne et nutrition,
Hôpital de Hautepierre, Strasbourg
Article reçu le 9 novembre 2002,
accepté le 18 décembre 2002
Résumé. La production hormonale de la glande thyroïde est composée pour
80 % par la thyroxine (T4) et pour 20 % par la tri-iodothyronine (T3). Dans le
sérum l’origine de la T4 est uniquement thyroïdienne alors que 80 % de la T3
provient d’une désiodation de la T4 en périphérie. Cette désiodation subissant
des influences diverses, la T3 est un moins bon reflet que la T4 du fonctionne-
ment de la thyroïde. Dans le sérum seulement 0,02 % de la T4 et 0,3 % de la T3
existe sous forme libre, le reste est lié aux protéines de transport. Le dosage de la
fraction libre de T4 (T4L) et de T3 (T3L) a supplanté celui des hormones totales
(libres + liées) en raison d’une meilleure sensibilité et spécificité diagnostiques.
Le dosage des hormones totales a une place limitée en recherche ou en cas
d’hyperthyroïdie très sévère. Pour le dosage des hormones libres, la dialyse/RIA
est la technique de référence actuelle. En routine sont utilisés des immunodosa-
ges automatisés directs en deux étapes ou une étape avec anticorps marqué ou
ligand macromoléculaire. Le dosage des fractions libres reste délicat, en parti-
culier dans le sérum des patients hospitalisés atteints de maladies graves non
thyroïdiennes dont la capacité de fixation de la thyroxine est abaissée. Les
interférences des anticorps anti-hormones thyroïdiennes et de la dysalbuminé-
mie familiale dépendent de la méthode de dosage. Elles sont devenues moins
marquées et se détectent rarement. La bonne maîtrise de l’interprétation des
résultats d’un dosage nécessite sa mise à l’épreuve sur un panel de sérums bien
caractérisés biologiquement et cliniquement. Le dosage de T4L (et de T3L si la
T4L est normale et une hyperthyroïdie suspectée) permet de confirmer et graduer
une dysthyroïdie (franche ou infraclinique). Dans toutes les situations où le
statut thyroïdien n’est pas en équilibre (début ou ajustement du traitement d’une
dysthyroïdie, évolution d’une thyroïdite subaiguë), et où l’intégrité de l’axe
hypothalamo-hypophysaire n’est pas respectée (hypothyroïdie secondaire ou
tertiaire), le dosage de TSH est défaillant et seuls les dosages de T4L ou T3L
permettent d’évaluer la fonction thyroïdienne.
Mots clés : thyroxine, tri-iodothyronine, technique de dosage, fonction
thyroïdienne, stratégie diagnostique
Summary. Hormonal production of the thyroid gland is constituted of thy-
roxine or T4 (80%) and triiodothyronine or T3 (20%). In the circulation, whole
T4 originates from thyroid secretion but most of T3 (80%) is produced extrathy-
roidally from T4 deiodination. Conversion of T4 to T3 may be influenced by
various conditions and circulating T3 is a less reliable reflection of thyroid
hormone production than T4. In serum most of T4 and T3 is bound to binding
proteins and only 0.02% of T4 and 0.3% of T3 is free. Because of their higher
diagnostic performance, free T4 (FT4) and free T3 (FT3) measurements have
superseded total (free + bound) hormone determination. Total hormone measu-
rements remain useful for research studies or in case of severe hyperthyroidism.
Equilibrium dialysis/RIA is considered as the reference method for free hor-
mone measurements. Routine clinical laboratories use automated direct two-
revue générale abc
Ann Biol Clin 2003, 61 : 411-20
Ann Biol Clin, vol. 61, n° 4, juillet-août 2003 411
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

step or one-step immunoassays with a high molecular weight ligand or labelled
antibody. Free hormone measurement remains technically demanding, espe-
cially in sera from severe non-thyroid ill patients with low serum thyroxine
binding capacity. Interference from anti-thyroid hormone antibodies and fami-
lial dysalbuminemic hyperthyroxinemia depends on the assay method, but is
now less marked and less frequently detected. To be able to correctly interpret the
results of an assay, it is necessary to assess its performance in biologically and
clinically well-characterised serum samples. FT4, and FT3 measurements, if
FT4 is normal and hyperthyroidism suspected, are used to confirm and assess the
level of hypo and hyperthyroidism (overt or subclinical). When the thyroidal
status is unstable (first months of a thyroid treatment, altered L-T4 dose,
subacute thyroiditis) or when the hypothalamic-pituitary function is disturbed
(central hypothyroidism), TSH determination is diagnostically misleading and
only free hormone measurements are reliable for thyroid function assessment.
Key words: thyroxine, triiodothyronine, assay method, thyroid function,
diagnostic strategy
Les indéniables progrès techniques du dosage de la TSH,
stimuline hypophysaire de la glande thyroïde, ont propulsé
ce dosage au premier rang des tests pratiqués pour diagnos-
tiquer un dysfonctionnement thyroïdien ou suivre l’effica-
cité d’un traitement à visée thyroïdienne. Si ce dosage est
ordinairement suffisant pour l’affirmation de l’euthyroïdie,
celui des hormones thyroïdiennes, 3,3’,5,5’ tétra-
iodothyronine ou thyroxine (T4) et 3,3’,5 tri-iodothyronine
(T3), conserve cependant une place importante dans le
bilan thyroïdien fonctionnel.
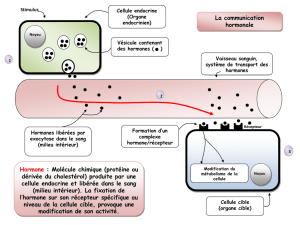
La T4 est produite en totalité par la glande thyroïde. Elle
constitue environ 80 % de la production hormonale thyroï-
dienne, le reste étant constitué par la T3. La demi-vie
plasmatique de la T4 est de 7 jours. En périphérie (foie,
rein, cœur, muscle, cerveau) elle est en partie convertie en
T3. La T4 et la T3 exercent aux niveaux hypophysaire et
hypothalamique un rétrocontrôle négatif sur leur propre
sécrétion. La demi-vie plasmatique de la T3 est de l’ordre
de 24 heures. Une partie (20 %) seulement de la T3 circu-
lante provient directement de la glande thyroïde, l’autre
(80 %) résulte de la dégradation en périphérie de la T4 sous
l’effet de désiodases. L’activité de ces enzymes subit diver-
ses influences (jeûne, pathologies, médicaments) qui peu-
vent moduler la concentration de T3. Pour cela, bien qu’elle
soit l’hormone thyroïdienne biologiquement active qui se
fixe aux récepteurs nucléaires, la T3 plasmatique est sou-
vent un reflet de la fonction thyroïdienne moins fidèle que la
T4 [1].
Transport plasmatique –
hormones totales - hormones libres
La T4 et la T3 circulent dans le sang sous deux formes en
équilibre : l’une libre et l’autre liée à des protéines de
transport. Chez un sujet euthyroïdien, seulement 0,02 % de
la T4 est libre, le reste est lié : 75-80 % à la thyroxine
binding globulin (TBG), 15-20 % à la préalbumine ou
transthyrétine (TTR) et 5-10 % à l’albumine. De même
seulement 0,3 % de la T3 est libre, le reste est lié : 75-80 %
à la TBG, moins de 10 % à la TTR et environ 10 % à
l’albumine [1].
Il est généralement admis que seule l’hormone libre tra-
verse la membrane capillaire et que le transport des hormo-
nes aux cellules cibles est proportionnel à la concentration
d’hormone libre. L’hypothèse selon laquelle la concentra-
tion d’hormone libre déterminée in vitro est un indicateur
fiable des effets de l’hormone in vivo ne constitue cepen-
dant au mieux qu’une approximation [2, 3]. C’est pourquoi
la normalité de la concentration en hormone libre chez un
sujet euthyroïdien, dans n’importe quelles circonstances,
en particulier quand les concentrations des protéines de
transport sont gravement perturbées, ne peut pas constituer
un critère de validité d’une méthode.
Il apparaît cependant clairement que ce sont les concentra-
tions de T4 libre (T4L) et de T3 libre (T3L) et non pas de T4
totale (libre + liée) (T4T) ou T3 totale (T3T), qui partici-
pent à la régulation de la sécrétion de TSH et qui, lorsqu’el-
les sont anormales, induisent des signes cliniques d’hypo-
ou d’hyperthyroïdie. En raison de ses meilleures sensibilité
et spécificité diagnostiques, le dosage de la fraction libre
Tirés à part : R. Sapin
revue générale
Ann Biol Clin, vol. 61, n° 4, juillet-août 2003412
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

des hormones thyroïdiennes a supplanté celui des hormo-
nes totales [4]. Le dosage des hormones totales conserve un
intérêt dans des situations particulières et comme outil de
recherche.
Dosages des hormones totales
La T4T et la T3T sont en général dosées dans le sérum à
l’aide d’immunodosages compétitifs utilisant des mar-
queurs isotopiques, enzymatiques ou luminescents et des
anticorps polyclonaux ou monoclonaux. Le 8-anilino-
naphtalène sulfonique acide (ANS) ou les salicylates sont
utilisés pour dissocier les hormones thyroïdiennes des pro-
téines de liaison. Un biais négatif, suite à une dissociation
incomplète, peut apparaître quand la concentration protéi-
que est élevée. Une meilleure standardisation à partir d’une
préparation unique apparaît encore souhaitable [4]. Les
anticorps anti-T4 ou anti-T3 peuvent fausser le résultat
respectivement de T4T ouT3T, vers le haut ou vers le bas en
fonction de la spécificité de la méthode de séparation em-
ployée dans le dosage. Cette interférence est exception-
nelle.
Les valeurs usuelles varient légèrement selon la technique
utilisée. À titre d’exemple, elles peuvent être pour la
T4T comprises entre 65 et 155 nmol/L (1 µg/L =
1,287 nmol/L) et pour la T3T entre 1,2 à 3,1 nmol/L
(1 µg/L = 1,536 nmol/L). Des valeurs plus élevées ont été
notées pour la T4T et T3T pendant la première année de vie
et pour la T3T et parfois la T4T pendant l’enfance et
l’adolescence [5, 6]. L’hormonémie totale présente l’incon-
vénient de dépendre de la concentration en protéines vec-
trices et de la liaison des hormones à ces protéines.
Le dosage des hormones totales reste précieux pour suivre
l’efficacité du traitement d’une hyperthyroïdie très sévère.
En effet, dans cette situation, pendant plusieurs semaines la
TSH peut rester abaissée et la concentration de T4L et T3L
supérieure à celle du dernier point de la gamme étalon. La
dilution du sérum ne permet pas d’obtenir la concentration
réelle en hormones libres. Seule la quantification des hor-
mones totales, que l’on peut obtenir par dilution, permet de
suivre la baisse de la concentration des hormones thyroï-
diennes et l’efficacité du traitement jusqu’à ce que l’hormo-
némie libre devienne mesurable. En recherche, le calcul du
rapport T4T sur T4L dosée par la méthode de dialyse
permet d’apprécier indirectement la capacité de fixation
des protéines de transport du sérum [7].
Dosages des hormones libres
Étape préanalytique
La T4L et la T3L sont en général dosées dans le sérum. Le
résultat n’est pas influencé par une hémolyse modérée. La
nature de l’anticoagulant utilisé pour l’obtention d’un
plasma doit être préalablement validée pour chaque mé-
thode de dosage. Le sérum est stable 8 jours à 4 °C et doit
être congelé à – 20 °C au-delà [8]. Cependant chez les
patients traités à l’héparine le sérum ne sera pas conservé
plus de 24 heuresà4°C[9].
Valeurs usuelles - Variations physiologiques
Les résultats de T4L et plus encore ceux de T3L dépendent
de la technique de dosage. La T4L est augmentée à la
naissance, dans les premiers mois de la vie et plus modéré-
ment dans l’enfance [5, 6]. Elle reste dans l’intervalle de
référence chez les personnes âgées et s’abaisse chez la
femme enceinte au deuxième et troisième trimestre de la
grossesse [10]. La T3 élevée à la naissance, décroît progres-
sivement jusqu’à l’âge de 20 ans, se stabilise et peut dimi-
nuer encore au-delà de 60 ans. Elle s’abaisse au deuxième
et troisième trimestre de la grossesse. Pour la T4L et laT3L,
il est impératif d’établir les valeurs usuelles au laboratoire
ou pour le moins de les valider localement (tableau I).
Techniques de dosage [13]
La très faible concentration de la fraction libre des hormo-
nes thyroïdiennes (0,02 % pour la T4, 0,3 % pour la T3) en
équilibre avec une concentration totale beaucoup plus éle-
vée rend difficile la mesure directe de la concentration des
hormones libres. Jusqu’à la fin des années 1970, seul un
index indirect calculé à partir de la T4T et d’un test évaluant
la capacité de fixation des protéines du sérum a permis cette
détermination. La mesure directe des concentrations de
T4L et T3L reste délicate et la prudence incite à considérer
le résultat de ces dosages comme une estimation de la
concentration en hormone libre [3]. La difficulté majeure
provient du fait que la méthode utilisée doit perturber le
moins possible l’équilibre libre-lié. Toutes les méthodes, à
l’exception de l’ultrafiltration, imposent une dilution du
sérum et plus généralement la séquestration d’une certaine
Tableau I. Valeurs usuelles de la T4L et T3L dosées par la
méthode Elecsys [11, 12]
T4 libre
Enfants de 1 jour à 1 an 14 – 26 pmol/L
Enfants à partir de 1 an et adultes 12 – 23 pmol/L
Grossesse deuxième trimestre 10 – 19 pmol/L
Grossesse troisième trimestre 9 – 17 pmol/L
T3 libre
De 1 jour à 1 an 4,5 – 10,5 pmol/L
1 an à 20 ans 5,4 – 9,1 pmol/L
20 ans à 60 ans 3,8 – 7,1 pmol/L
Au-delà de 60 ans 2,8 – 6,5 pmol/L
Grossesse troisième trimestre 3,4 – 6,5 pmol/L
Dosage des hormones thyroïdiennes
Ann Biol Clin, vol. 61, n° 4, juillet-août 2003 413
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

quantité d’hormone, dans le dialysat pour la dialyse à
l’équilibre, sur un adsorbant ou un anticorps pour les autres
méthodes. Il faut veiller à ce que la déplétion de l’hormone
liée soit limitée à 2-5 %, afin que la perturbation de l’équi-
libre initial soit négligeable [2, 3, 13, 14]. On distingue les
méthodes absolues avec calibrateurs en milieu tampon éta-
lonnés par gravimétrie et les méthodes relatives ou compa-
ratives avec calibrateurs sériques dont la concentration en
hormone libre est déterminée à l’aide d’une méthode abso-
lue. Les principales caractéristiques de ces méthodes sont
résumées dans le tableau II.
Méthodes absolues - Méthodes de référence
Ces méthodes nécessitent la séparation physique de l’hor-
mone libre par dialyse à l’équilibre ou ultrafiltration. Dans
le dialysat ou l’ultrafiltrat, la T4 ou la T3 est dosée directe-
ment par une méthode radio-immunologique (RIA) très
sensible [15, 16]. À l’heure actuelle, seul un dosage de T4L
par dialyse/RIA est commercialisé. On reproche à ces mé-
thodes absolues une reproductibilité peu performante et
surtout une lourdeur technique incompatible avec les ana-
lyses de routine.
Méthodes relatives - Immunodosages de routine
Les méthodes relatives ont en commun une réaction directe
du sérum avec un anticorps monoclonal ou polyclonal
anti-hormone. Cet anticorps séquestre une fraction de
l’hormone. Ces techniques de dosage mettent en jeu un
ligand qui entre en compétition avec l’hormone pour la
fixation sur les sites anticorps. Un marqueur radioactif
(RIA), enzymatique (EIA) ou luminescent (LIA) est fixé
sur le ligand ou l’anticorps. Ces techniques utilisées par les
laboratoires d’analyses médicales sont facilement automa-
tisables. Elles se différencient par la façon de quantifier
l’occupation des sites anticorps.
Dosages en deux étapes
Ces techniques sont connues également sous le nom de
méthode par immuno-extraction ou titrage en retour. Dans
Tableau II. Caractéristiques des principales méthodes de dosage des hormones thyroïdiennes libres
Méthode Qualités Défauts Interférences
Dialyse/RIA Méthode absolue Technique lourde peu applicable en
routine
Pas d’interférence de FDH
1
(T4L) et
AAHT
2
Dilution
Séparation longue (18 h)
Effet in vitro de l’héparine très
marqué (T4L)
Ultrafiltration/RIA Méthode absolue
Absence de dilution
Séparation rapide (1-2 h)
Technique très délicate non
commercialisée
Pas d’interférence de FDH (T4L) et
AAHT
Effet in vitro de l’héparine moins
marqué
Immunodosage en deux étapes Pas de contact direct entre le ligand
et le sérum
Automatisable
Méthode relative
Dilution - Séquestration
En méthode manuelle : reproductibilité
médiocre, dérive
Dynamique de réponse limitée
Faible ou nulle de la FDH (T4L)
Pas d’interférence des AAHT
Immunodosage en une étape
avec ligand marqué,
traceur analogue radioactif
Praticabilité
Reproductibilité
Dynamique de réponse suffisante
Méthode relative
Dilution - Séquestration
Influence de la concentration en
protéines de transport (albumine)
Très marquée et systématique de la
FDH (T4L) et des AAHT
Baisse paradoxale de T4L sous
héparine
Immunodosage en une étape avec
ligand macromoléculaire marqué
Praticabilité (automatisable)
Reproductibilité
Dynamique de réponse suffisante
Méthode relative
Dilution - Séquestration
Moindre effet des protéines de
transport
Possible des AAHT
Pas d’interférence de la FDH (T4L)
avec certaines trousses
Immunodosage en une étape
avec anticorps marqué
Praticabilité (automatisable)
Reproductibilité
Dynamique de réponse suffisante
Pas de réactivité du ligand avec les
protéines de transport
Méthode relative
Dilution - Séquestration
Faible de la FDH (T4L)
Possible des anti-T4 pour T4L
homologue
Possible des anti-T3 pour T4L
hétérologue et T3L homologue
Anticorps anti-phase solide
1
FDH : dysalbuminémie familiale ;
2
AAHT : anticorps anti-hormone thyroïdienne.
revue générale
Ann Biol Clin, vol. 61, n° 4, juillet-août 2003414
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.

la première étape, une fraction de l’hormone est extraite par
des anticorps anti-hormone immobilisés sur une phase so-
lide. Après lavage, dans la seconde étape, l’ajout du ligand
marqué (hormone ou dérivé marqué) permet la mesure des
sites restés libres. Cette méthode repose sur des bases
physicochimiques bien établies et présente l’avantage de ne
pas mettre en contact direct le ligand avec le sérum. Elle est,
de ce fait, en principe à l’abri des interférences dues à des
anomalies des protéines de transport ou à des anticorps
anti-hormones thyroïdiennes. En méthode manuelle elle
reste délicate et son développement actuel est lié à son
automatisation.
Dosages en une étape
Une seule incubation met en contact le sérum, le ligand et
l’anticorps. Pour assurer la validité de ces dosages, le ligand
doit conserver sa réactivité vis-à-vis de l’anticorps sans
interagir avec les protéines de liaison. Ce ligand peut d’une
façon générale être considéré comme un analogue de l’hor-
mone avec laquelle il doit conserver une certaine parenté
structurale. Le marqueur est porté soit par le ligand, soit par
l’anticorps.
Les premières techniques par ligand marqué qui utilisaient
un traceur radioactif ont fait l’objet de vives critiques, en
raison de leur sensibilité à l’influence de l’albuminémie
[17]. D’autres ligands marqués sont maintenant utilisés.
Dans le cas des traceurs macromoléculaires, l’hormone
peut être liée à une enzyme (traceur conjugué) ou une
immunoglobuline par exemple. Ces ligands de masse mo-
laire élevée ont en général une réactivité négligeable avec
les protéines de transport [18]. Des ligands biotinylés ou
d’autres dérivés de l’hormone sont aussi employés.
Dans le cas de la technique par anticorps marqué, mainte-
nant très répandue, le ligand est fixé à une phase solide ce
qui bloque ou limite sa réactivité avec les protéines de
transport [19]. Pour la T4L le ligand est soit de la T4
(dosage homologue), soit de la T3 (dosage hétérologue).
Pour la T3L le ligand est soit de la T3 (dosage homologue),
soit de la di-iodothyronine (dosage hétérologue).
À l’heure actuelle les dosages les plus utilisés sont des
immunodosages non isotopiques automatisés en deux éta-
pes ou une étape avec anticorps marqué ou ligand macro-
moléculaire.
Performances techniques [4]
Pour la T4L et la T3L respectivement, les limites de détec-
tion sont < 2 pmol/L et < 0,5 pmol/L. Ces valeurs sont suf-
fisantes pour l’utilisation clinique de ces dosages. Les coef-
ficients de variation (imprécision totale) sont
respectivement<7%et<10%.Pour la T3L en particulier
des progrès sont souhaitables. Le domaine de mesure peut
être compris entre 60 et 130 pmol/L pour la T4L et 0,5 -
40 pmol/L pour la T3L. Avec les immunodosages de rou-
tine, si le résultat de T4L ou T3L obtenu est au-delà du
dernier étalon de la gamme d’étalonnage, un résultat exact
ne pourra pas être obtenu par dilution. En effet, l’équilibre
initial entre hormone liée et hormone libre tend à se rétablir
après dilution dans un tampon inerte. Cette propriété peut
être mise à profit pour tester la sensibilité d’une méthode de
dosage à la capacité de fixation des protéines du sérum [7].
Influence des inhibiteurs de liaison —
Maladies non thyroïdiennes sévères — Héparine
La mesure des concentrations d’hormones libres est sou-
mise à l’influence de facteurs susceptibles de modifier
l’équilibre libre - lié : dilution, pH, force ionique, nature du
tampon et température (le dosage doit être fait à 37 °C). Des
inhibiteurs de liaison (ou compétiteurs) peuvent éventuel-
lement entrer en compétition avec les hormones thyroïdien-
nes pour la liaison aux protéines de transport.
Parmi ces inhibiteurs figurent des médicaments tels que le
furosémide, les salicylates et des anti-inflammatoires non
stéroïdiens (diclofénac, fenclofénac). L’effet à court terme
se traduit par une augmentation des hormones libres qui
peut à plus long terme, après mise en jeu du rétrocontrôle,
être suivie d’une baisse de l’hormone totale et d’une nor-
malisation de l’hormone libre [20]. L’effet inhibiteur de ces
médicaments est renforcé quand l’albuminémie est basse et
quand la concentration sérique d’inhibiteurs endogènes
augmente comme chez les patients atteints de maladies
générales sévères, dans le sérum desquels le rôle des acides
gras libres (AGL) comme inhibiteurs de liaison est sus-
pecté. En particulier dans l’insuffisance rénale chronique
ces inhibiteurs et les médicaments peuvent agir en cascade
[21].
L’élévation de la T4L observée lors d’un traitement à l’hé-
parine, même de bas poids moléculaire et à faible dose, est
expliquée par la libération d’AGL, in vivo et in vitro [9]. La
libération d’AGL, conséquence de l’activation de la lipo-
protéine lipase, est plus importante quand la concentration
des triglycérides est élevée. En pratique, afin de minimiser
l’effet de l’héparine de bas poids moléculaire, le prélève-
ment devra être effectué au minimum 10 heures après l’in-
jection et le sérum conservé moins de 24 heures à 4 °C
avant dosage.
Pour toutes ces raisons, c’est chez les patients hospitalisés
atteints de maladies graves non thyroïdiennes que la varia-
bilité des résultats de T4L et de T3L reste la plus grande et
que l’interprétation du résultat devra tenir le plus grand
compte de la méthode utilisée [22-24]. En particulier, plus
la dilution de l’échantillon est importante, plus l’effet des
compétiteurs est atténué et plus le résultat de T4L mesuré
in vitro est abaissé par rapport à sa valeur in vivo.Dela
même façon, l’intensité de la baisse de la T3L chez ces
patients dont la T3T est souvent basse dépend beaucoup de
la trousse utilisée. Outre les effets de la dilution, la présence
d’albumine ajoutée dans les réactifs dans le but d’amortir
Dosage des hormones thyroïdiennes
Ann Biol Clin, vol. 61, n° 4, juillet-août 2003 415
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 24/05/2017.
 6
6
 7
7
 8
8
 9
9
 10
10
1
/
10
100%