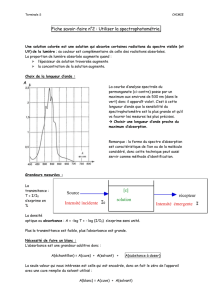
k V Φ = ⋅ ⋅Φ i

Photométrie
Nous allons voir dans ce chapitre comment les phénomènes d'émission et d'absorption de lumière par les
atomes ou les molécules peuvent être utilisés pour le dosage de certaines solutions les contenant. Pour
cela, nous devrons préalablement définir quelques grandeurs "photométriques" c'est-à-dire relatives à la
mesure de la lumière.
1 Le flux lumineux
1.1 Mise en évidence de l'énergie lumineuse
Un faisceau de lumière transporte de l'énergie. Cette
énergie peut être mise en évidence par l'expérience
illustrée par la figure 2 : un thermomètre dont le
réservoir a été noirci afin d'absorber l'énergie, est éclairé
par un faisceau lumineux. On constate au bout de
quelques instants une augmentation de la température.
L'énergie transportée par le faisceau lumineux s'est
transformée en chaleur sur la partie noire.
C'est aussi cette énergie, transportée par le faisceau
lumineux, qui impressionne la rétine et provoque le
mécanisme de la vision.
Flux lumineux
La température
monte
Fig 2 : Un faisceau lumineux transporte de l’énergie.
Cette énergie transformée en chaleur provoque une
élévation de la température.
1.2 Le flux énergétique
e
Φ
Une lampe à incandescence envoie de la lumière, donc de l'énergie, dans toutes les directions de
l'espace qui l'entoure.
On appelle flux énergétique, la quantité d'énergie émise, sous forme de rayonnement, par
une source lumineuse, pendant l'unité de temps.
Dans le système international d'unités, le flux énergétique s'exprime donc en joule par seconde,
c'est-à-dire en watt. Il est analogue à une puissance.
Pour une lampe à incandescence, le flux énergétique est la puissance indiquée sur la lampe.
Remarque :Le Soleil envoie sur la Terre un flux énergétique d'environ
17
2 10 W
× !
1.3 Le flux lumineux
Φ
l
Un flux énergétique pénétrant dans l'oeil produit sur la rétine une sensation lumineuse. Cette
sensation dépend, à flux énergétique donné, de la personne qui reçoit la lumière mais aussi de la
longueur d'onde de celle-ci. La sensation est en particulier plus intense pour de la lumière jaune
que pour de la rouge ou de la bleue.
On est donc amené à définir un autre flux que l'on appelle flux lumineux, qui est proportionnel au
flux énergétique, mais qui dépend de l'effet produit sur l'oeil. Le flux lumineux s'exprime en lumen
(
m
l
)
Il se calcule à l'aide de la formule
m e
k V
λ
Φ = ⋅ ⋅Φ
l
Le facteur k
m
est une constante qui permet de relier le watt et le lumen :

k
m
= 683 lumens par watt
V
λ
est l'efficacité lumineuse relative sur l'oeil de la longueur d'onde λ. Comme l'oeil présente
un maximum de sensibilité pour la radiation vert-jaune de longueur d'onde 555 nm, on choisit
V 1
λ
=
pour cette longueur d'onde. Pour les autres longueurs d'onde
V
λ
, est inférieur à 1 et
elle s'annule en dehors de l'intervalle 400 - 750 nm (fig. 3).
Pour une lampe de 60 W, le flux lumineux est de 600 lumens. Pour un tube fluorescent de 40 W, il
est de 2900 lumens.
Ces sources lumineuses émettent une lumière complexe composée de nombreuses longueurs
d'onde, le flux lumineux émis est alors la somme des flux correspondant à toutes les composantes
monochromatiques.
Fig 3 : Variation de l’efficacité lumineuse relative d’une
lumière sur l’œil en fonction de sa longueur d’onde.
L’œil est plus sensible vers 550 nm (couleur jaune-vert)
1.4 Mesure d'un flux lumineux ou énergétique
Le flux émis par une source lumineuse peut se mesurer : on utilise pour cela une cellule
photoélectrique, un phototransistor … Ce sont des récepteurs sensibles à la lumière qui, lorsqu'ils
sont éclairés par un faisceau lumineux, sont parcourus par un courant électrique dont l'intensité
est, dans certaines conditions, proportionnelle au flux reçu .
2 Absorbtion de lumière par une solution : Transmittance et absorbance.
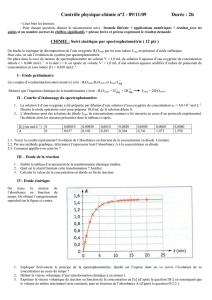
2.1 Les couleurs des solutions
La couleur d’une solution d’un composé est la conséquence de l’absorption d’une partie de la
lumière provenant d’un faisceau de lumière blanche qui la traverse.
Si la solution absorbe une partie de la lumière dans un domaine de longueurs d’ondes, la couleur
perçue par l’œil est la couleur complémentaire de celle associée aux photons absorbés.
Les domaines de longueurs d’ondes des six
couleurs de base sont indiqués dans le tableau ci-
dessous :
Couleur
absorbée
Longueur d’onde
(nm) Couleur perçue
Rouge 620-700 Cyan
Jaune 560-590 Bleu
Vert 520-560 Magenta
Cyan 480-500 Rouge
rouge
cyan
jaune
bleu vert
Couleurs
absorbées par le
permanganate
de potassium
Couleur du
permanganate
perçue par l’oeil

Bleu 420-460 Jaune
Magenta 380-420 vert
D’après CAPES et AGREGATION de Sciences Physiques :
100 manipulations de chimie. Chimie Générale et Analytique de Jacques Mesplède et
Jérôme Randon (Ed. Bréal)
Si la couleur absorbée est l’une des couleurs de base, la couleur perçue est celle qui figure en opposé dans
les triangles des couleurs ci-dessus.
Mais en réalité, comme la perception de l’œil n’est pas la même pour toutes les longueurs d’onde (il est
plus sensible pour le jaune que pour le bleu ou le rouge), la sensation visuelle diffère un peu.
Si la solution absorbe dans un domaine quelconque, la couleur perçue se déduit approximativement à
partir des triangles des couleurs.
Ainsi, comme l’a montré l’expérience réalisée avec la lumière issue de différents filtres à travers une
solution de permanganate de potassium dans l’eau, l’absorption est grande dans le cyan et le jaune et est
maximale dans le vert. L’œil perçoit les couleurs opposées : magenta, rouge et bleu dont le mélange
restitue la couleur caractéristique du permanganate de potassium en solution.
2.2 Transmittance T
Si nous éclairons une cuve contenant une solution
absorbante à l'aide d'un faisceau de lumière
monochromatique, nous constatons qu'à la sortie de la
cuve, le flux lumineux émergent est inférieur au flux
lumineux incident (fig. 5). La solution a donc absorbé
une partie de la lumière et transmis l'autre partie.
cuve avec
0
Φ
t
Φ
solution absorbante
Flux incident Flux transmis
t 0
Φ < Φ
Fig5
Si on note
0
Φ
, le flux lumineux (ou énergétique) incident et
t
Φ
, le flux lumineux (ou
énergétique) transmis, on appellera transmittance T de la solution le rapport du flux transmis au
flux incident, soit :
t
0
T
Φ
=
Φ
La transmittance, rapport de deux grandeurs de même nature s'exprime sans unité.
D'après sa définition même, la transmittance est inférieure ou égale à 1. Elle est égale à 1 pour une
solution qui n'absorbe pas du tout la lumière.
2.3 Absorbance A

Par définition, on appelle absorbance A d'une solution de transmittance T, le logarithme décimal
de l'inverse de T, soit
t
0
1
A log log
T
Φ
= =
Φ
Comme T, A n'a pas d'unité mais varie théoriquement entre 0 et l'infini. Dans la pratique A n'excède par
2, comme nous le verrons par la suite.
la figure 6 montre les variations relatives de T et A (pour une même solution) en fonction de
λ
.
fig 6
3 : Loi de Beer Lambert pour une solution absorbante
3.1 Enoncé
L'étude expérimentale de l'absorbance de
nombreuses solutions éclairées en lumière
monochromatique montre qu'elle dépend de
quatre facteurs :
l'épaisseur de solution traversée
la longueur d'onde de la lumière
utilisée;
la nature du soluté que contient la
solution
la concentration de la solution.
solution de concentration c
Flux
incident Flux transmis
l
Fig 7
Beer et Lambert ont montré que l'absorbance A d'une solution est donnée par la loi :
A c
ε
= ⋅ ⋅
l
(fig. 7)
-
l
est l'épaisseur (en m) de la solution traversée par la lumière.
- c est la concentration molaire (en mol.m
-3
) de cette solution.
-
ε
est le facteur qui dépend à la fois de la nature du soluté et de la longueur d'onde utilisée. On l'appelle
coefficient d’extinction molaire ou absorbance linélique molaire et on l'exprime en m
2
.mol
-1
dans le
système international.
Pour une solution donnée,
ε
varie beaucoup avec la longueur d'onde de la lumière utilisée (fig. 8) et très
peu avec la température.

Fig 8 : Variation de A avec la longueur d’onde pour
une solution de KMnO4. La courbe présente un
maximum à environ 525nm
3.2 Conditions d'utilisation de la loi
Pour que la loi puisse s'appliquer, il faut que certaines conditions soient remplies :
la lumière doit être monochromatique;
les solutions utilisées doivent être très peu concentrées sous peine d'absorber toute
la lumière ;
les solutions testées doivent être homogènes (ni suspension, ni émulsion) et non
fluorescentes.
3.3 Absorbance d'un mélange
Si une solution contient deux espèces absorbantes (ou plusieurs) de concentrations respectives c
l
et c
2
(c
3
, c
4
, ... ) qui ne réagissent par l'une sur l'autre, l'absorbance du mélange est alors la somme
des absorbances dues à chaque constituant du mélange:
1 2 1 1 2 2
A A A ( ...) c c ( ...)
ε ε
= + + = ⋅ ⋅ + ⋅ ⋅ +
l l
4 Dosage d’une solution par spectrophotométrie
4.1 Le spectrophotomètre
L'absorbance d'une solution étant une fonction linéaire de sa concentration, on pourra, à partir de
la mesure de son absorbance, déterminer la concentration molaire de la solution. L'absorbance
d'une solution peut se mesurer en utilisant l'appareil approprié qui est le spectrophotomètre (fig.
9). Il en existe de nombreux modèles mais tous possèdent :
une ou plusieurs lampes : par exemple une lampe à incandescence à filament de
tungstène pour la lumière visible et une lampe au deutérium pour l'ultraviolet.
un monochromateur, prisme ou réseau ou filtres , qui permet la séparation des
longueurs d'onde émises par la lampe. La rotation du monochromateur permet de
sélectionner la radiation désirée.
une ou deux cuves dans lesquelles on placera la solution à doser et de l'eau pour
laquelle l’absorbance A est nulle (étalonnage de l'appareil),
un système de mesure de l’absorbance A comportant une cellule photoélectrique, un
amplificateur, et un affichage de l'absorbance.
 6
6
 7
7
 8
8
 9
9
1
/
9
100%