3 – CLASSIFICATION PERIODIQUE DES ELEMENTS et évolution

51
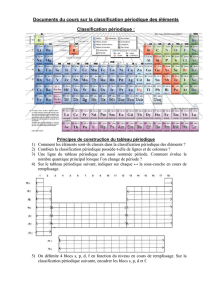
3 – CLASSIFICATION PERIODIQUE DES ELEMENTS
et évolution de grandeurs caractéristiques
Structure de la classification
A l'origine…
... diverses classifications des éléments "par familles", en fonction
de leurs propriétés chimiques (et physiques).
Exemple : tableau de Mendéléev (1869).
Classement par masses atomiques croissantes, qui prévoyait
l'existence d'éléments découverts bien plus tard...
Puis…
… classification établie à partir de la connaissance de la structure
électronique des atomes.
Si on classe les éléments par valeurs croissantes du numéro
atomique Z, apparaît une répétition périodique de leurs
grandeurs caractéristiques et de leurs propriétés.
La périodicité apparaît clairement comme le résultat de la
configuration électronique des éléments.
Constitution du tableau périodique
Lignes : chaque ligne est une période correspondant au
remplissage progressif des niveaux électroniques.
Quand on aborde le remplissage d'une nouvelle couche
électronique (niveau s), on passe à la ligne suivante.
Colonnes : les groupes d'éléments ayant des propriétés
communes apparaissent dans chaque colonne.
Ils ont les mêmes configurations électroniques de valence.

52
Classification périodique
Configurations électroniques de valence et blocs
1s
1
1s
2
2s
1
2s
2
2p
1
2p
2
2p
3
2p
4
2p
5
2p
6
2s
2
2s
2
2s
2
2s
2
2s
2
2s
2
3s
1
3s
2
3p
1
3p
2
3p
3
3p
4
3p
5
3p
6
3s
2
3s
2
3s
2
3s
2
3s
2
3s
2
4s
1
4s
2
4s
2
4s
2
4s
2
4s
1
4s
2
4s
2
4s
2
4s
2
4s
1
4s
2
4p
1
4p
2
4p
3
4p
4
4p
5
4p
6
3d
1
3d
2
3d
3
3d
5
3d
5
3d
6
3d
7
3d
8
3d
10
3d
10
4s
2
4s
2
4s
2
4s
2
4s
2
4s
2
5s
1
5s
2
5s
2
5s
2
5s
2
5s
1
5s
2
5s
2
5s
2
5s
2
5s
1
5s
2
5p
1
5p
2
5p
3
5p
4
5p
5
5p
6
4d
1
4d
2
4d
3
4d
5
4d
5
4d
6
4d
7
4d
8
4d
10
4d
10
5s
2
5s
2
5s
2
5s
2
5s
2
5s
2
6s
1
6s
2
6s
2
6s
2
6s
2
6s
1
6s
2
6s
2
6s
2
6s
2
6s
1
6s
2
6p
1
6p
2
6p
3
6p
4
6p
5
6p
6
5d
1
5d
2
5d
3
5d
5
5d
5
5d
6
5d
7
5d
8
5d
10
5d
10
6s
2
6s
2
6s
2
6s
2
6s
2
6s
2
7s
1
7s
2
7s
2
6d
1
6s
2
6s
2
6s
2
6s
2
6s
2
6s
2
5d
1
6s
2
6s
2
6s
2
6s
2
6s
2
6s
2
6s
2
5d
1
6s
2
4f
2
4f
3
4f
4
4f
5
4f
6
4f
7
4f
7
4f
9
4f
10
4f
11
4f
12
4f
13
4f
14
4f
14
7s
2
6d
1
7s
2
6d
1
7s
2
6d
1
7s
2
7s
2
7s
2
6d
1
7s
2
7s
2
7s
2
7s
2
7s
2
7s
2
7s
2
6d
1
7s
2
6d
2
5f
2
5f
3
5f
4
5f
6
5f
7
5f
7
5f
9
5f
10
5f
11
5f
12
5f
13
5f
14
5f
14
bloc f
bloc s
bloc p
bloc d

53
Evolution des énergies de 1ère ionisation
L'énergie d'ionisation d'un atome fait référence à la formation de
l'ion positif dans son état fondamental.
Ainsi, l'énergie de 1ère ionisation est l'énergie minimale
nécessaire pour former le cation mono-chargé, c'est à dire
"arracher" à l'atome l'électron le moins lié.
La valeur de I1 indique si l'ultime électron de valence est faiblement
ou fortement lié.
Elle traduit donc l'aptitude de l'atome à céder "plus moins
facilement" cet électron de valence...
Tendances générales d'évolution dans le tableau périodique
• augmentation de gauche à droite le long d'une période.
• diminution de haut en bas dans une colonne.
Evolution des énergies de 2ème, 3ème ,... ionisation
On peut poursuivre le processus d'ionisation en arrachant à l'atome
successivement les électrons les moins liés et en créant ainsi
des ions 2 fois chargés, 3 fois chargés,... dans leur état
fondamental.
Noter que pour un élément donné, on a toujours :
I2 > I1
L'énergie d'ionisation
I1 > 0
correspond au processus
−
+
+→ eXX fondétatfondétat ..
E
0
I
1

54
Energies de 1ère ionisation (eV)
0
5
10
15
20
25
1 6 11 16 21 26 31 36 41 46 51 56 61 66 71 76 81 86 91 96 101
Z
He
Ne
Ar
Kr
Xe
K
Na
Rb
Li
Rn
Cs Fr

55
Comparaison entre énergies de 1ère et 2ème ionisation (eV)
H
Li
Be BC
NO
F
Ne
Na Mg Al Si PSCl Ar
He
Li
Be
BC
N
OF
Ne
Na
Mg
Al Si PSCl
Ar
K
K
He
0
10
20
30
40
50
60
70
80
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19
Z
I1 (eV)
I2 (eV)
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
1
/
15
100%