Récidive d`un myxome Cardiaque non Familial

108
,</4:7:240%?94=40990':7?80H0< %<480=><0
Correspondance
Fennira Sana
Service de Cardiologie, Hôpital Habib Thameur.
8, rue Ali Ben Ayed- Montfleury 1008-Tunis
Mail : [email protected]
Récidive d’un myxome cardiaque non familial :
A propos d’un cas
Recurrence of a non-family cardiac myxoma:
A case report
Résu mé
Le myxome est la tumeur cardiaque primitive la plus fréquente. Le plus souvent la résection chirurgicale
est un traitement définitif. Cependant, quelques cas de récidive ont été rapportés dans la littérature. Dans
ce cadre nous rapportons l’observation d’un myxome cardiaque non familial qui a récidivé 6 ans après
la 1ère résection, découvert à l’occasion d’une échocardiographie de contrôle et qui a nécessité la réinter-
vention chirurgicale.
Summ ary
Cardiac myxomas are the most common primary cardiac tumors. Surgical resection usually provides
definitive treatment. However, postoperative tumor recurrence has been described. We report the case of
a cardiac myxoma recurrence detected in cardiac echocardiography 6 years later and have necessitated
the surgical reoperation.
0994<,$,9,9>4>$,:?==093,7/4,-4-77:?C0*,==49073,58:<,==09<,-0>,4=09:?==,0>34,+,4<43=09,8:?9
$:1409<,408$:9/:=
Service de Cardiologie, Hôpital Habib Thameur, Tunis, Tunisie
Mots-clés
Myxome cardiaque ;
Récidive ; échocardiogra-
phie
Keywords
Cardiac myxoma;
Recurrence;
Echocardiography
FAIT clINIqUE
, # )&)!#
. / ( # - # ( (

IntroductIon
?;DGK;H7H;:;I97H:?EF7J>?;I56B;CONEC;
;IJB7JKC;KH97H:?7GK;B7FBKI<HUGK;DJ;9>;PBk7:KBJ;
7L;9 KD; ?D9?:;D9; :k;DL?HED C?BB?ED :k?D:?L?:K
F7H 7D 56 &7 HU9?:?L; :; CONEC; 97H:?7GK; 7FHVI B7
HUI;9J?ED 9>?HKH=?97B; ;IJ H7H; 7DI 9; 97:H; DEKI
H7FFEHJEDI B; 97I :kKD; HU9?:?L; :; CONEC; ?DJH7
7KH?9KB7?H;
caS cLInIquE
'H ' S=U :; 7DI I7DI 7DJU9U:;DJI F7J>EBE=?GK;I
DEJ78B;I 9EDIKBJ7?J FEKH :OIFDU; :k;<<EHJ ULEBK7DJ
:;FK?ICE?I:k7==H7L7J?EDHU9;DJ;&k;N7C;DF>OI?GK;
JHEKL7?J KD HEKB;C;DJ :?7IJEB?GK; 7K <EO;H C?JH7B 7L;9
78I;D9; :; I?=D;I :k?DIK<<?I7D9; 97H:?7GK;
&kUB;9JHE97H:?E=H7CC; ?DI9H?L7?J KD HOJ>C; HU=KB?;H
I?DKI7BR9O9B;IC?DI7DIJHEK8B;:;B79ED:K9J?EDD?
:;B7H;FEB7H?I7J?ED&7H7:?E=H7F>?;:KJ>EH7NUJ7?JI7DI
7DEC7B?;I &kU9>E97H:?E=H7F>?; JH7DIJ>EH79?GK; ..
E8@;9J?L7?JKD;C7II;U9>E=VD;EL7B7?H;<7?I7DJ9C:;
=H7D:7N;I?V=;7DJ7KD?L;7K:;BkEH;?BB;JJ;=7K9>;7L;9
KD; 87I; :k?CFB7DJ7J?ED B7H=; 7K D?L;7K :K I;FJKC
?DJ;H7KH?9KB7?H; ?=KH;
;JJ; C7II; Ik;D9B7L7?J F7H CEC;DJ 7K D?L;7K :;
BkEH?<?9; C?JH7B &; :?7=DEIJ?9 :; CONEC; E8IJHK7DJ
BkEH?<?9;C?JH7B7UJUFEIU;JB;C7B7:;7UJU7:H;IIU;D
KH=;D9; FEKH 9>?HKH=?; &k;N7C;D C79HEI9EF?GK;
JHEKL7?J KD; JKC;KH FEBOBE8U; :k7IF;9J >UCEHH7=?GK;
:; 9EDI?IJ7D9; =UB7J?D;KI; <H?78B; ;J DED 7:>UH;DJ;
?=KH;&;F7J?;DJ78UDU<?9?U:kKD;;NUHVI;:;9;JJ;
C7II;7L;9<;HC;JKH;:;:U<;9JI;FJ7BF7HF7J9>
&kUJK:; >?IJEBE=?GK; CEDJH7?J KD; <EHC7J?ED JKCEH7B;
9EDIJ?JKU; F7H :;I 9;BBKB;I 9ED@ED9J?L;I <KI?<EHC;I ;J
UJE?BU;I DED 9E>UI?L;I DED 7JOF?GK;I :?IF;HIU;I :7DI
KD IJHEC7 CONEZ:; ;J <?8H?BB7?H; :UB?C?JU F7H KD; <?D;
97FIKB;<?8H;KI;;J7IF;9J>?IJEBE=?GK;;IJ9ECF7J?8B;
7L;9 KD CONEC; 97H:?7GK; ;FK?I B; F7J?;DJ <KJ
7IOCFJEC7J?GK;;JIK?L?HU=KB?VH;C;DJRB79EDIKBJ7J?ED
7DI7FHVIBk..:;9EDJH]B;FK?IBkU9>E97H:?E=H7F>?;
JH7DIE;IEF>7=?;DD; E8@;9J?L7?;DJ KD; C7II; U9>E=VD;
7HHED:?;NCCI;II?B;?DIUHU;IKHB;L;HI7DJ=7K9>;
:K I;FJKC ?DJ;H7KH?9KB7?H; ;J F7HJ?;BB;C;DJ 7K F7J9>
?=KH;
109
Cardiologie Tunisienne
2ème Trimestre 2013
Fennira S. & al.
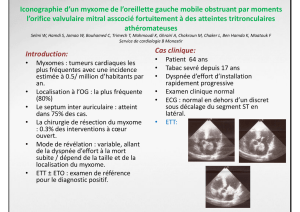
Figure 1: coupe 4 cavités en sous costal. Masse échogène
attachée au septum interatrial.
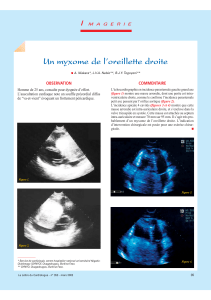
Figure 2 : Aspect macroscopique du myxome auriculaire
gauche
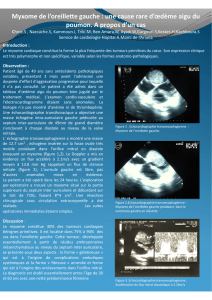
Figure 3 : Récidive du myxome atrial gauche objectivée à
l’ETO

110
Cardiologie Tunisienne
2ème Trimestre 2013
#D' I& *) #"&
BB;DkUJ7?J F7I E8IJHK9J?L; BB; ULEGK7?J B; :?7=DEIJ?9
:;HU9?:?L;:KCONEC; &; F7J?;DJ 7?J 8UDU<?9?U :kKD;
:;KN?VC; HUI;9J?ED 9>?HKH=?97B; :; 9;JJ; C7II; ;J :;
IED FU:?9KB; &k;N7C;D 7D7JECEF7J>EBE=?GK; :; B7
F?V9; EFUH7JE?H; 9ED<?HC7?J B; :?7=DEIJ?9 :; CONEC;
&k;DGKWJ;<7C?B?7B;D;JHEKL7?JF7I:;97II?C?B7?H;I:7DI
B7 <7C?BB; FHVI 7DI :kULEBKJ?ED B; F7J?;DJ <KJ
HU=KB?VH;C;DJ IK?L? #B Dk7 F7I ;K :k7KJH; HU9?:?L; :K
CONEC;
dIScuSSIon
&; H?IGK; :; HU9?:?L; :; CONEC; 97H:?7GK; ;IJ :;
BkEH:H;:;R:7DIB;I<EHC;IIFEH7:?GK;I#BF7II;R
:7DIB;I<EHC;I<7C?B?7B;I;J=H?CF;R:7DIB;
IOD:HEC; :; 7HD;O CONEC; 9KJ7DU CONEC;
97H:?7GK; ;J IOD:HEC; :; 9KI>?D= &7 HU9?:?L; F;KJ
IKHL;D?H:7DI:;ICONEC;ICKBJ?FB;I56&7HU9?:?L;
;IJ FBKI <HUGK;DJ; :7DI B;I <EHC;I <7C?B?7B;I R
JH7DIC?II?ED7KJEIEC7B;:EC?D7DJ;GK?9EDIJ?JK;DJ
:;ICONEC;I97H:?7GK;I56-;KB;C;DJ97I:;:;KN
HU9?:?L;I:;CONEC;I97H:?7GK;IEDJUJUH7FFEHJUI:7DI
B7B?JJUH7JKH;56
&7HU9KHH;D9;F;KJWJH;I;9ED:7?H;IE?JRKD;HUI;9J?ED
?D9ECFBVJ;:;B7C7II;IE?JRBk;C8EB?;:;I<H7=C;DJI
7K9EKHI:;Bk;NJH79J?ED:;IJKC;KHIJHVI<H?78B;IIE?JR
B7 FHUI;D9; :; JKC;KHI CKBJ?<E97B;I DED ?:;DJ?<?78B;I
C79HEI9EF?GK;C;DJ EK FBKI H7H;C;DJ R B7
JH7DI<EHC7J?EDC7B?=D;:KCONEC;56
?;D GKk?BI IE?;DJ 8UD?DI 9;HJ7?DI CONEC;I 97H:?7GK;I
F;KL;DJ 7LE?H KD FEJ;DJ?;B ?DJH?DIVGK; :; C7B?=D?JU
9ECC; T7 UJ7?J :UCEDJHU F7H B7 FHUI;D9; :; BUI?EDI
>?IJEBE=?GK;I FBKI 7=H;II?L;I :7DI B;I F?V9;I
7D7JECEF7J>EBE=?GK;I :;I CONEC;I HU9?:?L7DJI56 &;
CONEC; F;KJ CWC; I; JH7DI<EHC;H ;D I7H9EC; D
;<<;JB;CONEC;;IJKD;JKC;KH:kEH?=?D;;D:E97H:?GK;
9EDIJ?JKU; :; 9;BBKB;I CUI;D9>OC7J;KI;I 7O7DJ
CKBJ?FB;IFEJ;DJ?;BIBB;IIEDJ97F78B;I:;:;L;D?H:;I
9;BBKB;ID;KH7B;IEK;D:EJ>UB?7B;I56
&7 CKJ?<E97B?JU :;I JKC;KHI C?9HEI9EF?GK;I ;IJ KD;
>OFEJ>VI;FEII?8B;D;<<;J:7DI9;HJ7?DI97IFK8B?UI
B;CONEC;HU9?:?L7DJ;IJ:;I?V=;:?<<UH;DJ:;B7JKC;KH
FH?C?J?L;56
&7 IOCFJEC7JEBE=?; ;D 97I :; HU9?:?L; ;IJ I?C?B7?H; R
9;BB; :K CONEC; FH?C?J?< BB; :UF;D: :; B7 J7?BB; :K
I?V=; ;J :; B7 CE8?B?JU :; B7 JKC;KH /D EK FBKI?;KHI
IOCFJ]C;I :; B7 JH?7:; JOF?GK; F;KJ WJH; FHUI;DJ
799?:;DJ ;C8EB?GK; I?=D;I =UDUH7KN 9ED=;IJ?ED
FKBCED7?H; ;I <H7=C;DJI JKCEH7KN EK :;I ;C8EBI
<EHCUIRB7IKH<79;:;B7JKC;KHF;KL;DJ;NFB?GK;HB;I
799?:;DJI ;C8EB?GK;I GK? IKHL?;DD;DJ 9>;P :;I
F7J?;DJI 56 &7 B?8UH7J?ED :k?DJ;HB;KA?D; F7H B7
JKC;KH ;IJ R BkEH?=?D; :;I I?=D;I =UDUH7KN 7IJ>UD?;
<?VLH; 7HJ>H7B=?; 7C7?=H?II;C;DJ &;I I?=D;I
:k?DIK<<?I7D9; 97H:?7GK; =7K9>; IEDJ B?UI R KD;
UL;DJK;BB; E8IJHK9J?ED :; B7 L7BL; C?JH7B; F7H B;
CONEC; ;F;D:7DJ B; CONEC; ;IJ IEKL;DJ
7IOCFJEC7J?GK; :kE^ Bk?DJUHWJ :K 9EDJH]B;
U9>E97H:?E=H7F>?GK; HU=KB?;H &7 L?J;II; :; 9HE?II7D9;
:K CONEC; 97H:?7GK; F;KJ WJH; 97B9KBU; ;D I; 87I7DJ
IKH B;I C;IKH;I U9>E97H:?E=H7F>?GK;I ?JUH7J?L;I EK IKH
Bk?DJ;HL7BB;GK?IUF7H;B;I?DJ;HL;DJ?EDI;JJ;L?J;II;
;IJ:;BkEH:H;:;CCCE?IEKCC56
&;JH7?J;C;DJ :;I CONEC;I O 9ECFH?I B;I HU9?:?L;I;IJ
;II;DJ?;BB;C;DJ 9>?HKH=?97B &7 9>?C?EJ>UH7F?; ;J B7
H7:?EJ>UH7F?; EDJ UJU :UB7?IIU;I /D 97I :;
JH7DIFB7DJ7J?ED97H:?7GK;FEKHCONEC;7JH?7BHU9?:?L7DJ
7UJUH7FFEHJU:7DIB7B?JJUH7JKH;56&k7DJ?9E7=KB7J?ED
;IJ H;9ECC7D:U; :7DI B;I 97I ?DEFUH78B;I 7<?D :;
FHUL;D?HB;H?IGK;J>HEC8E;C8EB?GK;
&7FHUI;D9;:;:?<<UH;D9;I=UDUJ?GK;I;DJH;B;I<EHC;I
<7C?B?7B;I;JDED<7C?B?7B;I567UJU:UCEDJHU;7DI
B; <KJKH KD; UJK:; =UDUJ?GK; 9>;P B;I F7J?;DJI EFUHUI
FEKHCONEC;97H:?7GK;F;HC;JJH7?J:;:UF?IJ;H9;KNR
H?IGK; :; HU9?:?L; *EKH B; CEC;DJ KD 9EDJH]B;
U9>E97H:?E=H7F>?GK; HU=KB?;H 9>;P 9;I F7J?;DJI ;IJ
H;9ECC7D:U7<?D:;<7?H;B;:?7=DEIJ?9:kKD;UL;DJK;BB;
HU9?:?L;RJ;CFI
'9 7HJ>O *' *?;>B;H $' -9>7<< "0 .>; I?=D?<?97D9; E< CKBJ?FB;
H;9KHH;DJ 7D: 9ECFB;N; 97H:?79 CONEC7 $ .>EH79 97H:?EL7I9 IKH=
7HD;O $ "HKIA7 &- ;7K9>7CF ! !EH:ED " EC?D7DJ ?D>;H?
J7D9;E<J>;9ECFB;NE<CONEC7IIFEJJOF?=C;DJ7J?ED7D:;D:E9H?D;
EL;H79J?L?JO'7OE9B?D?9FHE9
'7H:EP7;HDIJ;?D ;HH;?H7'KBJ?FB;H;99KH;D9;IE<DED<7C?
B?7B97H:?79CONEC7I.;N";7HJ#DIJ$
$7D7H,$KJ;B;O,- ;DJED*-7HA7H*->EKB:M;F;H<EHC7FH;EF;
H7J?L; 9EHED7HE=HF>O 7D=?E=H7F>O ?D 7BB 97I;I E< 7JH?7B CONEC7
7J;J>;H97H:?EL7I9KB7H?DJ;HL
';D:EI7;HDIJ;?D ;HH;?H7'KBJ?FB;H;9KHH;D9;IE<DED<7C?
B?7B97H:?79CONEC7I.;N>;7HJ?DIJ$
B;L;B7D:1;IJ78O-%7HF,.H;7JC;DJE<?DJH797H:?79JKCEH
$'
KJ7DO$(7?H0(7I;;CK::?D(7?H!'7JJED7H:?79JKCEHI
:?7=DEI?I7D:C7D7=;C;DJ&7D9;JED9EB
*7HM?I,$7L?;H!$7L?;H-7L?:"7H:?79CONEC7F;H?EF;H7
J?L;:?7=DEI?IKI?D=7CKBJ?CE:7B?C7=?D=7FFHE79>7D:IKH=?97BEKJ
9EC;?D7B7H=;9ECJ;CFEH7HOI;H?;I#DJ;H79J97H:?EL7I9J>EH79IKH=
HE97 ';I7 !' EC?D=K;P )B?L;H !' ,7C?H;P / CKBJ?FB;
H;9KHH;D9; E< 7 IFEH7:?9 97H:?79 CONEC7 KH $ 97H:?EJ>EH79 IKH=
CEOII7A?I # D7IJ7IJ7I?7:?I ! '7H=EI * 0EJJ;7I 0 -;9ED: H;99K
H;D9;E<97H:?79CONEC7?D7OEKD=F7J?;DJ97I;H;FEHJ#DJ;H$
7H:?EB
&7: 0- $7?D $ =7HM7B7 - -?D>7 0% ,?=>J 7JH?7B JH7DII;FJ7B
7FFHE79><EHB;<J7JH?7BCONEC7";7HJBKD=?H9
#F;A!H;DJK=0*EB7J*;A;H)-KH=?97BC7D7=;C;DJE<97H:?79
CONEC7$97H:IKH=
-M7HJP' &KJP$>7D:7D0-&7D:7D-JH?7BCONEC7F7J>EBE
=?9 JOF;I JKCEH BE97J?ED 7D: FH;I;DJ?D= IOCFJECI $ 97H: IKH=
7A7;;D !,;7:ED'$EI;BB?$-'?BB;HIKH=?97BEKJ9EC;?D
F7J?;DJIM?J>FH?C7HO97H:?79JKCEHIC$IKH=
B8;AA7B?3EKB7>O717>?: 'ONEC;I7JH?7KNRFHEFEI:;97I
EFUHUI,;L'7H97H:?E
rEFErEncES
1
/
3
100%