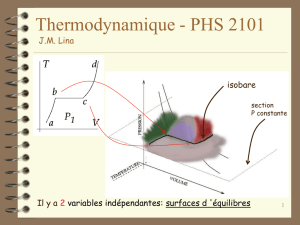
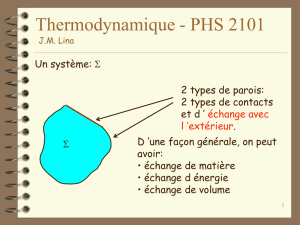
Document

Considérons le
cycle moteur
:
T2
V
P
T1
W < 0
Q
1
< 0
T1
T2
Q
2
> 0
Premier Principe
:
W + Q
1
+ Q
2
= 0 (cycle)
- W : travail fourni
Q
2
: combustion requise
- Q
1
: énergie perdue!
Thermodynamique - PHS 2101- III-2/2
J.M.Lina

T2
V
P
T1
W < 0
Q
1
< 0
T1
T2
Q
2
> 0
rendement
:
W + Q
1
+ Q
2
= 0 (cycle)
W
= - W : travail fourni
Q
= Q
2
: énergie requise
Q’
= - Q
1
: énergie perdue!
11 <−=== Q
Q'
Q
Q'
-
Q
Q
W
η
Rendement du cycle moteur:
Considérons le
cycle moteur
:
Thermodynamique - PHS 2101- III-2/2
J.M.Lina

Le
cycle
précèdent
est réversible
:
P
T2
V
T1
W > 0
Q
1
> 0
T1
T2
Q
2
< 0
Cette fois-ci
:
W
= W : travail requis
Q’
= - Q
2
: chaleur évacuée
vers la source chaude
Q
= Q
1
: chaleur
extraite à la
source froide!
Vous avez un cycle
réfrigérant
!
Thermodynamique - PHS 2101- III-2/2
J.M.Lina

Le
cycle
précèdent
est réversible
:
P
T2
V
T1
W > 0
Q
1
> 0
T1
T2
Q
2
< 0
Rendement du cycle réfrigérant
:
W
= W : travail requis
Q’
= - Q
2
: chaleur évacuée
Q
= Q
1
: chaleur
extraite
1
1−
=== Q
Q'
Q'-Q
Q
W
Q
η
Rendement du cycle réfrigérant:
Thermodynamique - PHS 2101- III-2/2
J.M.Lina
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
1
/
19
100%