cinétique enzymatique 2

128
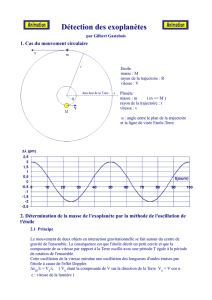
4. Effet de la concentration d’enzyme
Lorsque [enzyme] << [substrat],
la vitesse de la réaction est
directement proportionnelle à la
concentration de l’enzyme.
La vitesse de réaction augmente
lorsque [enzyme] augmente.
Ceci est vraie pour n’importe quel
catalyseur.
[Enzyme]
Vitesse de réaction
129
3.6 Cinétique enzymatique
Les enzymes détiennent leur
sélectivité et capacité à accélérer
la vitesse d’une réaction de la
formation d’un complexe enzyme-
substrat:
E + S E·S E + P
où E= enzyme, S= substrat,
E·S = complexe enzyme-substrat
et P est le produit de la réaction
La formation du complexe E·S
donne lieu à un état de transition
pour la réaction ayant une barrière
énergétique d’activation (∆G‡)
abaissée; la réaction a donc moins
besoin d'un apport externe
d'énergie pour se dérouler.
∆G‡=
(sans enzyme)
=∆G‡
(avec enzyme)
(D’après Tinoco, Sauer, Wang & Puglisi,
Physical Chemistry: Principles & Applications
In Biological Sciences, 4eéd., 2002)
∆Gréaction
n’est pas affectée
par l’enzyme

130
La 1ère étape critique dans une réaction avec catalyse enzymatique est la
formation du complexe E·S.
Puisque c’est le complexe E·S qui est le réactif dans l’étape de conversion du
substrat en produit, sa concentration détermine la vitesse de réaction.
La vitesse de réaction est maximale lorsque toutes les molécules d’enzyme sont
complexées au substrat. Cette situation correspond à des concentrations élevées
de substrat, où l’enzyme est soit disant saturée avec le substrat.
Pour une concentration fixe de l’enzyme, un graphique de la vitesse initiale de
réaction (Vo) en fonction de la concentration initial du substrat [S] exhibe une
courbe typique d’une cinétique de saturation, où un plateau est observé à [S]
élevées lorsque V= vitesse maximale (Vmax).
VoVitesse de réaction approche Vmax
Voα[S]
131
3.6.1 Réaction à un substrat:
cinétique de Michaelis-Menten
Le modèle cinétique est basé sur la formation du complexe E·S selon les
étapes suivantes:
(1)
On cherche une expression qui relie la vitesse de réaction aux
concentrations du substrat et de l’enzyme et aux vitesses des étapes
individuelles; le point de départ étant que la vitesse de réaction est égale
au produit de [E·S] et la constante de vitesse k3: V=k3[E·S] (2)
Les vitesses de formation et de décomposition du complexe E·S sont
données par:
vitesse de formation de E·S = k1[E][S] (3)
vitesse de décomposition de E·S = (k2+ k3)[E·S] (4)
Sous conditions d’état stable: k1[E][S] = (k2+ k3)[E·S] (5)
Par réarrangement de l’éqn 5, on obtient: (6)
E + S ES E + P
k1
k2
k3
132 )/(
[E][S]
S][E kkk +
=⋅

132
L’équation précédente peut être simplifiée en définissant une nouvelle
constante, Km, qui est la constante de Michaelis:
(7)
En substituant l’expression pour Kmdans l’éqn 6, on obtient:
(8)
De plus, [S] ≈[S]totale, si [E] << [S]
[E] = [E]totale – [E·S] (9)
Donc, [E·S]=([E]totale –[E·S])[S]/Km (10)
Par réarrangement de l’éqn 10, on obtient (11)
1
32
mkkk
K
+
=
m
[E][S]
S][E K
=⋅
m
totale [S]
[S]
]E[S][E K+
=⋅
133
En substituant cette expression pour [E·S] dans l’équation 2, on obtient:
(12)
La vitesse maximale, Vmax, est atteinte lorsque tout les sites enzymatiques
sont saturés de substrat, c’est à dire, lorsque [S] >> Kmet donc
[S]/([S] + Km) tend vers 1. Il s’ensuit que Vmax = k3[E]totale (13)
La substitution de l’éqn 13 dans l’éqn 12 donne l’équation de Michaelis-
Menten:
(14)
L’équation de Michaelis-Menten décrit la courbe cinétique de Vo-[S]:
- Pour des concentrations faibles de substrat, lorsque [S] << Km,
V = [S]Vmax/Kmet la vitesse est directement proportionnelle à la
concentration de substrat.
- Pour des concentrations élevées de substrat, lorsque [S] >>Km, V = Vmax
et la vitesse est indépendante de la concentration de substrat.
- La signification de la constante Kmest évidente. Lorsque [S] = Km,
V = Vmax/2. Kmest la concentration de substrat nécessaire pour que
l'enzyme atteigne (1/2) Vmax.
m
totale3 [S]
[S]
]E[ K
kV +
=
m
max [S]
[S]
K
VV +
=

134
Méthodes graphiques pour la détermination
de Kmet Vmax
Il y a deux régions d’utilité analytique dans la courbe cinétique de
Vo-[S]: - [S] < 0.1Km(pour la quantification du substrat)
-[S] > 10Km(pour la quantification d’enzyme)
Dans le développement d’un essais enzymatique, il est important de
connaître la valeur de Kmde l’enzyme et d’ajuster la valeur de Vmax afin que
l’essais est accompli dans le minimum de temps requis pour une précision
donnée.
Il y a quatre méthodes graphiques pour établir les valeurs de Kmet Vmax
dans des conditions expérimentales données: Lineweaver-Burk, Eadie-
Hofstee, Hanes et Cornish-Bowden-Eisenthal.
Les quatre méthodes nécessitent des données expérimentales pour la
vitesse initiale de la réaction en fonction de la concentration initiale du
substrat pour une concentration fixe d’enzyme.
135
Données cinétique
01234567
0.0
0.1
0.2
0.3
0.4
0.5
0.6
Vo (∆A340nm/min)
[S] mmol/L

136
1. Méthode de Lineweaver-Burk
Le réciproque de l’équation de Michaelis-Menten est très utile pour l’analyse
des données de cinétique:
qu'on peut aussi écrire
et qui se simplifie en
L'avantage de cette transformation mathématique est qu'elle permet de
tracer un graphique 1/Vovs 1/[S] dont la courbe est en fait une droite pour
les enzymes obéissant à la relation Michaélienne entre vitesse de réaction
et concentration du substrat.
]S[
]S[1
max
m
o⋅
+
=V
K
V
]S[
111
max
m
maxo
⋅+= V
K
VV
]S[
]S[
]S[
1
maxmax
m
o⋅
+
⋅
=VV K
V
137
Y = (1.12551±0.08398) + (3.79517±0.06135) * X
-0.5 0.0 0.5 1.0 1.5 2.0 2.5 3.0 3.5
0
2
4
6
8
10
12
14
1/Vo
1/[S]
Km/Vmax
1/Vmax
-1/Km
Km= 3.37 mmol/L
Vmax = 0.89 unités d’absorption/min
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
1
/
13
100%