Exercice n° : Proposer la synthèse du composé 3 ci

Exercice n° :
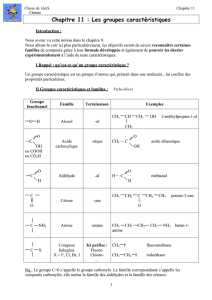
Proposer la synthèse du composé 3 ci-dessous à partir de deux composés symétriques. L’un
deux est le 1,2-diaminobenzène 1 :
N
N
NH
2
NH
2
+
?
1,2-diaminobenzène
1composé inconnu
23
1-
donner la formule du composé inconnu
2
2-
proposer un mécanisme réactionnel conduisant au composé
3
à partir des composés
1
et
2
. Cette réaction s’effectue en milieu acide modéré.
Exercice n° :
Ecrire un mécanisme en milieu acide qui rende compte de la mutarotation du D-Mannose
représenté ci-dessous :
CHO
HHO
HHO
OHH
OHH
CH
2
OH
O
OH
OH
OH
HO
OH
H
carbone anomérique
H
+
D-Mannose
Problème n°1
Problème n°1Problème n°1
Problème n°1
(les trois parties sont indépendantes)
Le phosphate de pyridoxal (PLP) est un composé indispensable au fonctionnement de
nombreuses enzymes sa formule développée est la suivante :
N
CHO
OH
POH
2
C
H
+
P = groupe phosphate
PLP
1) La fonction carbonyle de cette molécule peut réagir avec le groupe amine des acides
aminés. A titre d’exemple la réaction avec l’alanine s’écrit :

N
CHO
OH
POH
2
C
H
++
H
2
N CH CH
3
COOH
Alanine
PLP
N
CH
OH
POH
2
C
H
+
NCH
CH
3
COOH
+ H
2
O
A
a- proposer un mécanisme pour cette réaction en milieu acide modéré
b- quels sont les atomes du composé A
AA
A susceptibles d’être impliqués dans une liaison
hydrogène intramoléculaire, la dessiner
2) a- Montrer que l’hydrogène en α de la fonction –COOH du composé A
AA
A est mobile :
N
CH
OH
POH
2
C
H
+
NCH
CH
3
COOH
A
H mobile
c- Ecrire l’équilibre acide-base correspondant à l’arrachement de cet hydrogène
d- Ecrire toutes les formes mésomères de la base conjuguée B
BB
B du composé A
AA
A
3) La fonction imine du composé
B
BB
B
peut être hydrolysée en milieu basique selon le
bilan réactionnel suivant :

N
CH
OH
POH
2
C
H
NC
CH
3
COOH
+ OH-
N
CH
OH
POH
2
C
H
NH
2
CH
3
COO
-
O
+
B
Proposer un mécanisme réactionnel pour cette hydrolyse
Problème (extrait de concours) :
Transformation du fructose-1,6 diphosphate (FDP) en dihydroxyacétone phosphate (DHAP)
et glycéraldéhyde-3 phosphate (G3P).
On étudie les réactions suivantes :
Réaction 1
O
HO H
HCH
2
OPO
32-
HOHOH
2-
O
3
POH
2
Cconfiguration du carbone non précisée
CH
2
OPO
32-
CH
2
OPO
32-
O
HO H
H OH
H OH
FDP furanose FDP
Réaction 2
CH
2
OPO
32-
CH
2
OPO
32-
O
HO H
H OH
H OH
CH
2
OPO
32-
CH
2
OH
OCH
2
OPO
32-
H OH
O
H
DHAP G3P
FDP
+
Le FDP sous sa forme ouverte cétonique, le DHAP et le G3P sont représentés en projection
de Fischer
1°) Réaction 1 :
1.1 Quelle est la nature de la réaction 1 qui donne lieu à l’équilibre entre la forme cyclique et
la forme ouverte cétonique du FDP ?
1.2 Ecrire le mécanisme de la réaction 1 catalysée par un couple acido/basique faible
(BH
+
/B), en schématisant le FDP sous la forme :

O
R
H
OH
R
forme schématique du FDP
2°) Réaction 2 :
2.1 Quelle est la liaison du FDP rompue dans la réaction 2 ?
2.2 Quelle est la nature de la réaction 2 ?
2.3 Donner un mécanisme théorique pour la réaction 2 catalysée par un couple
acido/basique faible (BH
+
/B). Dans le but de clarté il est demandé de représenter la FDP
sous sa projection de Fischer.
2.4 Il a été démontré qu’au site actif de l’enzyme qui catalyse la réaction 2 la première étape
de cette réaction est la formation d’une imine protonée impliquant le –NH
2
d’une chaîne
latérale de la lysine (de l’enzyme) et la fonction carbonyle du FDP.
2.4.1 Donner le mécanisme détaillé de la formation d’une imine entre une cétone R-CO-R et
une amine primaire R’-NH
2
catalysée par un acide faible (milieu acide modéré).
2.4.2 L’Enzyme est symbolisée par :
+
H
3
N E
B
H
2
N E
BH
+
a) écrire la formule développée de l’imine formée au site actif à partir du FDP.
b) Proposer un mécanisme de formation du G3P à partir de cette imine protonée. On ne
demande pas le mécanisme de l’hydrolyse de l’énamine formée simultanément qui
conduit au DHAP.
1
/
4
100%