Réaction Ac-Ag Et ses appllications pratiques

Réaction Ac-Ag
Et ses appllications pratiques
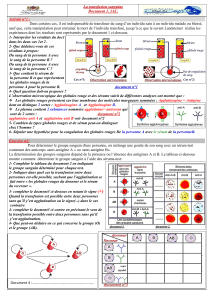
Caractéristiques générales de la réaction AcAg.
La liaison AgAc
Pour qu’il y ait une liaison, il faut une « complémentarité stérique » entre le paratope de l’Ac et l’épitope
de l’Ag.
Complémentarité stérique : complémentarité conformationnelle, représentation dans l’espace.
Complémentarité entre l’épitope et le paratope :
La cristallographie aux rayons x permet de définir une structure 3D d’une molécule. A partir de cette
technique on a pu définir la structure d’un Ac. Aux régions hypervariables, les AA vont se lier aux Ac
(comme une mâchoire). Cela concerne que quelques AA, tout le reste est plus ou moins une
« charpente ».
Il y a bcp de forces de répulsions, les liaisons intermoléculaires sont faibles => énergie de liaison faible.
Si l’épitope correspond bien à l’épitope alors il n’y a que des forces d’attraction et pas de forces de
répulsions. Alors les forces d’attractions sont optimales et l’énergie de liaison est bcp plus importante.
La bonne complémentarité entre paratope et épitope entraîne la formation du Complexe Immun.
Paratope et Epitope peuvent se déformer légèrement pour permettre la formation du CI.
Forces impliquées :
Ici, il s’agit de liaisons de faibles énergies (et non de liaisons covalentes !). Ces liaisons sont dues à
plusieurs forces, établies entre AA hypervariables et épitope.
Force électrostatiques : qui s’établies entre groupement chimiques ionisées de charges opposées.
Forces issues des liaisons hydrogènes : issues de liaisons entre atomes de charges +, comme H,
et des atomes de charges -, comme O ou N. l’interaction avec H est d’autant plus forte qu’il y a
exclusion des molécules d’eau.
Forces issues des interactions hydrophobes : liées à des groupements apolaires (de nombreux AA
sont hydrophobes ex : AA aromatiques, tyrosine, phénylalanine, …). Se sont ces interactions qui
représentent les forces les plus importantes dans le CI. => composante majeure de l’énergie de
liaison entre épotipe et paratope.
Forces de VanDerWaals : crées par les interactions des nuages électroniques des atomes.
Ces 4 types de forces sont attractives ce qui entraînent et maintiennent la formation du CI.
Affinité :
Elle caractérise la force de cette liaison.
Affinité = forces attractives + forces répulsives
Comment se mesure-t-elle ?
Elle se définit par réaction chimique : Ac+Ag
Ac-Ag
Cette réaction est réversible, le complexe peut se dissocier.
Cette réaction peut aussi se définir par des constantes cinétiques avec :
k = constante cinétique d’association
k’ = ‘’ ‘’ de dissociation
A l’équilibre, la vitesse d’association = vitesse de dissociation. On établit alors une constante
d’association de l’équilibre KA :

KA = [Ac-Ag]eq / [Ac]eq x [Ag]eq
Vitesse d’association:
Va = k[Ac][Ag]
Vitesse de dissociation :
Vd = k’ [Ac-Ag]
A l’équilibre, Va = Vd
k[Ac][Ag] = k’ [Ac-Ag]
KA = [Ac-Ag]eq / [Ac]eq x [Ag]eq => k/k’
On peut aussi établir une constante de dissociation à l’équilibre KD:
KD = 1/KA
L’unité de KA est L/mol, et pour KD c’est le mol/L.
Quand il y a une bonne affinité alors KA est élevé. On dispose d’Ac dont KA=1010 L/mol.
Bonne affinité : 103 < KA <1010 L/mol.
Avidité :
Pour avoir une bonne affinité :utilisation d’Ac monoclonaux. C’est-à-dire un seul type d’Ac donc un seul
paratope.
Quand on utilise du sérum polyclonal avec des Ag multivalents (cad plusieurs épitopes) : on parle
d’avidité car on mélange plusieurs Ac différents capables de reconnaître plusieurs épitopes différents.
nAc + mAg nAc-mAg appelé “complexe multimoléculaire”.
L’avidité se caractérise par une constante
d’association KA qui donne toujours KA>>KA1 ;KA2.
Le complexe est plus stable du fait des différents
Ac qui se lient à l’Ag.
Remarque KA : Cette constante dépend du nombre d’Ac capables de reconnaître des déterminant
antigéniques différents. Elle dépend également des conditions physico-chimiques du milieu cad pH,
Temp°C et force ionique du milieu. En faisant varier ces conditions, on stabilise ou on fragilise le CI.
Spécificité des Ac
Représente la capacité d’un Ac à discriminer 2 déterminants antigéniques semblables en se liant à eux
avec une affinité différente.
Ici on considère que l’Ac est bien spécifique de c
déterminant antigénique car grande différence
d’affinité entre les deux déterminants antigéniques.
Les Ac monoclonaux sont dit bcp plus spécifiques pour un Ag donné que pour les sérums polyclonaux.
Il peut y avoir des réactivités croisées car les Ac produits pour un Ag1 peuvent reconnaître des
déterminants antigéniques de d’autres Ag. Ces problèmes de réactivités croisées se posent quand un
Ag possède des déterminants antigéniques similaires ou semblables. Donc avec le même sérum
polyclonal on peut avoir une affinité élevée KA1 avec Ag1 et une autre affinité KA2 pour l’Ag Ag2. Il faut
alors vérifier et contrôler si le sérum est bien spécifique des Ag.
Pour les Ac monoclonaux la spécificité est meilleure car il y a un seul type d’Ac donc le problème des
réactivité croisée est moindre.

Détection des réactions AgAc
Présentation générale
Ac : outil de reconnaissance spécifique ; il faut être capable de détecter le CI.
Détection visible à l’œil nu :
Agglutination : Elle concerne les Ag insolubles ou particulaires.
Précipitation : L’Ag est solubles mais le CI formé précipite.
Complexe Immun non visible à l’œil nu :
On utilse des révélateurs pour mettre en évidence le CI.
Marquage : marquage soit de l’Ag soit de l’Ac. Il existe trois types de marquages : fluorescent
« immunofluorescence », radioactif « radioimmunologie », enzymatique « immunoenzymologie ».
Utilisation du complément
Neutralisaiton de l’activité enzymatique : Bloquer l’activité enzymatique d’un Ac notamment du type
toxique (quand il y formation du CI, il y a perte de l’activité toxique).
Les réactions d’Agglutination
Principe :
Les réactions d’agglutinations sont la conséquences d’Ac agglutinant sur un Ag particulaire permettant
ainsi la formation de ponts spécifiques entre les particules ce qui constitue un réseau visible sous forme
d’amas.
Conditions nécessaires à l’agglutination :
Les particules généralement utilisées sont chargées + ce qui entraîne une répulsion. Or pour former un
réseau il faut former des liaisons afin de rapprocher les particules. Ces liaisons > forces de répulsions.
Ces forces de répulsions sont reliées à un potentiel (zêta) :
ζ = σ / D x racine carrée de μ
avec σ = charge électrique des particules
avec D = constante d’électricité
avec μ = force ionique du milieu
Ce potentiel traduit les force de répulsions entre les particules.
Il existe de sAc qui agglutinent facilement à des particules et d’autres qui ont plus de difficultés, ce sont
les Ac non-agglutinants. Les Ac agglutinants sont souvent des immunoglobulines du types IgM, et les
non-agglutinants sous souvent du type IgG. Ce qui permet de dire que si les Ac sont, ou non, agglutinant
et la valence (IgM = 10 ; IgG = 2).
Les Ig masquent les chargent électriques à la surface des particules (surtout IgM car elles sont plus
grosses).
On peut également agir sur la force ionique du milieu en augmentant la concentration en ions (plus la
force ionique augmente plus zêta diminue).
La température joue une rôle important. L’augmentation de la Temp°C = agitation moléculaire. Cette
agitation favorise la rencontre Ac/Ag.
L’agglutination est plus rapide à températures élevées qu’à températures froides. Dans de cas on parle
« d’Ac chauds ». Il existe des Ac froids qui agglutinent davantage à 4°C qu’à 37°C. En effet l’agitaiton
moléculaire peut rompre les liaisons entre les particules.
Les différents types d’agglutination :
Il faut que l’Ag soit particulaire. Cet Ag peut-être naturellement particulaire (comme les Ag A,B,O porté
sur les hématies). Dans ce cas, il y a « Agglutination Active ».
Il existe aussi des Ag que l’on a rendu particulaire = Ag que l’on fixé volontairement sur une particule (ex
billes de latex). Dans ce cas il s’agit d’une « Agglutination Passive ».

Exemple d’agglutination directe :
Détermination des groupes A,B,O = on veut mettre en évidence une particularité sur les hématies =>
technique qualitative.
Détermination de la quantité d’Ac contenu dans un sérum => technique quantitative. Travail effectué en
microplaques.
Application : Ac antiSalomnelles et antiBrucella.
Titre du Sérum = quantité d’Ac présent dans le sérum qui correspond à l’inverse de la plus grande
dilution du sérum pour laquelle on observe encore une réaction d’agglutination.
Exemple d’agglutination active indirecte :
Ac non- agglutinant : ne provoque pas d’agglutination spontanée =>souvent des IgG. On utilise des
« artifices » afin d’obtenir des réactions d’agglutination. => Ajouter au milieu réactionnel des
macromolécules qui vont réaliser des ponts fixés à des molécules voisines.
On crées des ponts artificiels entre les Ig. On utilise souvent du sérum d’Albumine provenant de Bœuf
(SAB). Il existe aussi du Dextran et du Ficoll qui ont la même fonction que la SAB.
Remarque : Hydrolyse partielle de l’Ag
Parfois avec des IgM il n’y a pas d’agglutination. L’utilisation d’enzymes protéolytiques qui vont couper
certaines parties de l’Ag sont responsables de la non agglutination.
Exemple d’agglutination Passive :
Au départ l’Ag est soluble puis on le rend particulaire en le fixant sur un support spécial (ex bille de latex
ou hématies). Or les hématies ne sont pas antigéniquement neutres. Il faut alors vérifier que les
hématies n’agglutinent pas spontanément avec les Ac utilisées. De plus les hématies sont fragiles ; elles
s’hémolysent très facilement : on utilise du formol pour les rendre plus stables (en plus de les garder à
+4°C).
L’Ag choisit peut se fixer très facilement sur les hématies, par simple contact ou réaction chimique.
Les billes de latex présentent un autre avantage : antigéniquement neutre et très peu fragiles.
L’agglutination sera pourtant plus sensible et plus simple avec les hématies plutôt qu’avec les billes de
latex.

Exemple : Recherche du facteur rhumatoïde :
Polyarthrite rhumatoïde = maladie auto-immune ( IgM anti Fc IgG).
Les réactions d’agglutination sont donc très faciles à mettre en œuvre et peu coûteuses, en générale.
Elles sont appliquées dans de nombreux domaines (notamment microbiologie, sérologie, alimentair et
biotechnologie).
Réactions de précipitation
Principe :
Réactions qui mettent en jeu des Ac spécifiques et des Ag solubles. Il se forme un réseau
multimoléculaires entre les Ac et les Ag et qui, dans certaines conditions, peut devenir insoluble et
précipite. Contrairement à la réaction d’agglutination, ce n’est pas des particules mais des protéines ou
des polyosides.
C’est donc le CI qui devient insoluble. C’est peut-être sa taille qui en est à l’origine.
Remarque : Il existe des Ac qui précipite et d’autres qui ne précipitent pas. C’est-à-dire que tous les cI
ne sont pas précipitables.
Conditions nécessaires à la précipitation :
Il y a différents milieux possibles pour la précipitation : liquide ou « solides » (= gélifié). Les
concentrations en Ag et en Ac sont déterminantes.
Il existe différentes techniques pour déterminée la quantité du précipité : en milieu liquide on peut
analyser le résultat via un dosage de Kjeldahl pour mesurer l’azote qui est directement proportionnelle
au précipité (cf . Biochimie) ; par néphélométrie ; par turbidimétrie ; …
Il y a augmentation de la quantité de précipité en fonction de la quantité
d’Ag. Puis un plateau quand la quantité de précipité est maximal. Puis la
quantité de précipité diminue.
Quand il y a un excédant d’Ac, il n’y a en fait quasiment pas de réseau
moléculaire. Puis à l’équivalence, tout les Ac sont reliés aux Ag =
réseau macromoléculaire. On parle ici de « concentration optimale ».
Puis il y a un excédant de précipité = bcp d’Ag vont rester insolubles
mais quelques rares CI ne vont pas former de réseau.
Avant tout réaction de précipitation il faut définir les concentrations optimales entre Ac et Ag pour avoir le
maximum de précipité (ordre de grandeur de la concentration : entre 1 à 10µg/mL).
Il existe d’autres techniques plus sensibles.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
1
/
12
100%