TD 2 BIOPHYSIQUE Photon –Niveaux d`énergie dans un atome

TD 2 BIOPHYSIQUE
Photon –Niveaux d’énergie dans un atome –Interaction matière-rayonnement –
Radioactivité – Dosimétrie
Exercice 1 – Effet photoélectrique
On considère les résultats d’une expérience sur l’effet photoélectrique. Le tube photoélectrique utilisé
possède une électrode (cathode) couverte de césium. Les valeurs du potentiel électrique U0 appliqué
pour lesquelles le courant dans le tube photoélectrique tombe à zéro en fonction de l’inverse de la
longueur d’onde λ des raies d’une lampe spectrale est tracé ci-dessous.
Déterminer la valeur de la constante de Planck et donner le travail d’extraction W du césium. Donner le
domaine du spectre à laquelle les raies utilisées appartiennent.
Exercice 2 – Le photon
21 Montrer que l’énergie E d’un photon et sa longueur d’onde λ vérifient la relation :
.
22 Calculer la fréquence et la longueur d’onde dans le vide de l’onde associée à un photon γ
d’énergie 140 keV.
Exercice 3 - Atome d’hydrogène
Déterminer la longueur d’onde de la lumière émise lorsque l’électron de l’atome d’hydrogène passe
311 de l’état caractérisé par une valeur de n=3 à l’état n=2.
312 de l’état n=2 à l’état n=1.
Calculer les longueurs d’onde des frontières cotées ondes courtes des séries de Lyman et de Paschen du
spectre de l’atome de l’hydrogène. Utiliser la valeur expérimentale de RH=109677,6 cm-1 (constante de
Rydberg pour l’hydrogène).
321 Quelle est l’énergie des photons en exprimée en eV ?
322 Quelle est la signification de cette énergie ?
Aide : Formule de Rydberg pour hydrogène où
λvac est la longueur d'onde de la lumière dans le vide.
RH est la constante de Rydberg de l'hydrogène
n1 et n2 sont des entiers tels que n1 < n2.

Exercice 4 – Coefficients d’absorption
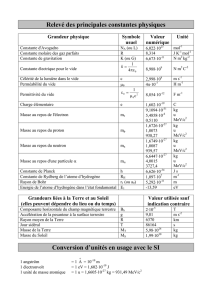
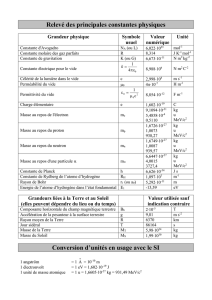
41 Calculer le coefficient d’absorption massique pour de l’eau H2O, densité ρ=1,000g/cm3, et du
lipide (composé modèle trioléine C57H104O6, densité 0,915g/cm3). On utilise la formule :
avec xi : pourcentage massique d’un élément i par rapport à la masse totale du
composé. On trouve les xi à partir de la formule du composé et des masses atomiques.
: coefficient d’absorption massique de l’élément.
Elément
Masse
atomique
Coefficient d’absorption
µ/ρ [cm2/g]
10 keV
50 keV
200 keV
H
1
0,385
0,335
0,243
C
12
2,373
0,187
0,123
O
16
5,953
0,212
0,124
42 Quelle est la proportion de photons transmis IT/I0 après le passage de 3cm de lipide ou d’eau pour
les différentes énergies ? A quelle énergie est-ce qu’on obtient le meilleur contraste défini comme
IT1 / IT2 ?
43 Donner la profondeur de pénétration avant l’atténuation de 90% des photons rayons X incidents
pour les deux matériaux et les trois énergies.
Exercice 5 – Energie de liaison du noyau
51 – Calculer l’énergie de liaison du noyau de et déterminer l’énergie de liaison du dernier neutron
de ce noyau. La masse de = 11,011402 u.
52 – Le noyau de est un des noyaux les plus stables. Sa masse atomique relative est égale à
54,93046. Déterminer son énergie de liaison par nucléon.
53 – Le noyau de lithium (M = 7,01601 u) est formé de 4 neutrons et 3 protons. Calculer le défaut de
masse lors de la formation du noyau.
Masse de l’électron me = 0,00055 u
Masse du neutron mn = 1,00866 u
Masse du proton mp = 1,00728 u
1 u = 1,66.10 - 27 kg
c = 3.10 8 m / s
Exercice 6 – Energie libérée
61 - En 2005, la décision a été prise de construire un réacteur de fusion expérimental à Cadarache dans
les Bouches du Rhône (ITER). Ici nous considérons quelques aspects d’un tel réacteur de fusion.
Dans des futurs réacteurs de fusion nucléaire on compte exploiter la réaction
Quelle sera l’énergie libérée par événement de fusion ?
Masse atomique 2H : 2,0141 ; 3H : 3,0160 ; 4He : 4,0026
A- 2,20 MeV
B- 4,4 MeV
C- 16,5 MeV
D- 17,6 MeV
E- 18,7 MeV.
62 - Quelle est l’énergie libérée lors de la désintégration β+ du 18F? Les masses atomiques suivantes sont
données : 18O : 17,99916 u ; 18F : 18,00094 ; 18Ne : 18,00571. Utiliser toutes les décimales pour le calcul.
A- 1,66MeV
B- 1,15 MeV
C- 0,63 MeV
D- 4,44 MeV
E- 3,93 MeV

63 - Le 210Po est soumis à une désintégration α pure qui produit un noyau de plomb.
L’énergie libérée est 5,4 MeV (énergie de la particule α : 5,3 MeV).
Les masses atomiques sont : 210Po=209,983 u ; 4He : 4,003 u.
A- On produit un noyau de 205Pb
Quelle est la masse atomique de l’isotope produit ?
B- 205,980 u
C- 205,974 u
D- La différence d’énergie entre celle de la particule α et l’énergie libérée est emportée sous
forme d’énergie cinétique par un antineutrino.
E- La différence d’énergie entre celle de la particule α et l’énergie libérée est emportée sous
forme d’énergie cinétique par le noyau de plomb formé après la désintégration.
Exercice 7 : Datation au carbone 14
71 – Dans un tronc d’arbre fossile, la proportion de 14C (par rapport au carbone 12, largement
prépondérant) est 8% de la proportion mesurée dans un arbre actuel de la même variété. Calculer
l’âge de l’arbre fossile.
72 – La datation par le carbone 14 suppose que la concentration en 14C est restée constante au cours des
âges. En réalité, en raison de modification du champ magnétique terrestre qui agit comme un
« bouclier » contre les rayons cosmiques, la teneur en 14C était plus importante à l’ère
préindustrielle qu’actuellement. Si on ne tient pas compte de cette variation, est-on conduit à une
sur- ou à une sous-estimation de l’âge des fossiles (cette correction est de l’ordre de 2500 ans
pour un âge supposé de 30000 ans) ?
Exercice 8 – Radioactivité
81 - Une source radioactive est constituée de deux radioéléments d’activités initiales égales et de périodes
respectives 1h et 3h. Au bout de combien de temps l’activité de l’une sera-t-elle inférieure à 1% de celle
de l’autre ? Montrer que le graphe, en coordonnées semi-logarithmiques, de l’activité totale de la source
en fonction du temps présente une partie incurvée puis une partie linéaire.
82 – Soit un échantillon d’iode
€
53
131I
de masse 0,8 mg pour lequel on compte le nombre de désintégrations
par minute, grâce à un compteur Geiger. On trouve 20 000. Ce même comptage effectué 8 jours après
donne 9 900.
821 – Déterminer la constante radioactive λ puis la période de l’iode
€
53
131I
.
822 – Calculer l’activité (ou vitesse de désintégration) de cet échantillon à l’instant initial.
On donne le nombre d’Avogadro : NA = 6.1023.
83 - Le 210Po est soumis à une désintégration α pure qui produit un noyau de plomb. L’énergie libérée est
5,4 MeV (énergie de la particule α : 5,3 MeV). Du polonium 210 a été utilisé dans le cas de
l’empoisonnement de A. Litvinenko. On considère une dose d’exposition au rayonnement de 20 Sv
comme létale. Litvinenko était mort 3 semaines après l’administration du 210Po. Estimer la quantité
minimale de 210Po qui a été utilisée en faisant l'hypothèse d'une absorption complète, un poids de la
victime de 80 kg, une distribution homogène dans l’organisme et en négligeant les décroissances
radioactives et biologiques. Le facteur d’efficacité biologique des particules α émises est de 20.
Activité présente dans l’organisme est:
A- 6⋅1010 Bq
B- 5⋅107 Bq
C- 640000 Bq.
Exercice 9 – Dosimétrie
91 - Une source a une activité initiale A0 et un période radioactive T et une constante radioactive λ. Le
nombre total de désintégrations N ayant lieu durant un temps très grand par rapport à T est donné par la
relation :

Quelle est la dose physique, due aux rayonnements β+, reçue par un patient de 70 kg à qui une activité
totale de 370 MBq de 18FDG a été administrée ?
(On suppose que sa période efficace dans l’organisme est de 70 min. L’énergie moyenne des rayons β+
est de 450 keV.)
A- 160 mGy
B- 2,3 mGy
C- 2,3 mSv
D- 160 mSv
E- 38 µGy
92 - Un ingénieur travaillant sur un réacteur de recherche a été accidentellement irradié par des neutrons.
Il a reçu une dose de 100 mSv en travaillant dans une zone dont le niveau de radiation dû aux neutrons
est de 80 mGy/heure.
A- Il a passé moins de 40 min dans cette zone.
B- Il a passé 75 min dans cette zone
C- Par définition, les rayons γ de 1 MeV ont un facteur d’efficacité biologique de 1,0.
D- Les rayons α ont des facteurs d’efficacité biologique élevés
E- Le facteur d’efficacité biologique des neutrons thermiques est plus petit que celui des rayons
γ de 200 keV car les neutrons interagissent peu avec la matière.
93 - Au moment de l’arrêt d’un réacteur, il y a une activité de 107 Bq dans un échantillon dû au 55Fe qui
a une période radioactive de 2,7 ans. Quelle sera l’activité restante après 20 ans ?
A- 58900 Bq
B- 6070 Bq
C- 5,8.106 Bq
Le se désintègre par capture électronique. Quel est son produit de désintégration ?
D-
E-
Exercice 10 – Période physique, période efficace, période biologique
101 - Le traceur 18FDG a été utilisé pour visualiser l’activité du cerveau d’un patient. La période
physique du 18F est de 1,8 h. Durant 4,4 h on perd 90 % de l’activité de 18F présente dans le cerveau.
Quelle est la période efficace du 18FDG dans le cerveau?
A- 1,50 h
B-1,32 h
Quelle est sa période biologique ?
C- 11 h
D- 4,5 h
E- 5 h
102 - On cherche à établir la période biologique de la protéine prothrombine humaine dans le plasma.
Pour cela, avant injection, on l’a marquée avec du 131I avec une période physique de 8 jours. On
détermine une période efficace de 2,1 jours. Quelle est la période biologique de la prothrombine ?
A-1,7 jours
B- 2,8 jours
C- 10,1 jours
103 - Une personne a accidentellement absorbé du 90Sr ayant une activité de 1000 Bq. La période
physique du 90Sr est de 28,5 ans. La période biologique est moins bien définie et elle est comprise entre
16 et 20 ans en fonction du patient. Quelle est l’activité moyenne au bout de 40 ans?
A- 27 Bq
B- 80 Bq

C- 177 Bq
D- 250 Bq
E- 378 Bq
104 - Du polonium 210 a été utilisé dans le cas de l’empoisonnement de A. Litvinenko. Sa période
radioactive est de 139 jours, sa période biologique de 60 jours.
La période efficace du 210Po dans l’organisme est :
A- 189 jours
B- 105 jours
C- 79 jours
D- 42 jours
E- 20 jours
1
/
5
100%