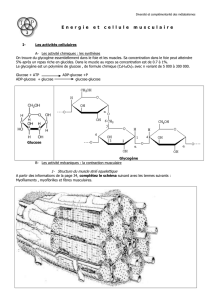
C + ATP - Parlons Chimie

'ATP n'est pas une source d'énergie, mais un vecteur d'énergie, qui
permet de "transporter" l'énergie des réactions qui la dégagent
(oxydation des sucres, etc.) à celles qui en ont besoin.
ATP + 2 H2O → ADP + Pi + H3O+ : ΔG°' = -30,5 kJ⋅mol-1
ATP + 2 H2O → AMP + PPi + H3O+ : ΔG°' = -45,6 kJ⋅mol-1.
L'énergie est donc stockée dans les liaisons entre les groupements phosphate. La
stabilité de ces liaisons en solution est assurée par leur énergie d'activation, que
les enzymes ont la capacité d'abaisser pour en faciliter l'hydrolyse.
Si l'énergie est ainsi stockée dans les liaisons anhydrides, on peut se demander quel est
l'intérêt pour les êtres vivants de synthétiser la molécule entière, et non uniquement des
pyrophosphate libres. La réponse est probablement dans la capacité des enzymes à
reconnaitre l'ATP, plus aisé à hydrolyser spécifiquement que des pyrophosphate libres,
très semblables à tous les groupements phosphate présents dans les biomolécules.
Les stocks d'ATP de l'organisme ne dépassent pas quelques secondes de
consommation. En principe, l'ATP est produite en permanence, et tout processus qui
bloque sa production (ce qui est le cas de certains gaz de combat conçus à cet effet, ou
de poisons, comme le cyanure, qui bloque la chaîne respiratoire, ou l'arsenic qui
remplace le phosphore et rend inutilisables les molécules phosphorées) provoque en
conséquence une mort rapide de l'organisme contaminé.
C'est alors qu'interviennent les molécules de créatine : elles lient un phosphate par une
liaison riche en énergie tout comme l'ATP. L'ADP peut donc ainsi redevenir de l'ATP par
couplage avec l'hydrolyse de la créatine-phosphate. La créatine recycle donc en quelque
sorte le phosphate libéré par hydrolyse de la molécule d'ATP originale. Elle permet de
conserver une énergie aussi facilement mobilisable que l'ATP, sans pour autant épuiser
les réserves d'ATP.
L'ATP ne peut être stockée à l'état brut excepté au sein des vésicules synaptiques, seuls
des intermédiaires de la chaîne de production de l'ATP peuvent être stockés. Exemple
du glycogène qui pourra se transformer en glucose et alimenter la glycolyse si
l'organisme a besoin de plus d'ATP. L'équivalent végétal du glycogène est l'amidon.
L'énergie peut aussi être stockée sous forme de graisses, par néo-synthèse d'acides
gras.
ATP + Glucose Glucose 6P + ADP ΔG°3= -4kcal/mol (3)
L’énergie libérée par l’hydrolyse de l’ATP permet de réaliser la phosphorylation du glucose.
Les transferts d’énergie par couplage sont très importants dans la cellule, les enzymes
représentant des

facteurs de couplage. En particulier, les réactions faisant intervenir l’ATP sont toujours
couplées.


Les voies de formation de l'A.T.P sont différentes
selon l'intensité de l'effort :
effort violent : les réserves d'A.T.P s'épuisant en quelques secondes, c'est la
phosphoprotéine qui en permet la formation pendant 15 secondes. Au delà,
l'A.T.P provient des stocks de glycogène intramusculaire et du glucose sanguin.
Les réserves en glycogène qui sont de 9 à 15 g/kg de muscle vont s'épuiser
rapidement et ne peuvent être transférées d'un muscle à l'autre. Le
renouvellement de l'ATP est surtout assuré par les mécanismes anaérobie

alactique : formation d'ATP à partir de la phosphocréatine et de la molécule
d'ADP. Processus sans O2 et sans acide lactique.
PC + ADP C + ATP
effort modéré : l'A.T.P provient de la dégradation du glycogène en glucose.
Processus sans O2 et avec du glucose qui se met en route dès que le taux de
phosphocréatine diminue dans le muscle.
Glucose + 3 ADP + 3 P 2 Lactases + 3 ATP
effort réduit : les acides gras fournissent l'A.T.P. Au bout de 10 minutes l'énergie
des glucides est égale à 90% de l'énergie totale. Après 40 minutes d'effort, 75% de
l'énergie provient du glucose sanguin et le reste de la dégradation des réserves
lipidiques. La consommation maximale d'oxygène d'un individu est un indicateur
pertinent de sa capacité à effectuer des exercices prolongés (plus de 400 mètres en
natation). Intervention du glucose et de l'O2.
C6H12O6 + O2 + ADP + P 6 H2O + 6 CO2 + ATP
 6
6
1
/
6
100%