Les anions multipolaires : une ionisation tout en douceur P

Molécules et noyaux déformés
Les anions multipolaires :
une ionisation tout en douceur
Ioniser une molécule provoque usuellement une modification plus ou moins importante
de la configuration des noyaux. Pour un assez grand nombre de systèmes moléculaires, il est
néanmoins possible d’opérer en douceur en créant de nouveaux ions négatifs qui possèdent
un électron très faiblement lié à grande distance des molécules neutres. L’étude de ces anions
est née d’un vieux problème de la mécanique quantique, celui des états liés dans un potentiel en
1/r
2
. Elle conduit à des applications dans la spectrométrie de masse de systèmes neutres, grâce à
un processus d’ionisation aisément réversible, ou dans la compréhension des mutations induites
par les rayonnements ionisants à la suite de la capture d’électrons par les bases de l’ADN
et de l’ARN.
LES E
´TATS LIE
´S DU POTENTIEL EN 1/r
2
P
armi les systèmes quantiques,
l’atome d’hydrogène joue un
rôle privilégié car l’électron y
est essentiellement soumis à l’inter-
action coulombienne variant en 1/r.
La résolution de l’équation de
Schrödinger montre alors qu’il existe
une infinité d’états liés, repérés prin-
cipalement par un nombre quantique
n, et dont les énergies sont données
par la formule de Rydberg,
E
n
=−R/n
2
, établie ilyaunsiècle.
La situation est très différente pour
un potentiel attractif à symétrie sphé-
rique en −C/r
2
qui présente un com-
portement physique pathologique en
tout ou rien. Ce potentiel admet une
infinité d’états liés d’énergies infini-
ment négatives si C est supérieur à
une valeur critique de 1/8 (en unités
atomiques) mais plus aucun état lié si
C<1/8. Pour tous les potentiels à
plus courte portée, en C/r
3
, C/r
4
..., il
existe toujours une infinité d’états
liés quelle que soit la valeur de C.
L’étude d’un potentiel en 1/r
2
a
longtemps été considérée comme par-
faitement académique et « dépourvue
de sens physique direct » (Traité de
mécanique quantique de Landau et
Lifschitz § 35). Elle a néanmoins
acquis un début d’intérêt physique
lorsqu’en 1947 Fermi et Teller ont
prédit qu’un électron devait être lié à
un dipôle électrique ponctuel – dans
un potentiel qui varie bien en −1/r
2
mais qui est aussi fortement aniso-
trope – pourvu que ce moment
dipolaire atteigne la valeur critique
de 1,625 debye [un dipôle est
constitué de 2 charges opposées
– voir encadré 1 – 1 debye (D) =
3,3 10
−30
C.m.]. Vingt ans après,
des théoriciens, dont J.-M. Lévy-
Leblond, étendent ce résultat à un
dipôle de taille finie. En 1970, des
physiciens moléculaires prédisent
l’existence d’anions baptisés « dipo-
laires » qu’il serait possible d’obtenir
à partir de molécules réelles possédant
un dipôle permanent de plus de
2,5 debye. Quelques observations
d’ions dipolaires ont effectivement
lieu à partir de 1984, mais dans
des conditions expérimentales non
contrôlées ne permettant pas de pré-
ciser le mécanisme de création de ces
ions. Ce n’est que lors de ces derniè-
res années que nous avons pu étudier
de façon systématique de tels ions
dipolaires et, très récemment, des ions
quadripolaires (voir leur définition
dans l’encadré 1).
D’UNE ORBITALE DIFFUSE A
`L’AUTRE
Dans un anion multipolaire, l’élec-
tron en excès se trouve dans une
orbitale de très grande extension spa-
tiale.Un moyen pour parvenir à l’y
placer est de « préparer » l’électron à
partir d’un atome dans un état très
excité (« état de Rydberg ») où il se
trouve déjà dans une orbitale diffuse
(cf. Images de la Physique 1985).
Lors d’une collision entre un atome
de Rydberg dans un état caractérisé
par le nombre quantique n et une
molécule possédant un moment dipo-
laire ou quadripolaire permanent, il y
a possibilité de capture par la molé-
cule neutre d’un électron initialement
lié au cœur ionique de l’atome excité.
Ce processus de transfert d’électron
se révèle très efficace mais unique-
ment dans une très faible plage d’ex-
citation des atomes de Rydberg ca-
ractérisée par le nombre quantique n,
centrée autour d’une valeur optimale
n=n
max
. Ce comportement très par-
ticulier en fonction du nombre n per-
met, comme le montre la figure 1, de
différencier clairement la formation
d’un ion multipolaire (celui d’adé-
nine) de celle d’un ion négatif de va-
lence (SF
6
−
) dont la dépendance en n
est monotone (les notions d’ions
– Laboratoire de physique des lasers,
UMR 7538 CNRS, Institut Galilée, Univer-
sité Paris 13, avenue J.-B. Clément, 93430
Villetaneuse.
52

Encadré 1
ANIONS DE VALENCE ET ANIONS MULTIPOLAIRES
Les atomes et les molécules sont des édifices neutres formés
d’un nombre d’électrons liés à un nombre égal de protons par
l’attraction coulombienne. Alors qu’il est relativement aisé
d’arracher un ou plusieurs électrons du cortège électronique
pour obtenir des ions positifs (cations) à partir de n’importe
quel atome, molécule ou agrégat, il est plus délicat d’attacher
un électron excédentaire tout en minimisant les perturbations.
En effet, ce nouvel électron subit à la fois l’attraction des
noyaux et la répulsion des autres électrons déjà présents qui
participent aux liaisons chimiques (électrons de valence). Un
anion est dit de valence lorsque le nouvel électron pénètre
dans une orbitale libre, semblable à celles qui assurent la
stabilité chimique de l’édifice moléculaire. La réorganisation
plus ou moins grande de la géométrie des noyaux se traduit
par une différence de structure entre l’ion négatif ainsi formé
et le système neutre (molécule isolée ou agrégat) qui lui a
donné naissance. Elle peut s’accompagner d’excitation de
vibrations, d’évaporation ou même de la dissociation de l’un
des constituants. Cela est particulièrement important dans un
édifice fragile tel qu’un agrégat moléculaire au sein duquel
les molécules sont liées entre elles par des interactions de
faible énergie (van der Waals ou liaisons hydrogène).
Suivant la distribution des charges dans la molécule, celle-ci
peut posséder un moment dipolaire µou quadripolaire Q. Ces
moments sont représentés de manière simplifiée par 2 charges
opposées dans le cas dipolaire et 3 charges alignées, la
charge centrale étant l’opposé du double des charges
extrêmes, dans le cas quadripolaire. Si une molécule ne
présente pas d’orbitale disponible pour un nouvel électron
mais un moment dipolaire µ ou quadripolaire Q, un électron
incident perçoit tout d’abord à grande distance un potentiel
qui peut être attractif charge-dipôle −µcos h
r2ou charge-
quadripole −Q
4r3
~
3 cos2h−1
!
, puis un potentiel répulsif à
courte distance au voisinage du nuage électronique de la
molécule (hest l’angle entre la direction incidente de
l’électron et l’axe principal de symétrie de la molécule).
L’ensemble est susceptible de former un puits de potentiel
dans lequel il peut y avoir un état lié si µ ou Q est supérieur
à une valeur critique. L’orbitale de l’électron en excès
possède alors une grande extension spatiale, l’anion est dit à
caractère multipolaire.
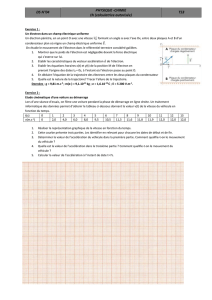
Figure - Densité de probabilité, dans un plan contenant l’axe dipolaire, de l’électron en excès d’un anion multipolaire d’adénine (µ =2,5 debye,
Q=+13 debye.Å). Cette densité est obtenue à partir d’un modèle électrostatique ajusté sur la valeur expérimentale de l’énergie de liaison
E = 11,5 meV. Le lobe principal correspond à l’attraction dipolaire dans la direction du dipôle et le lobe secondaire à l’attraction quadripolaire re-
lativement moins importante. Les deux lobes sont séparés par un creux de probabilité de présence au voisinage de l’origine des coordonnées, où le
nuage électronique des électrons de valence de la molécule neutre repousse l’électron excédentaire.
Molécules et noyaux déformés
53

multipolaires et de valence sont rap-
pelées dans l’encadré 1).
Ces résultats expérimentaux sont
obtenus grâce au dispositif de jets
croisés représenté dans la figure 2.
Des atomes de xénon sont portés
préalablement dans des états métas-
tables par bombardement électroni-
que avant d’être excités sélective-
ment dans des états de Rydberg. Ce
jet d’atomes de xénon métastables et
le laser qui réalise leur excitation
fonctionnent en impulsion. Ils sont
synchronisés avec un jet supersoni-
que de molécules ou d’agrégats mo-
léculaires de façon à ce que les ato-
mes de Rydberg entrent en collision
avec les molécules ou agrégats étu-
diés. Après capture d’électron par ces
derniers (en régime de collision uni-
que), les anions créés sont accélérés
par un champ électrique pour être en-
suite détectés individuellement par
des galettes de microcanaux et triés
en masse selon leur temps de vol.
La valeur de l’énergie de liaison E
de l’électron en excès sur la molécule
peut être déduite de la variation en
fonction de n du taux de capture par le
système moléculaire de l’électron ex-
terne de l’atome excité dans un état de
Rydberg. Pour cela, on ajuste la me-
sure expérimentale avec les résultats
d’un modèle de cette dépendance en
n. Le calcul s’effectue en prenant en
compte les distributions de vitesse des
jets atomiques et moléculaires, en
connaissant l’état quantique de
l’atome excité et en utilisant les don-
nées de la littérature concernant le
système moléculaire accepteur (struc-
ture, dipôle, quadripôle, polarisabi-
lité,...). La molécule ou l’agrégat ac-
cepteur est alors décrit de façon semi-
empirique comme un ensemble de
charges électrostatiques en ne gardant
qu’un seul paramètre ajustable, la dis-
tance à partir de laquelle l’électron
capturé « ressent » la répulsion du
nuage électronique de la molécule à
laquelle il est lié.
Si l’on considère la formation d’un
ion de valence, l’orbitale de l’élec-
tron capturé est localisée dans une ré-
gion de très faible taille devant celle
de l’atome excité et on utilise alors
un modèle dit à électron « quasi li-
bre », déjà introduit par Fermi pour
décrire les collisions faisant interve-
nir des atomes très excités. Le cœur
ionique positif de l’atome excité ne
joue là qu’un rôle de spectateur et la
valeur de n n’est pas un paramètre
critique. Au contraire, dans la forma-
tion d’un ion multipolaire, les orbita-
les de l’électron, avant et après cap-
ture, sont de dimensions comparables
et le modèle d’interaction électron-
molécule localisée précédent ne s’ap-
plique plus. On utilise alors un mo-
dèle collisionnel avec croisements
entre courbes de potentiel covalentes
(atome excité et système moléculaire
neutre) et ioniques (cœur de l’atome
excité et anion formé) semblables à
celles décrivant une molécule
ionique.
Pour chaque système étudié, l’al-
lure de la variation relative en fonc-
tion de n de son taux de capture
d’électrons provenant d’atomes exci-
tés renseigne immédiatement sur la
nature multipolaire ou de valence de
l’anion créé (figure 1). Accumulées
sur un grand nombre d’ions multi-
polaires (plus d’une trentaine) formés
à partir de molécules ou d’agrégats
possédant différents moments dipo-
laires ou quadripolaires, les valeurs
de l’énergie de liaison E déduites de
la confrontation au modèle ou bien
d’une autre méthode indépendante
qui sera décrite plus loin, se situent
dans le domaine thermique et sub-
Figure 1 - Evolution du taux de formation
d’anions formés par transfert d’électron entre
des atomes de Rydberg de nombre quantique
principal n et des molécules neutres d’adénine
(anions multipolaires) ou de SF
6
(anions de va-
lence). La courbe en trait plein est le résultat
d’un modèle simple d’échange de charge ajusté
sur les points expérimentaux discrets à l’aide du
seul paramètre qui est la valeur de l’énergie de
liaison de l’électron en excès E = 11,5 meV.
Figure 2 - Schéma de principe du montage expérimental des expériences de formation d’ions négatifs
par la méthode de transfert d’électrons de Rydberg. Les anions multipolaires formés peuvent être dé-
tachés par un champ électrique statique externe et une grille permet ensuite de ne détecter que les par-
ticules neutres.
54

thermique. Elles se trouvent être
directement reliées à la valeur opti-
male n
max
par une relation empirique
simple : E =23 eV/n
max
2,8
, relation qui
peut être justifiée approximativement
à l’aide du modèle ionique-covalent
évoqué ci-dessus.
En effectuant une sélection parmi la
grande quantité de molécules polaires
ou quadripolaires, principalement des
cétones, aldéhydes ou nitriles, il a été
possible de déterminer le moment
dipolaire et le moment quadripolaire
critiques nécessaires pour lier un élec-
tron (figure 3). Les valeurs expéri-
mentales obtenues sont µ
crit
≈2,5 D,
en très bon accord avec la prédiction
théorique de 1970 et avec les calculs
quantiques les plus récents, et
Q
crit
≈45 D.Å, qui constitue une va-
leur élevée pour des molécules usuel-
les. Quant aux ions qui seraient for-
més par un potentiel en 1/r
4
(interactions octopolaires ou de
polarisation), les moments critiques
attendus très grands rendent leur ob-
servation expérimentale encore
hypothétique.
UNE IONISATION NON PERTURBATRICE
ET RE
´VERSIBLE
L’énergie de liaison E de l’électron
en excès dans les anions multipolai-
res est très faible, typiquement com-
prise entre 10
–4
et 10
–1
eV. L’attache-
ment de cet électron perturbe très peu
les liaisons chimiques intramoléculai-
res (quelques eV) et même les faibles
liaisons intermoléculaires telles que
les liaisons hydrogène (quelques cen-
taines de meV) ou les interactions de
van der Waals (quelques dizaines de
meV).Autrement dit, on s’attend à ce
que la formation d’un anion multi-
polaire à partir d’une espèce neutre
(molécule ou agrégat moléculaire) ne
modifie ni sa structure, ni même ses
vibrations internes. Contrairement
aux procédés d’ionisation usuels (for-
mation d’ions positifs ou négatifs de
valence) qui provoquent toujours une
réorganisation du système neutre ini-
tial, on dispose ici d’un procédé qui
permet d’apporter une charge à un
système moléculaire neutre sans le
dénaturer et qui, surtout, est aisément
réversible.
On peut s’en convaincre en effec-
tuant une seconde mesure de l’éner-
gie de liaison E, indépendamment de
celle obtenue à partir du comporte-
ment en n du taux de formation. Dans
un champ électrique statique externe
de grandeur raisonnable (typiquement
quelques kV/cm pour des valeurs de E
de quelques meV), l’électron en ex-
cès d’un ion multipolaire peut échap-
per à la faible attraction multipolaire
de l’espèce moléculaire neutre. Au-
delà d’un champ critique, l’électron se
détache en traversant par effet tunnel
la barrière de potentiel formée par la
superposition du potentiel moléculaire
et du potentiel électrique externe (fi-
gure 4). Une modélisation simple de
ce processus permet là aussi, en ne se
servant que du seul paramètre ajusta-
ble évoqué précédemment, de déter-
miner la valeur de E à partir des ré-
sultats expérimentaux. Les valeurs de
E ainsi obtenues lors du processus de
détachement sont, dans la grande ma-
jorité des cas étudiés, très proches de
celles mesurées au moment du pro-
cessus d’attachement par transfert
d’électron de Rydberg.
D’autres expériences de spectro-
scopie de photo-électrons, menées en
particulier à l’Université John Hop-
kins de Baltimore, ont également
montré que la structure électronique
et nucléaire n’était pratiquement pas
affectée lors de l’ionisation multi-
polaire. De récents calculs, en parti-
culier ceux de notre groupe et ceux
du Laboratoire de Chimie quantique
de l’Université d’Arizona, ne font
aussi apparaître que de très faibles
perturbations de la géométrie ou de
l’état électronique des espèces neu-
tres, ce qui est remarquable lorsqu’il
s’agit de l’ionisation d’agrégats mo-
léculaires dont les énergies de liaison
intermoléculaires sont faibles.
LA SPECTROME
´TRIE DE MASSE DE
SYSTE
`MES MOLE
´CULAIRES NEUTRES
L’étude des interactions entre mo-
lécules au sein des liquides ou bien
entre molécules biologiques (liaisons
hydrogène ou liaisons de van der
Waals) s’est considérablement déve-
loppée au cours des dernières années
grâce aux jets supersoniques qui per-
mettent de créer des assemblées
(agrégats) de molécules faiblement
Figure 3 - Energie de liaison de l’électron en ex-
cès dans des ions dipolaires ou quadripolaires, en
fonction des moments dipolaires ou quadripolai-
res pour plusieurs espèces moléculaires neutres
étudiées ; carrés et ronds noirs : valeurs expéri-
mentales, carrés et ronds blancs : valeurs calcu-
lées maximales pour des ions qui n’ont pu être ob-
servés. Les courbes illustrent les résultats de la
modélisation électrostatique semi-empirique de
ces anions multipolaires. La courbe en pointillés
et les courbes en traits pleins correspondent
respectivement aux molécules polaires
(µcrit ≈2,5 D) et aux molécules acceptrices à
moment quadripolaire positif (Qcrit ≈+45 D.Å)
ou négatif (Qcrit ≈−52 D.Å).
Figure 4 - Fraction d’anions dipolaires de la
molécule d’adénine détachés lors du passage de
ces ions à travers une courte zone de champ
électrique statique. La courbe en trait plein est le
résultat d’un modèle de détachement par effet
tunnel de l’électron en excès qui est ajusté sur
les points expérimentaux à l’aide du seul para-
mètre qui est la valeur de l’énergie de liaison de
cet électron E égale à 11,5 meV.
Molécules et noyaux déformés
55

liées. Au sein d’un jet d’agrégats, on
ne trouve pas une taille bien définie
mais une distribution en masse assez
large. Même si l’on dispose de lasers
finement accordables dans le do-
maine d’absorption des molécules
étudiées, il est souvent très difficile
de distinguer par des méthodes
spectroscopiques à quelle structure
moléculaire on a affaire. S’il s’agit de
molécules polaires, la formation
d’ions dipolaires permet d’ioniser, de
façon non perturbante et réversible,
tous les agrégats dont le moment
dipolaire total, somme géométrique
des dipôles moléculaires constituants,
est supérieur à la valeur critique
µ
crit
≈2,5 D. Après une accélération
par un premier champ électrique suf-
fisamment faible pour ne pas les dé-
tacher, les anions formés sont triés
par temps de vol, ce qui permet d’en
effectuer la sélection en masse. Dans
un second temps, on détache l’élec-
tron en excès des anions grâce à un
second champ électrique statique suf-
fisant pour finalement retrouver
l’agrégat neutre initial après l’avoir
sélectionné en masse. Nous pouvons
donner deux exemples caractéristi-
ques : les petits agrégats homogènes
de molécules d’eau (dipôle molécu-
laire 1,85 D <µ
crit
) ou d’acétonitrile
(dipôle moléculaire 3,92 D >µ
crit
).
Chaque fois que les calculs théori-
ques et les résultats expérimentaux
concernant la structure de l’eau ou
l’acétonitrile en phase liquide pré-
voyaient que les structures d’équili-
bre de ces agrégats devaient posséder
un moment dipolaire total supérieur à
la valeur critique, nous avons bien
observé la formation d’ions dipolai-
res, et seulement dans ces cas-là.
Le cas du dimère mixte eau-
acétonitrile, qui possède deux confi-
gurations géométriques (isomères)
énergétiquement voisines mais de
moments dipolaires totaux différents,
nous permet de montrer que l’on peut
faire encore mieux (voir encadré 2).
L’énergie de liaison E de l’électron
attaché dépend en effet beaucoup du
moment dipolaire total. Pour chaque
valeur du moment résultant, il existe
donc, en première approximation,
une valeur optimale n
max
du nombre
quantique n des atomes de Rydberg
qui conduit à l’observation de l’anion
dipolaire correspondant. Avec le laser
accordable créant les atomes de Ryd-
berg, on sélectionne l’isomère désiré
en favorisant ou non le transfert
d’électron vers telle ou telle configu-
ration géométrique. La sélection
peut être effectuée également en
Encadré 2
SÉLECTION D’ISOMÈRES NEUTRES D’AGRÉGATS
MOLÉCULAIRES POLAIRES
Le cas illustré ici est celui du dimère acétonitrile-eau. Les
calculs de chimie quantique, effectués dans le groupe de
P. Millié au CEA Saclay, prévoyaient deux isomères
géométriques de même énergie de liaison intermoléculaire
(180 meV) mais de moments dipolaires permanents totaux très
différents. L’un de grand moment dipolaire (5,5 debye) et
l’autre de moment dipolaire juste supérieur au dipôle critique
(2,6 debye). L’énergie de liaison E de l’électron en excès dans
un ion dipolaire dépendant fortement du moment dipolaire
total de l’espèce neutre qui l’attache, on s’attendait donc à
observer deux types d’anions dipolaires bien distincts et à
mesurer deux valeurs de E bien différentes. La figure montre
que c’est bien le cas en ce qui concerne l’évolution du taux de
formation d’anions en fonction du nombre quantique principal
de l’électron de Rydberg transféré. La modélisation de chacun
des deux pics observés à l’aide du seul paramètre ajustable
qu’est l’énergie de liaison E donne E = 35 meV pour le pic à
nmax =10 −11, qui est naturellement attribué à l’isomère de
grand moment dipolaire, et E = 2 meV pour le pic moins
marqué à nmax ≈28, qui correspond à l’isomère de faible
moment dipolaire. Les expériences de détachement par champ
électrique externe confirment totalement ces deux valeurs. A
l’issue de la zone de détachement, on obtient donc un jet de
dimères neutres, sélectionnés à la fois en masse et en isomère,
en changeant le niveau de Rydberg impliqué dans le processus
de transfert d’électron.
Figure - Evolution du taux de formation d’anions dipolaires formés par
transfert d’électron entre des atomes de Rydberg de nombre quantique
principal n et des dimères neutres acétonitrile-eau.
56
 6
6
 7
7
1
/
7
100%