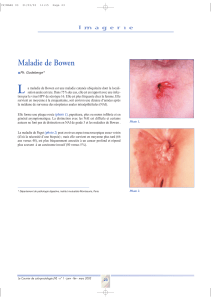
Les vibrations d`une molécule de sel

42
Grâce au développement des
lasers à impulsion femtose-
conde, on suit en temps réel
les mouvements des atomes à l’inté-
rieur d’une molécule. Un premier
laser excite le système, c’est-à-dire
qu’il crée le mouvement de vibration
des atomes. Un second laser ultra-
bref sonde le système à différents
retards. La succession de ces mesu-
res pompe-sonde constitue le film du
mouvement moléculaire. A l’aide de
ces méthodes, les molécules sont
observées pendant qu’elles réagis-
sent ou qu’elles se fragmentent, et les
potentiels moléculaires peuvent être
déterminés.
Lorsque l’on connaît la dyna-
mique de vibration d’une molécule,
on utilise cette molécule comme
sonde de la structure d’un agrégat
moléculaire. Ces petits agrégats sont
des systèmes composés de quelques
molécules seulement. Ils permettent
d’étudier un phénomène physique
ou chimique au niveau élémentaire,
sans perturbation par le milieu envi-
ronnant. La dynamique d’une molé-
cule est modifiée d’une façon qui
dépend de l’arrangement de cet
agrégat. En retour, cela fournit des
informations sur la nature même de
l’agrégat.
Cette méthode est appliquée ici au
cas de la molécule d’iodure de
sodium (sel NaI) dont la dynamique
est bien établie, et à ses agrégats
avec différentes molécules polaires.
On découvre ainsi qu’une molécule
de sel ne se dissout pas facilement
dans une nano-gouttelette d’eau à
basse température.
IONISATION D’UN PAQUET
D’ONDE MOLÉCULAIRE
Le mouvement des atomes dans
l’espace est un phénomène où la des-
cription classique est en général une
bonne approximation. En revanche,
dès que l’on cherche à les confiner en
contrôlant leur quantité de mouve-
ment, le comportement des atomes
devient quantique en vertu du prin-
cipe d’incertitude d’Heisenberg.
Dans une molécule au sein de
laquelle les atomes sont confinés par
la liaison chimique, l’énergie de
vibration des noyaux est quantifiée.
C’est donc dans un cadre quantique
que les vibrations moléculaires sont
étudiées par la spectroscopie.
Lorsque les états électroniques
fondamental et excité d’une molé-
cule ont des distances d’équilibre
très différentes, on peut préparer un
paquet d’onde avec un laser ultra-
rapide et considérer son évolution
temporelle dans le potentiel inter-
atomique. Classiquement, on dit
que si l’impulsion lumineuse est
beaucoup plus courte que le temps
caractéristique d’une vibration
moléculaire, on porte « instantané-
ment » la molécule dans un état
excité, c’est-à-dire en gardant la dis-
tance entre les atomes identique à
celle qu’elle était dans l’état fonda-
mental à l’instant t=0de l’excita-
tion.
Une expérience d’observation de
mouvements moléculaires se déroule
en deux temps qui justifient l’appella-
tion d’expérience pompe-sonde. Une
première impulsion laser (la pompe)
prépare le système dans l’état excité.
Cette opération définit l’origine du
temps de l’expérience. C’est elle qui
déclenche le chronomètre (encadré
1). Une seconde impulsion (la sonde)
« photographie » le système à diffé-
rents instants ultérieurs. Il existe plu-
sieurs manières de faire cette
« photo », l’ionisation étant la plus
efficace et universelle. C’est ce pro-
cessus d’ionisation de paquets d’onde
que nous allons décrire maintenant
pour le cas de NaI.
IONISATION FEMTOSECONDE DE NaI
La molécule de NaI est l’un des
plus beaux exemples permettant de
suivre l’évolution du paquet d’onde.
Les travaux de A.H. Zewail, qui a
obtenu le prix Nobel de chimie en
1999, ont montré que l’on accède à
l’évolution de ces paquets d’onde
par des techniques de fluorescence
induite par laser.
Dans la molécule isolée, l’état
fondamental Xpossède une structure
de paire d’ions en contact Na+I–
(NaI est un sel), alors que le premier
état électronique excité Aprésente
une structure neutre qui correspond
à l’interaction entre les atomes de
sodium et d’iode dans leur état fon-
damental (encadré 2). L’excitation de
Molécules et agrégats
Les vibrations
d’une molécule de sel
Lorsqu’une molécule vibre, la distance entre les atomes change rapidement. Ce mouvement est suivi
en temps réel à l’aide de lasers femtoseconde. On détermine ainsi s’il existe des distances privilé-
giées pour lesquelles l’électron de la liaison chimique est plus efficacement arraché lors du processus
d’ionisation. Le changement de la dynamique dans un agrégat par rapport à celle de la molécule
isolée renseigne sur la structure de l’agrégat. Ainsi, une molécule de sel se « dissout » dans un
agrégat d’une dizaine de molécules d’ammoniac, alors qu’elle reste à la surface d’un agrégat d’eau.
– Laboratoire de photophysique molécu-
laire, UPR 3361 CNRS, université Paris
Sud, 91405 Orsay cedex.

43
Molécules et agrégats
la molécule par absorption d’un pho-
ton pompe correspond au transfert de
l’électron de I –vers Na +.
Dans ces expériences, un premier
photon prépare un paquet d’onde
dans l’état excité A(figure 1, flèche
de Xvers A), à la distance d’équilibre
de l’état fondamental (2,7 Å). Les
deux atomes Na et I, tous deux
neutres, ressentent alors une force
fortement répulsive : le paquet d’on-
de évolue rapidement vers les
grandes distances internucléaires. Au
point de croisement entre la courbe
neutre et la courbe ionique Na+–I
–
(7 Å), il y a dans 90 % des cas un
transfert d’électron entre Na et I, le
Encadré 1
SCHÉMA EXPÉRIMENTAL
Grâce à un jet supersonique, on prépare des molécules de NaI
en phase vapeur ou des agrégats qui contiennent une molécu-
le de NaI et des molécules de solvant. Pour augmenter la
taille moyenne des agrégats, on accroît la pression de vapeur
saturante des molécules de solvant, soit en chauffant, soit en
augmentant la concentration du mélange He/solvant. Le flux
d’hélium sert à refroidir les agrégats et à les entraîner entre
les plaques d’un spectromètre d’électron et d’ion.
Les molécules y sont excitées et ionisées par les impulsions
laser (figure 1). Les ions ainsi obtenus sont accélérés par un
champ électrique, puis volent dans une zone libre de champ
et sont enfin détectés. En mesurant le temps qui sépare l’im-
pulsion lumineuse de l’arrivée sur le détecteur, on détermine
la masse de l’ion puisque le temps de vol est proportionnel
à la racine carrée de la masse.
Dans les expériences femtoseconde, le retard entre l’impulsion
de pompe et celle de sonde change selon le chemin optique
relatif des faisceaux laser à raison de 6,7 ps par mm de dépla-
cement de la ligne à retard optique.
Le principe d’une mesure pompe-sonde est illustré sur la
figure 2 : une première impulsion laser, la pompe (flèche
bleue), porte la molécule à l’état excité et définit le temps 0 de
l’expérience. Cette impulsion pompe crée un paquet d’onde
sur le mur répulsif du potentiel de l’état excité (à gauche). Il
est repoussé vers les grandes distances internucléaires jusqu’à
ce qu’il heurte le mur de potentiel de droite et rebrousse che-
min. Le paquet d’onde oscille ainsi dans le puits de l’état
excité avec une période T. Pour caractériser ce mouvement,
on envoie une seconde impulsion laser, la sonde (flèche vio-
lette), avec un retard variable entre la pompe et la sonde. A
t=0, le photon sonde peut ioniser la molécule (flèche t0) et
on observe un signal d’ion, de même qu’au temps t1. En
revanche, quand le paquet d’onde s’éloigne vers t2, on ne
peut plus atteindre la courbe de l’ion, et le signal d’ion
revient à zéro pour croître à nouveau quand le paquet d’onde
revient dans la partie gauche du potentiel, autour du temps
t=T(figure 2 en bas). Les oscillations du paquet d’onde
dans l’état excité se reflètent dans le signal d’ion.
L’une des difficultés de cette expérience consiste à mesurer le
temps t=0où les impulsions laser arrivent en même temps
à l’intersection du jet et du spectromètre. Pour y parvenir, on
ajoute une molécule aromatique (de type benzène) dans le jet.
Cette molécule n’est ionisée et détectée que si l’impulsion
pompe à 266 nm arrive avant l’impulsion sonde à 310 nm. En
changeant continûment le retard entre les deux impulsions, le
signal décrit une fonction de Heaviside (dite « en marche
d’escalier ». Le saut de la marche donne le temps t=0et sa
largeur la somme des largeurs temporelles des deux impul-
sions.
Figure 2 - Principe d’une mesure pompe-sonde.
Figure 1 - Vue simplifiée du dispositif expérimental.

44
couple Na+I–se forme (encadré 2).
Après ce transfert, l’essentiel du
paquet d’onde poursuit son chemin
sur la courbe ionique jusqu’à 12 Å
où il fait demi-tour (figure 1). Au
point de croisement, il y a de nou-
veau transfert d’électron et le sys-
tème parcourt la courbe de potentiel
de l’état neutre jusqu’à sa position
initiale (2,7 Å) puis repart. A chaque
passage au point de croisement, une
petite partie du paquet d’onde
(10 %) ne subit pas de transfert
d’électron, s’échappe et conduit à la
dissociation de NaI en deux atomes
neutres, sodium et iode. Le paquet
d’onde oscille ainsi entre 2,7 et 12 Å,
avec une atténuation progressive
d’intensité due à la fuite au point de
croisement.
Pour observer le mouvement du
paquet d’onde, un deuxième laser
décalé temporellement le sonde par
absorption d’un photon. Pour engen-
drer des oscillations temporelles, il
faut que cette absorption ne se pro-
duise que pour une distance internu-
cléaire donnée.
Dans les expériences de A.H.
Zewail, l’évolution du paquet d’onde
est caractérisée par fluorescence
induite par laser. Le laser sonde
porte le système dans un état excité
(par exemple l’état Bcorrespondant
au premier état excité de l’atome de
sodium) et la lumière qui résulte de
la désexcitation est recueillie. Dans
ce cas, la sélectivité en fonction de la
Encadré 2
LA MOLÉCULE DE NaI
Les molécules de sel sont caractérisées par des liaisons
ioniques, par contraste avec des liaisons covalentes. Dans ces
dernières, des électrons sont mis en commun pour former une
liaison chimique. En revanche, dans une liaison ionique, un
ou plusieurs électrons sont échangés entre les atomes qui sont
alors liés par une force électrostatique de Coulomb en 1/R (où
R est la distance entre les atomes). Les molécules de sel les
plus simples contiennent deux atomes, un halogène (F,Cl, I...)
et un alcalin (Li, Na, K…). L’atome alcalin, qui a un potentiel
d’ionisation très bas, donne un électron à l’atome d’halogène
pour former, par exemple, Na+Cl–qui est notre sel de cuisine.
Les courbes de potentiel de la molécule de NaI (variation de
l’énergie potentielle entre les atomes en fonction de R) sont
représentées sur la figure ci-contre.
– L’état fondamental de la molécule d’iodure de sodium (NaI)
est de nature ionique. L’atome de sodium donne un électron à
l’atome d’iode et forme une paire d’ions Na+I–. Le potentiel
est répulsif à courte distance et coulombien en 1/R à distance
supérieure à ≈3 Å.
– Le premier état excité correspond à une interaction entre les
atomes neutres Na et I dans leur état fondamental. Comme il
n’y a pas de liaison chimique entre Na et I à la distance
d’équilibre de l’état fondamental, les deux atomes subissent
une force répulsive. Dès que la distance est supérieure à
≈4 Å, l’interaction entre ces deux atomes est très faible. Il en
résulte une courbe essentiellement plate en fonction de R et la
molécule devrait se dissocier rapidement à l’état excité. A une
distance de 7 Å, la courbe de l’état fondamental croise celle
du premier état excité. Comme ces deux états ont la même
symétrie, ils sont faiblement couplés. Or, en mécanique quan-
tique, lorsque deux états couplés ont la même énergie, ils se
repoussent. Le potentiel auquel sont soumis les atomes est
alors représenté par la courbe mixte (en gras sur la figure).
Il présente un vaste puits de potentiel au fond très plat. Du
fait de ce croisement, la molécule est piégée dans ce puits,
avec toutefois un petite probabilité de se dissocier.
– Les états plus excités (B,C) correspondent à des états excités
de l’atome de sodium en interaction avec l’atome d’iode dans
son état fondamental. Ce sont des états peu liés, essentielle-
ment neutres mais faiblement couplés aux états ioniques.
– Enfin, dans l’ion NaI+, un électron est arraché à l’atome de
sodium. L’énergie de liaison est due principalement à une
interaction charge/dipôle induit. Elle est faible et diminue
rapidement avec R.
Figure - Courbes de potentiel de NaI.

45
Molécules et agrégats
distance internucléaire est assurée
par le principe qui suit. L’absorption
d’un photon ne change ni la position
des atomes ni leur énergie cinétique.
L’absorption n’a lieu que lorsque la
différence d’énergie entre les
courbes de potentiel de l’état initial
(A) et de l’état final (B) est égale à
l’énergie du photon : c’est une
condition de résonance.
en l’ionisant avec un photon à
266 nm (flèche en tiret, figure 1).
Cela indique que le processus d’io-
nisation se produit bien pour une
distance internucléaire fixée. Dans
ce cas, nous détectons deux ions par
spectrométrie de masse à temps de
vol : NaI+et Na+issu de la dissocia-
tion de NaI+. Le maximum de signal
d’ion est observé après 0,6 ps. Le
paquet d’onde initialement localisé à
très courte distance (2,7 Å) évolue
jusqu’à 12 Å, puis fait demi-tour et,
avec la longueur d’onde de pompe
utilisée (310 nm), la période de
vibration est de 1,2 ps ; le maximum
de signal correspond donc à une
demi-période ; il est obtenu lorsque
la distance internucléaire est voisine
de 12 Å, au point de rebroussement
externe (figure 1 à droite).
Ce résultat s’explique en utilisant
des arguments de mécanique clas-
sique et des considérations sur la
nature de l’état électronique Adans
lequel évolue le paquet : à courte
distance, cet état est essentiellement
un état neutre Na – I (les deux
atomes sont dans leur état fonda-
mental) alors qu’à grande distance,
la nature de l’état est de type ionique
Na+– I–. Lors de l’ionisation à courte
distance, c’est un électron du sodium
qui est éjecté (l’énergie du photon
sonde ne permet pas d’ioniser
l’atome d’iode) alors qu’à grande
distance, c’est l’électron de l’anion
I–qui part (l’énergie du photon
sonde est suffisante pour arracher
l’électron de l’anion). Or, la section
efficace d’ionisation de l’anion I–est
200 fois plus grande que celle de
l’atome de sodium : on ionise le
paquet d’onde essentiellement lors-
qu’il est localisé sur la courbe de
potentiel à caractère ionique, soit
aux grandes distances internu-
cléaires. Une fois l’électron arraché
à I–, on obtient soit l’ion NaI+stable,
soit son produit de dissociation Na+.
Nous avions pensé « à tort » que
si l’on devait observer l’ion NaI+,on
devait le détecter en opposition de
phase (donc à courte distance) par
rapport à l’ion Na+issu de la disso-
ciation de NaI+. En effet, NaI+est
très stable à courte distance internu-
cléaire (0,5 eV), son énergie de liai-
son diminue lorsque la distance aug-
mente. Au voisinage du point de
rebroussement externe, soit à 12 Å,
l’ion NaI+n’est quasiment pas lié :
son énergie de liaison est alors de
0,003 eV. De plus, l’excès d’énergie
(énergie du photon moins l’énergie
nécessaire pour arracher l’électron)
apporté par les photons est de 0,3 eV,
donc très grand devant l’énergie de
liaison de NaI+à 12 Å. Et c’est pour-
tant à 12 Å qu’est observé l’ion
NaI+! Pourquoi ?
Comme l’électron est 2 000 fois
plus léger que le proton (et 200 000
fois plus que l’atome d’iode), son
éjection lors de l’ionisation ne
change quasiment pas l’énergie ciné-
tique des atomes (l’énergie commu-
niquée à I par l’électron éjecté de I–
est de l’ordre de 10–6 eV). Au point
2 4 6 8 10 12 14 16 18 20
-3
-2
-1
0
1
2
3
4
5
6
7
e
-
e
-
266 nm
Point de croisement
C
B
A
X
395 nm
310 nm
Na
+
+ I
-
Na(3s)+I
Na(4p)+I
Na(3p)+I
Na
+
+I
Énergie / eV
R(Na-I) / Angström
Figure 1 - Courbes de potentiel de la molécule
de NaI obtenues par des calculs de chimie quan-
tique. Le paquet d’onde formé par excitation de
NaI (flèche 310 nm) oscille dans l’état A issu
d’un croisement des courbes Na – – I et
Na+––I
–. A chaque passage au point de croi-
sement, une petite partie du paquet d’onde
s’échappe, menant à la formation de deux
atomes séparés Na et I. Le mouvement du
paquet d’onde est sondé par ionisation à un
photon (flèche en tirets 266 nm) ou par ionisa-
tion à deux photons par l’intermédiaire de l’état
C (flèches 395 nm). Après absorption du, ou
des, photon(s), un électron est émis.
L’ionisation à un photon a lieu autour du point
de rebroussement à 12 Å (voir texte).
Dans le cas de l’ionisation à deux photons, la
transition de A vers C n’a lieu que lorsque le
paquet d’onde est à 10 Å.
Dans notre cas, le photon sonde
ionise la molécule en portant directe-
ment le système dans un double
continuum d’ionisation et de disso-
ciation. Si l’on obtient facilement
des conditions de résonance entre
deux états neutres, cela paraît moins
évident lors de l’ionisation dans un
continuum de dissociation.
L’expérience qui est représentée
sur la figure 2 montre bien que l’on
observe la vibration de la molécule
-1 0 1 2 3
0
2
4Na+
Signal d’ion Na (V)
∆t (ps)
0.2
0.4
0.6
Signal d’ion NaI (V)
NaI
+
Figure 2 - Observation des oscillations du
paquet d’onde par ionisation à un photon de la
molécule NaI. En abscisse : retard en pico-
secondes entre l’impulsion pompe (310 nm) et
l’impulsion sonde (266 nm). En ordonnée :
signal d’ion. En bas, Na+, en haut, NaI+. Les
deux échelles sont dans la même unité et reflè-
tent l’abondance relative des deux ions. La
faible atténuation des oscillations successives
est due à la fuite du paquet d’onde au point de
croisement entre l’état fondamental ionique et
l’état excité covalent. Lorsque les impulsions
laser arrivent en même temps (t=0), l’ioni-
sation de (NaI)2formé en très faible quantité
lors de la vaporisation du sel NaI, donne un
signal à la masse de l’ion NaI+.

46
de rebroussement externe (12 Å), les
atomes sont immobiles l’un par rap-
port à l’autre, et le restent lors de
l’ionisation : c’est l’électron éjecté
qui emporte tout l’excès d’énergie et
la très faible interaction entre Na+et
I suffit à maintenir la stabilité de
l’ion NaI+.
En revanche, dès que l’énergie
cinétique des atomes, lors de leur
oscillation, est plus grande que
l’énergie potentielle qui les lie dans
l’ion, l’ion NaI+n’est pas stable et se
casse en Na++ I. Si l’on étudie clas-
siquement ce processus en résolvant
les équations du mouvement dans le
potentiel moléculaire, on calcule que
l’ion NaI+n’est formé que pendant
les 10 fs où le paquet d’onde est
localisé autour du point de rebrous-
sement externe, alors que Na+est
obtenu pendant 200 fs – soit lorsque
la distance Na-I est comprise entre
8 Å et 11,8 Å. Compte tenu de la lar-
geur temporelle des lasers (150 fs),
cette différence se traduit par une
différence de largeur temporelle des
oscillations suivant l’ion observé : la
figure 2 montre bien que la largeur
des pics de récurrences associés à
l’ion NaI+est plus étroite que celle
des pics associés à Na+.
IONISATION DU PAQUET D’ONDE
A DEUX PHOTONS
Bien souvent dans les expériences
de photoionisation femtoseconde en
phase gazeuse, le laser sonde n’a pas
une énergie suffisante (une longueur
d’onde assez courte) pour ioniser
directement le système (ce qui est le
cas des agrégats). C’est l’absorption
de plusieurs photons qui fournit suf-
fisamment d’énergie pour arracher
un électron. On fait implicitement
l’hypothèse que l’absorption de
deux photons d’une même impul-
sion laser est très rapide par rapport
à la dynamique des atomes. Nous
verrons que cette hypothèse n’est
pas forcément justifiée.
Lors d’une ionisation multiphoto-
nique résonante passant par un état
intermédiaire, l’aspect des oscilla-
tions est fortement dominé par la
condition de résonance du premier
photon sonde absorbé. Dans notre
cas, pour une longueur d’onde du
laser sonde de 395 nm comme indi-
qué sur la figure 1, le premier photon
de l’impulsion sonde est en réso-
nance lorsque la distance Na…I est
de 10 Å. Cette distance est parcou-
rue en 300 fs par le paquet d’onde.
Le processus d’ionisation est le sui-
vant : lorsque la distance est de
10 Å, un photon du laser sonde est
absorbé, portant le système dans
l’état excité Cqui correspond au
deuxième état excité du sodium
Na (4p). Une fois dans cet état, la
molécule absorbe un deuxième pho-
ton qui la porte dans le continuum
d’ionisation : l’électron est éjecté.
Les signaux obtenus en ionisant
avec un ou deux photons sont très dif-
férents alors que, dans les deux cas,
c’est la même dynamique du paquet
d’onde dans l’état Aqui est sondée
(figures 2 et 3) : avec la sonde à deux
photons, le signal d’ion est maximum
pour deux délais pompe-sonde dis-
tincts (pics verts et bleus) par période
d’oscillation (1,2 ps), alors que l’on
n’observe qu’un pic par période pour
la sonde à un photon.
Le premier pic (bleu) est observé
à 300 fs. Il correspond au premier
passage du paquet d’onde à la dis-
tance de 10 Å où la condition de
résonance vers l’état Cest réalisée
(le paquet d’onde va du point tour-
nant interne où il est préparé vers le
point de rebroussement externe). Le
deuxième pic (vert) correspond à
cette même condition de résonance,
lorsque le paquet d’onde revient du
point de rebroussement externe
(12 Å).
De plus, une asymétrie marquée
entre ces deux séries de pics appa-
raît. Les pics de récurrences sont
plus intenses lorsque le paquet
d’onde est rentrant (vert) que lors-
qu’il est sortant (bleu). On en déduit
que l’efficacité d’ionisation du
paquet d’onde dépend du sens de
propagation. L’évolution temporelle
du paquet d’onde dans l’état inter-
médiaire joue un rôle crucial.
L’interprétation de ce résultat a
priori surprenant utilise des argu-
ments de mécanique classique en
considérant que la section efficace
d’ionisation varie avec la distance
Na – I, car la nature de l’état électro-
nique excité Cchange avec la dis-
tance internucléaire. En particulier,
son faible caractère ionique (dû aux
couplages entre états neutres et
ioniques) augmente quand la distance
Figure 3 - Observation des oscillations du paquet d’onde dans l’état A de NaI par ionisation à deux
photons. Le photon pompe est à 310 nm et deux photons sonde (à 395 nm) sont utilisés. Les pics bleus
correspondent au paquet d’onde qui se déplace du point tournant interne (2,7 Å) vers le point tournant
externe (12 Å), la première oscillation est décalée de 300 fs. Les pics verts correspondent au paquet
d’onde qui se déplace dans l’autre sens. Les carrés noirs sont les points expérimentaux et la courbe en
rouge est la somme de tous les pics (bleus et verts).
 6
6
 7
7
1
/
7
100%