Couplage Coeur M1-UE8 2008-2009

Le Cœur en Tant que Pompe
Couplage des Cavités Cardiaques,
Couplage Cœur-Système Artériel
Année 2008-2009
Professeur Alain Nitenberg
SMBH Léonard de Vinci – Bobigny
Université Paris 13
Service de Physiologie et d’Explorations Fonctionnelles
CHU Jean Verdier - Bondy

Généralités

Volume
Volume
T
Té
él
lé
édiastolique
diastolique
Volume
Volume
T
Té
él
lé
édiastolique
diastolique
Diastasis
Diastasis
Volume
Volume
T
Té
él
lé
ésystolique
systolique
Volume
Volume
T
Té
él
lé
ésystolique
systolique
Le Cycle
Le Cycle
Cardiaque
Cardiaque
Contraction
Contraction
Isovolumique
Isovolumique
Systole
Systole
Auriculaire
Auriculaire
Éjection
Ventriculaire
Relaxation
Relaxation
Isovolumique
Isovolumique
Remplissage
Remplissage
Rapide
Rapide
L’activité du cœur est cyclique. Le cycle cardiaque est décomposé en plusieurs phases qui se
succèdent sans discontinuité. On distingue 6 phases:
le cycle cardiaque débute avec la systole auriculaire car les oreillettes sont les premières à
être activées à partir du nœud sinusal. Viennent ensuite:
la phase de contraction isovolumique,
la phase d’éjection,
la phase de relaxation isovolumique,
la phase de remplissage rapide,
la phase de diastasis ou remplissage lent qui précède la systole auriculaire suivante.
Ce sont ces phases qui vont être décrites.

Télédiastole Télésystole
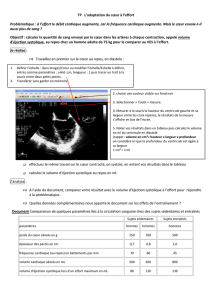
Ventriculographie Gauche
Ce schéma montre la forme du ventricule gauche en télédiastole et en télésystole. La cavité
est opacifiée par un liquide de contraste injecté dans le ventricule.

Volume
Télédiastolique
120 mL
80 mL/m
2
Volume
Télésystolique
50 mL
35 mL/m
2
Volume d' Éjection
Systolique
70 mL
45 mL/m
2
Fraction d'Éjection
60%
Chez un adulte normal au repos, les volumes caractéristiques du ventricule droit et du
ventricule gauche sont sensiblement identiques, même si la forme de ces 2 ventricules est
totalement différente. Le volume maximal du ventricule en fin de diastole (après la systole
auriculaire) est appelé volume télédiastolique. Ce volume est d’environ 120 mL. À la fin de
l’éjection ventriculaire, le volume ventriculaire appelé volume télésystolique est d’environ 50
mL, le ventricule n’est jamais vide de sang à la fin de l’éjection. La différence entre ces 2
volumes est le volume d’éjection systolique, c’est la quantité de sang qui a été injectée dans
le système artériel. Sa valeur est d’environ 70 mL. Le rapport volume d’éjection
systolique/volume télédiastolique s’appelle la fraction d’éjection, c’est la fraction du
volume télédiastolique qui a été injectée dans le système artériel. Sa valeur est d’environ
60%. Cette valeur est l’indice de performance ventriculaire le plus simple à déterminer, c’est
une grandeur sans dimensions, indépendante du poids et de la taille du sujet.
Afin de comparer des sujets de corpulences différentes, les volumes doivent normalisés
(divisés) par la surface corporelle du sujet qui dépend du poids et de la taille du sujet. On
obtient un index télédiastolique de 80 mL/m², un index télésystolique de 35 mL/m² et un
index systolique de 45 mL/m².
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
1
/
36
100%