Réseaux immunitaires - site de l`association GENS

RESEAUX IMMUNITAIRES
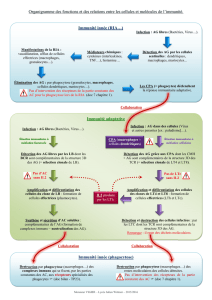
Pour comprendre le système immunitaire, il est nécessaire de connaître ses composantes tout en
sachant que le système agit comme un tout et qu'aucune composante n'agit de façon autonome. Dans
toute réponse immunitaire, les composantes agissent de concert, en tandem, ou en opposition,
comme p. ex. la capacité du système immunitaire d'éliminer les micro-organismes. Les micro-
organismes extracellulaires (la plupart des bactéries encapsulées) n'ont besoin que d'être phagocytés
pour être lysés. Cependant, les micro-organismes intracellulaires (p. ex. mycobactéries) sont
rapidement phagocytés, mais ne peuvent être lysés à moins que le macrophage ne reçoive un signal
d'activation.
La stratégie d'élimination des micro-organismes extracellulaires est donc dirigée vers la phagocytose,
qui est facilitée par l'opsonisation (couverture d'un micro-organisme par des Ac et/ou des composants
du complément). La plupart des phagocytes possédant des récepteurs pour la partie Fc des Ac du
complément, la présence de ces molécules sur une bactérie facilite son adhésion et sa phagocytose.
Cette réponse immunitaire « simple » nécessite une synthèse d'Ac efficace, l'activation de la cascade
du complément et un système phagocytaire intact. Les Ac sont produits par les cellules B ; toutefois,
les cellules B sont stimulées ou soumises à suppression par les cellules T. En outre, les cellules
phagocytaires sont recrutées par les facteurs chimiotactiques, dont certains sont produits par les
cellules T.
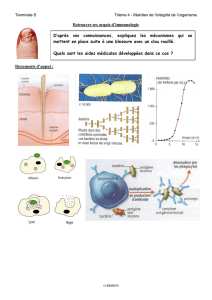
La stratégie d'élimination de certains micro-organismes intracellulaires qui infectent les phagocytes
implique une activation des cellules hôtes, qui deviennent alors « armées » et capables de tuer ces
micro-organismes de manière non-spécifique. L'activation des macrophages est au centre de la
réaction d'hypersensibilité de type retardé (HTR), et le test HTR cutané est un exemple excellent des
diverses cascades impliquées au niveau d'une réponse immunitaire. Le concept à la base du test HTR
cutané est qu'une injection intradermique d'un Ag auquel le patient a été auparavant exposé, produit
une induration locale dans les 48 h. Le réseau complexe impliqué au niveau d'une telle réponse est
illustré dans la FIG. 146-2.

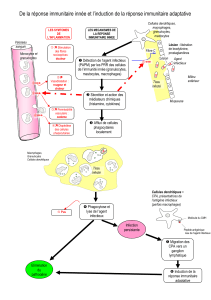
Au moment de l'injection, les cellules de Langerhans (CPA) de la peau captent l'Ag, le traitent et le
présentent (complexé avec le CMH de classe II) à une cellule CD4+ qui avait été précédemment
exposée à l'Ag (c.-à-d. qui a circulé en tant que cellule-mémoire de longue durée). Une fois que la
cellule CD4+ entre en contact avec le complexe CMH/Ag, elle exprime les récepteurs IL-2 et libère
plusieurs cytokines (p. ex. INFγ, IL-2 et des facteurs chimiotactiques, des lymphocytes et des
macrophages). L'INFγ- fait que les cellules endothéliales augmentent l'expression de leurs molécules
d'adhésion, facilitant ainsi le passage des lymphocytes et des macrophages à travers la barrière
endothéliale. L'IL-2 et l'INFγ- agissent également comme des signaux de prolifération/différenciation,
permettant aux clones des cellules T mémoire et aux nouvelles cellules T de se multiplier. Une fois
que les macrophages ont rejoint le lieu d'injection, ils sont empêchés de repartir par des facteurs
inhibiteurs de la migration (MIF) sécrétés par les cellules T activées. L'INFγ- et le GM-CSF, sécrétés
tous 2 par les cellules T, agissent alors comme des facteurs d'activation des macrophages (MAF). Les
macrophages sont à présent « armés » et peuvent tuer les organismes intracellulaires et n'importe
quelle cellule tumorale avoisinante.
Les macrophages activés sécrètent l'IL1 et le TNFα, qui stimulent la sécrétion d'INFγ- et de GM-CSF,
augmentent l'expression des molécules d'adhésion sur les cellules endothéliales et permettent à ces
cellules de sécréter le facteur tissulaire, qui déclenche la cascade de la coagulation, se terminant par
le caillot de fibrine. Simultanément, les lymphocytes activés sécrètent le facteur inducteur de
procoagulation des macrophages (MPIF), qui permet l'expression de l'activité procoagulante du
macrophage (MPCA) activé ; le MPIF active également la cascade de la coagulation qui aboutit au
caillot de fibrine. Le dépôt de fibrine est responsable du durcissement observé lors du test HTR de la
peau.

La voie de l'HTR est importante au niveau du processus d'élimination des micro-organismes qui
infectent les cellules phagocytaires. Certains micro-organismes (p. ex. les virus) peuvent infecter des
cellules qui ne possèdent pas cette machinerie lytique et celles-ci ne peuvent donc déclencher leur
propre mort par ce mécanisme intracellulaire. De tels agents pathogènes sont éliminés par les LTC.
En cas d'infection par un virus, les cellules expriment les Ag viraux sur leur surface dans le CMH. Le
complexe virusCMH stimule la production des LTC syngéniques qui tuent alors les cellules exprimant
ce complexe. Suivant l'association du produit viral avec la classe I ou II du CMH, le LTC appartiendra
aux sous-populations CD4 ou CD8 respectivement. Comme décrit plus haut, l'association avec l'une
des classes du CMH dépend de la voie utilisée pour apprêter l'Ag ; p. ex. la plupart des LTC générés
contre la rougeole et le virus Herpes simplex appartient à la sous-population CD4. Dans l'infection au
virus de la grippe, les LTC dirigés contre l'Ag nucléoprotéique sont des CD8, alors que ceux dirigés
contre l'Ag hémaglutininique sont des CD4.
1
/
3
100%