Sélénium et fonction thyroïdienne - iPubli

MINI-SYNTHÈSE
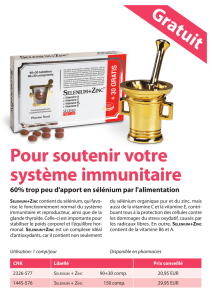
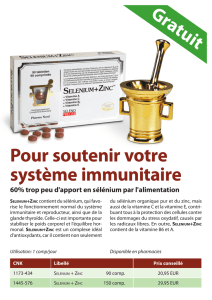
Sélénium et fonction thyroïdienne

m/ n° 10,

A
A
r
A
FA B]
n° 96
1
/
3
100%