Effets négatifs sur la sexualité des traitements

Progrès
en
urologie
(2015)
25,
115—127
Disponible
en
ligne
sur
ScienceDirect
www.sciencedirect.com
REVUE
DE
LA
LITTÉRATURE
Effets
négatifs
sur
la
sexualité
des
traitements
médicamenteux
des
symptômes
du
bas
appareil
urinaire
liés
a
l’hypertrophie
bénigne
de
la
prostate
Negative
effects
on
sexual
function
of
medications
for
the
treatment
of
lower
urinary
tract
symptoms
related
to
benign
prostatic
hyperplasia
A.
Descazeauda,∗,
A.
de
La
Tailleb,
F.
Giulianoc,
F.
Desgrandchampsd,
G.
Doridote
aService
de
chirurgie
urologique,
CHU
de
Limoges,
87042
Limoges
cedex,
France
bService
d’urologie,
faculté
de
médecine
de
Créteil,
groupe
hospitalier
Henri-Mondor,
94000
Créteil,
France
cService
de
médecine
physique
et
de
réadaptation,
faculté
des
sciences
de
la
santé,
université
de
Versailles
Saint-Quentin
en
Yvelines,
hôpital
Raymond-Poincaré,
92380
Garches,
France
dService
d’urologie
et
de
transplantation,
hôpital
Saint-Louis,
université
Paris
7,
institut
des
maladies
émergentes
et
des
thérapies
innovantes
(iMETI),
75010
Paris,
France
e24,
boulevard
Vital-Bouhot,
92521
Neuilly-Sur-Seine
cedex,
France
Rec¸u
le
21
juillet
2014
;
accepté
le
18
d´
ecembre
2014
Disponible
sur
Internet
le
17
janvier
2015
MOTS
CLÉS
Symptômes
du
bas
appareil
urinaire
;
Hypertrophie
bénigne
de
la
prostate
;
Alpha-bloquants
;
Résumé
But.
—
L’objectif
de
cette
revue
était
de
discuter
les
effets
négatifs
sur
la
sexualité
des
médi-
caments
des
symptômes
du
bas
appareil
urinaire
liés
à
l’hypertrophie
bénigne
de
la
prostate
(SBAU-HBP).
Matériel.
—
Une
revue
non
systématique
de
la
littérature
a
été
réalisée.
Elle
englobait
les
études
randomisées
des
sept
médicaments
concernés
et
les
résumés
des
caractéristiques
de
ces
produits.
Ce
travail
n’a
pas
pour
objectif
de
comparer
les
différents
médicaments.
∗Auteur
correspondant.
Adresse
e-mail
:
(A.
Descazeaud).
http://dx.doi.org/10.1016/j.purol.2014.12.003
1166-7087/©
2014
Elsevier
Masson
SAS.
Tous
droits
réservés.

116
A.
Descazeaud
et
al.
Inhibiteurs
de
la
5-alpha-reductase
;
Inhibiteurs
de
la
PDE5
;
Tadalafil
;
Dysfonction
érectile
;
Troubles
de
l’éjaculation
Résultats.
—
Seules
les
fréquences
maximales
rapportées
sont
présentées
dans
ce
résumé.
Avec
l’alfuzosine
LP,
elles
étaient
de
2,8
%
vs
1,3
%
avec
le
placebo
pour
la
dysfonction
érectile
(DE)
et
de
1
%
vs
0
%
pour
les
troubles
de
l’éjaculation
(TEj).
Avec
la
doxazosine,
l’incidence
était
de
5,8
%
vs
3,3
%
pour
la
DE,
3,6
%
vs
1,9
%
pour
la
baisse
de
la
libido
(BL)
et
0,4
%
vs
1,4
%
pour
les
TEj.
L’incidence
des
TEj
avec
la
tamsulosine
était
de
11
%
vs
<
1
%
pour
le
placebo,
et
pour
la
silodosine,
elle
était
de
28,1
%
vs
1,1
%.
Avec
le
finastéride
sur
12
mois,
la
fréquence
la
plus
élevée
était
de
9
%
vs
5
%
pour
la
DE,
4,4
%
vs
1,5
%
pour
les
TEj
et
6,4
%
vs
3,4
%
pour
la
BL.
À
24
mois,
pour
le
dutastéride,
les
fréquences
étaient
7,3
%
vs
4,0
%
pour
la
DE,
2,2
%
vs
0,8
%
pour
les
TEj
et
4,2
%
vs
2,1
%
pour
la
BL.
Aucun
effet
négatif
sur
l’éjaculation
ou
la
libido
n’a
été
rapporté
pour
le
tadalafil,
inhibiteur
de
la
PDE5
et
la
toltérodine,
anticholinergique.
Pour
les
extraits
de
plantes,
aucun
effet
indésirable
(EI)
sexuel
n’a
été
rapporté
parmi
les
EI
les
plus
fréquents.
Conclusion.
—
Les
médicaments
des
SBAU-HBP
peuvent
altérer
l’érection,
l’éjaculation
et
la
libido.
Une
meilleure
connaissance
des
effets
indésirables
de
chaque
médicament
pourrait
mieux
orienter
les
médecins
dans
la
prise
en
charge
des
hommes
ayant
des
SBAU-HBP.
©
2014
Elsevier
Masson
SAS.
Tous
droits
réservés.
KEYWORDS
Lower
urinary
tract
symptoms;
Benign
prostatic
hyperplasia;
5-alpha-reductase
inhibitors;
Alpha-blockers;
PDE5
inhibitors;
Tadalafil;
Erectile
dysfunction;
Ejaculatory
dysfunction
Summary
Purpose.
—
The
aim
of
this
review
is
to
discuss
the
negative
effects
on
sexual
function
of
medi-
cations
for
lower
urinary
tract
symptoms
secondary
to
benign
prostatic
hyperplasia
(LUTS-BPH).
Methods.
—
An
international
non-systematic
literature
review
was
performed.
It
included
ran-
domized
trials
of
seven
drugs
of
interest
and
the
summaries
of
the
characteristics
of
these
products.
This
work
did
not
aim
comparison
between
the
drugs.
Results.
—
Only
maximal
reported
frequencies
are
presented
in
this
abstract.
With
prolonged-
release
alfuzosin,
they
were
2.8%
vs.
1.3%
for
erectile
dysfunction,
compared
to
placebo
and
1%
vs.
0%
for
ejaculatory
dysfunction.
With
doxazosin,
the
incidence
was
5.8%
vs.
3.3%
for
erectile
dysfunction,
3.6%
vs.
1.9%
for
reduced
libido
and
0.4%
vs.
1.4%
for
ejaculatory
disorders.
The
incidence
of
ejaculatory
disorders
with
tamsulosin,
was
11%
vs.
<1%
with
the
placebo
and
with
silodosin,
it
was
28.1%
vs.
1.1%.
With
finasteride,
at
12
months,
the
highest
frequency
was
9%
vs.
5%
for
erectile
dysfunction,
4.4%
vs.
1.5%
for
ejaculatory
disorders
and
6.4%
vs.
3.4%
for
reduced
libido.
At
24
months,
for
dutatsteride,
frequencies
were
7.3%
vs.
4.0%
for
erectile
dysfunction,
2.2%
vs.
0.8%
for
ejaculatory
disorders
and
4.2%
vs.
2.1%
for
reduced
libido.
For
tadalafil,
a
phosphodiesterase-5
inhibitor,
and
tolerodine,
an
anticholinergic
drug,
no
negative
effect
on
ejaculation
or
libido
has
been
reported.
For
plant
extracts,
no
sexual
adverse
effects
(AEs)
were
reported
among
the
most
common
AEs.
Conclusion.
—
The
medications
for
LUTS-BPH
may
alter
erection,
ejaculation
or
libido.
A
greater
knowledge
of
the
adverse
effects
of
each
of
these
drugs
could
guide
physicians
in
the
clinical
management
of
men
with
BPH-LUTS.
©
2014
Elsevier
Masson
SAS.
All
rights
reserved.
Introduction
Les
symptômes
du
bas
appareil
urinaire
(SBAU)
reflètent
une
perturbation
de
la
production
d’urine,
de
son
stockage
dans
la
vessie
ou
de
son
évacuation
via
l’urètre
et
le
méat.
Ils
se
divisent
en
symptômes
de
la
phase
de
remplissage
(augmen-
tation
de
la
fréquence
des
mictions
avec
ou
sans
urgenturie),
symptômes
de
la
phase
mictionnelle
(gène
à
l’évacuation
de
l’urine)
et
symptômes
de
la
phase
post-mictionnelle
(sensation
de
vidange
incomplète
et
gouttes
retardataires)
[1].
L’hypertrophie
bénigne
de
la
prostate
(HBP)
représente
l’étiologie
la
plus
fréquente
des
SBAU.
La
sexualité
masculine
est
segmentée
en
libido
(désir),
érection,
éjaculation
et
orgasme.
Diverses
études
épi-
démiologiques
ont
montré
la
coexistence
de
SBAU-HBP
et
de
dysfonction
sexuelle
chez
l’homme
vieillissant
[2].
L’enquête
MSAM-7
a
mis
en
évidence
un
lien
fort
entre
les
troubles
sexuels,
l’âge
et
la
sévérité
des
SBAU
[3].
Chez
ces
patients,
les
troubles
de
l’éjaculation
sont
aussi
fré-
quents
que
la
dysfonction
érectile
[3—5].
Le
fondement
de
la
relation
entre
dysfonction
érectile
et
SBAU
n’est
pas
encore
élucidé
mais
ce
lien
serait
dû
à
des
mécanismes
physiopathologiques
communs,
mis
en
évidence
par
des
études
précliniques.
Ces
mécanismes
passeraient
par
des
dérèglements
de
la
voie
NO-cGMP,
de
la
voie
Rho-kinase

Effets
négatifs
des
médicaments
de
l’HBP
sur
la
sexualité
117
et
du
système
nerveux
autonome.
Toutes
ces
anomalies
auraient
comme
point
de
départ
une
athérosclérose
pel-
vienne
[2].
De
plus,
il
est
admis
depuis
des
décennies
que
certains
traitements
chirurgicaux
ou
pharmacologiques
de
l’HBP
peuvent
avoir
un
impact
négatif
sur
la
sexualité
[6,7].
Un
médicament
de
la
classe
des
inhibiteurs
de
la
phosphodiestérase-5,
indiqué
par
ailleurs
dans
le
traitement
de
la
dysfonction
érectile,
a
été
récemment
introduit
dans
l’arsenal
thérapeutique
de
l’HBP
[1].
Cette
revue
discute
les
effets
négatifs
sur
la
sexua-
lité
des
traitements
pharmacologiques
des
SBAU-HBP
en
se
basant
sur
les
données
des
études
cliniques
randomisées
publiées.
Les
classes
thérapeutiques
et
molécules
considé-
rées
dans
cette
revue
sont
les
alpha-bloquants
alfuzosine,
doxazosine,
tamsulosine
et
silodosine,
les
inhibiteurs
de
la
5-alpha-réductase
finastéride
et
dutastéride,
l’inhibiteur
de
la
phosphodiestérase-5
tadalafil,
l’anticholinergique
tolté-
rodine,
et
les
extraits
de
plante
Serenoa
repens
et
Pygeum
africanum.
Méthodologie
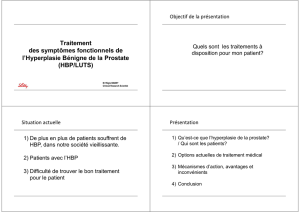
Une
recherche
non
systématique
de
la
littérature
interna-
tionale
a
été
réalisée
en
septembre
2013
à
partir
de
la
base
de
données
Medline
(National
Library
of
Medicine,
États-
Unis)
(Fig.
1).
Les
études
cliniques
randomisées,
rapportant
les
résultats
de
médicaments
approuvés
par
les
autorités
de
santé
ou
recommandés
par
les
sociétés
savantes
dans
la
prise
en
charge
des
SBAU
associés
à
une
HBP,
publiées
ces
23
dernières
années
(1991
à
2013),
ont
été
sélectionnées
selon
les
avis
des
auteurs.
Les
informations
sur
les
événe-
ments
indésirables
sexuels
ont
été
extraites
et
présentées
selon
leur
pertinence
du
point
de
vue
des
auteurs.
Les
mots
clés
en
anglais
utilisés
pour
la
recherche
principale
étaient
:
alfuzosin,
doxazosin,
tamsulosin,
silodosine,
toltérodine,
finasteride,
dutasteride,
tadalafil,
Serenoa
repens,
Pygeum
africanum,
benign
prostatic
hyperplasia,
sexual
dysfunc-
tion,
erectile
dysfunction,
ejaculatory
dysfunction.
Au
total,
34
études
ou
analyses
groupées
ont
été
rete-
nues,
9
portant
sur
l’alfuzosine,
5
sur
la
tamsulosine,
11
sur
le
finastéride,
4
sur
le
tadalafil,
4
sur
la
doxazosine,
4
sur
le
dutastéride,
3
sur
la
silodosine
et
1
sur
la
toltérodine.
Huit
études
ou
analyses
groupées
ont
été
exclues
:
1
portant
sur
l’alfuzosine
(<
12
semaines),
1
sur
la
doxazosine
(ana-
lyse
groupée
d’études
à
méthodologie
différente),
1
sur
la
tamsulosine
(analyse
groupée
d’études
à
méthodologie
différente),
2
sur
le
finastéride
(1
avec
des
résultats
sur
un
sous-groupe,
1
analyse
groupée
d’études
à
méthodolo-
gie
peu
précise),
1
sur
le
dutastéride
(patients
autorisés
à
prendre
la
tamsulosine)
et
2
sur
le
tadalafil
(1
étude
d’escalade
de
dose
et
1
étude
urodynamique).
Pour
Serenoa
repens
et
Pygeum
africanum,
seules
les
méta-analyses
les
plus
récentes
de
la
Cochrane
Database
of
Systematic
Reviews
ont
été
consultées.
De
plus
le
résumé
des
caractéristiques
du
produit
(RCP)
[8]
de
chaque
médicament
a
été
récupéré
du
répertoire
des
médicaments
de
l’agence
nationale
de
sécurité
du
médicament
et
des
produits
de
santé
(ANSM)
ou
de
l’agence
européenne
des
médicaments
(EMA).
Compte
tenu
de
la
méthodologie
adoptée,
ce
travail
ne
permet
de
comparaison
entre
les
différentes
molécules.
Présentation
de
la
littérature
Les
alpha-bloquants
L’alfuzosine
a
obtenu
son
autorisation
de
mise
sur
le
marché
(AMM)
le
12
novembre
1987.
Plusieurs
formulations
ont
été
développées.
L’alfuzosine
à
libération
prolongée
est
recom-
mandée
à
la
posologie
de
10
mg
en
une
prise
quotidienne.
Avec
l’alfuzosine
standard
(2,5
mg),
3
prises
par
jour
[9—11]
et
l’alfuzosine
à
libération
soutenue
(5
mg),
2
prises
par
jour
[12],
la
fréquence
des
troubles
sexuels
était
simi-
laire
à
celle
rapportée
avec
le
placebo.
Dans
les
études
évaluant
l’alfuzosine
à
libération
prolongée
(10
mg)
en
une
prise
quotidienne
pendant
3
mois
[11,13,14],
la
fréquence
de
la
dysfonction
érectile
variait
de
0
%
à
2,8
%
vs
0
à
1,1
%
avec
le
placebo
et
celle
des
troubles
de
l’éjaculation
de
0
à
1
%
vs
0
%.
L’analyse
groupée
de
ces
3
études
[15]
trou-
vait
une
fréquence
de
1,5
%
(vs
0,6
%)
pour
la
dysfonction
érectile
et
de
0,6
%
pour
les
troubles
de
l’éjaculation.
Dans
une
étude
menée
sur
2
ans
chez
1522
patients,
la
dysfonction
érectile
a
été
rapportée
chez
1,8
%
et
2
%
des
patients
traités
par
l’alfuzosine
et
le
placebo
respectivement.
Les
troubles
de
l’éjaculation
n’ont
été
rapportés
qu’avec
l’alfuzosine
et
étaient
de
0,4
%
[16]
(Tableau
1).
Dans
le
RCP,
seul
le
priapisme
avec
une
fréquence
indéterminée
est
mentionné
dans
les
affections
des
organes
de
reproduction
et
du
sein
(Tableau
2
:
RCP
de
l’alfuzosine).
La
doxazosine
a
obtenu
son
AMM
le
3
août
1999.
La
poso-
logie
recommandée
est
de
4
à
8
mg
en
une
prise
quotidienne.
Aucun
EI
sexuel
n’a
été
rapporté
dans
les
premières
études
avec
la
doxazosine
à
libération
prolongée
[17,18].
Dans
les
études
menées
sur
1
et
5
ans
comparant
la
doxazosine
et
un
inhibiteur
de
la
5-alpha-réductase
en
monothérapie
et
en
association
[19,20],
les
fréquences
de
la
dysfonction
érectile,
de
la
baisse
de
la
libido
et
des
troubles
de
l’éjaculation
avec
la
doxazosine
étaient
similaires
à
celles
sous
placebo
(Tableau
1).
Dans
le
RCP
de
la
doxa-
zosine,
la
dysfonction
érectile
est
rapportée
comme
peu
fréquente,
le
priapisme
comme
très
rare
et
l’éjaculation
rétrograde
avec
une
fréquence
inconnue
(Tableau
2
:
RCP
de
la
doxazosine).
La
tamsulosine
a
obtenu
son
AMM
le
20
décembre1995.
La
posologie
recommandée
est
de
0,4
mg
en
une
prise
quo-
tidienne.
Dans
les
études
randomisées
de
la
tamsulosine,
l’incidence
des
troubles
de
l’éjaculation
était
significati-
vement
plus
élevée
par
comparaison
au
placebo
aussi
bien
dans
les
études
de
courte
durée
[21,22]
qu’au
cours
d’une
extension
à
1
an
[23].
Les
troubles
de
l’éjaculation
ont
été
décrits
comme
éjaculation
rétrograde,
réduction
de
volume
de
l’éjaculât
ou
anéjaculation.
L’incidence
des
troubles
de
l’éjaculation
variait
de
6
%
à
11
%
vs
<
1
%
dans
le
groupe
placebo
[21—23].
Dans
l’étude
CombAT
comparant
la
tamsulosine,
le
dutastéride
et
leur
association,
à
2
ans,
l’éjaculation
rétro-
grade
a
été
rapportée
chez
1,1
%
des
patients
traités
par
tamsulosine,
l’anéjaculation
chez
0,8
%
et
une
diminution
de
volume
d’éjaculât
chez
0,8
%
[24].
D’autre
part,
la

118
A.
Descazeaud
et
al.
Publicaons re
pérées
dans la base de données* (Medline)
(n = 351)
Sélecon Inclusion Eligibilité Idenficaon
Publica
ons
re
pérée
s dans d’autres
sources (n = 0)
Publicaons après retrait des doublons
(n = 310)
Publicaons
sélec
onnées
(n = 310)
Publica
ons
exclues
(n = 250)
Arcles
com
plets
éval
ués
(n = 60)
Arcles
complets ex
clus pou
r le
s ra
isons
suivantes (
n = 26
):
- Durée du t
raitement < 12
semain
es (
3)
- Dose administ
rée < d
ose appr
ouvée (1)
- Analyse g
roupée d’étud
es à m
éthodologi
e
différent
e ou
manquan
t de pr
écisi
on (3)
- Analyse ré
trospec
ve (
1)
- Ré
sultat
s inclus
dans d’a
utre
s ar
cles (
3)
- Paen
ts au
torisés
à prend
re un
produ
it à
même
visée théra
peuqu
e (
1)
- Ré
sultats
de toléra
nce non
rapportés
(4)
- Ex
tension
sa
ns bras
pl
acebo (4)
- Dose d
e traitement
mo
difiée
(1)
- R
ésultats
de s
ous-g
roupe (1)
- Absenc
e de
br
as pl
acebo
(4
)
Études
incluses
(n = 34)
La sélection des articles était à la discrétion des auteurs.
*La recherche bibliographique n’a pas été réalisée pour
les
extraits
de
pla
nte.
Pour cette
clas
se,
deux meta-
analyses
on
t été utilisées, un
e pour se
renoa repens et
une pour pygeum africa
num
Figure
1.
Diagramme
PRISMA.
dysfonction
érectile,
la
diminution
de
la
libido
et
la
perte
de
la
libido
ont
été
rapportées
chez
3,8
%,
1,7
%
et
0,9
%
respectivement.
À
4
ans,
les
fréquences
étaient
de
1
%
pour
l’éjaculation
rétrograde
et
<
1
%
pour
l’anéjaculation
et
la
diminution
de
volume
d’éjaculât
Avec
ce
recul,
la
dysfonc-
tion
érectile
a
été
rapportée
chez
5
%
des
patients,
la
baisse
et
la
perte
de
la
libido
chez
respectivement
2
%
et
1
%
des
patients
[25]
(Tableau
1).
Dans
une
étude
portant
sur
48
volontaires
sains,
90
%
des
sujets
ayant
rec¸u
la
tamsulosine
0,4
mg,
2
fois
par
jour
pendant
5
jours
ont
eu
une
diminution
d’au
moins
20
%
du
volume
d’éjaculât
et
35
%
une
anéjaculation
[26].
Dans
le
RCP
de
la
tamsulosine,
l’éjaculation
anormale
est
rapportée
comme
peu
fréquente
et
le
priapisme
est
consi-
déré
comme
très
rare
(Tableau
2
:
RCP
de
la
tamsulosine).
La
silodosine
a
obtenu
son
AMM
le
29
janvier
2010.
La
posologie
recommandée
est
de
8
mg
en
une
seule
prise
quotidienne.
Dans
les
études
randomisées,
l’incidence
des
troubles
de
l’éjaculation
(éjaculation
rétrograde,
émission
réduite
ou
nulle
de
sperme)
était
significativement
plus
fré-
quente
avec
la
silodosine
qu’avec
le
placebo
:
22,3
%
vs
0
%
;
28,1
%
vs
0,9
%
et
14,2
%
vs
1,1
%
[27—29]
(Tableau
1).

Effets
négatifs
des
médicaments
de
l’HBP
sur
la
sexualité
119
Tableau
1Résumé
des
effets
indésirables
sexuels
dans
les
études
cliniques
randomisées
contrôlées.
Référence
étude Posologie Durée
du
traitement
Effectif Effets
indésirables
(%
patients)
Érection
Éjaculation
Libido
Dysfonction
sexuelle
T
P
T
P
T
P
T
P
T
P
Alpha-bloquants
Alfuzosine
Jardin
[9] Std
2,5
mg,
3
fois/j
6
mois 251
267
<
1 2,3
—
—
—
—
—
—
Hyearsen
[10] Std
2,5
mg,
3
fois/j
12
semaines 104
101
—
—
—
—
—
—
—
—
Debruyneb[50] 5
mg
LP,
2
fois/j
6
mois 358
—
2,2
—
0
—
0,6
—
Buzelin
[12] 5
mg
LP,
2
fois/j
12
semaines 194
196
—
—
—
—
—
—
—
—
Van
Kerrebroeck
[11]
Std
2,5
mg,
3
fois/j
10
mg
LP,
1
fois/j
3
mois 149143
154
0,7
0
1,3
—
—
—
—
—
—
Roehrborn
[13] 10
mg
LP,
1
fois/j
3
mois 176
175
2,8
1,1
<
1
0
—
—
—
—
Nordling
[14] 10
mg
LP,
1
fois/j
12
semaines 154
154
1
0
1
0
—
—
—
—
Roehrborna[15] 10
mg
LP,
1
fois/j
12
semaines 473
482
1,5
0,6
0,6
0
—
—
—
—
Roehrborn
[16] 10
mg
LP,
1
fois/j
2
ans 759
763
2
1,8
0,4
0
—
—
—
—
Doxazosine
Andersen
[17] Std
1—8
mg/j
4—8
mg
LP/j
13
semaines 322317
156
—
—
—
—
—
—
—
—
Kirbya[19] Std
1—8
mg/j
4—8
mg
LP/j
13
semaines 651666
156
—
—
—
—
—
—
—
—
—
Kirby
[18] Std
1—8
mg/j 52
semaines 275
269
5,8
3,3
0,4
1,5
3,6
1,9
—
—
McConnell
[20] Std
1—8
mg/j 5
ans 756
737
3,6e3,3e1,1e0,8e1,6e1,4e—
—
Tamsulosine
Narayan
[21] 0,4
mg/j 13
semaines 248
239
—
—
11
<
1—
—
—
—
Lepor
[22] 0,4
mg/j 13
semaines 254
254
—
—
6
0
—
—
—
—
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
1
/
13
100%