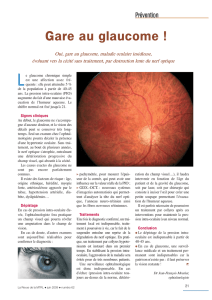
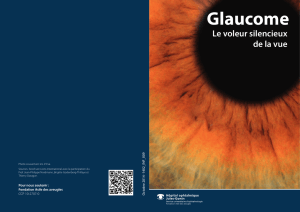
thèse incidence du glaucome primitif a angle ouvert a l`iota de juillet

1
MINISTÈRE DES ENSEIGEMENTS RÉPUBLIQUE DU MALI
SECONDAIRE, SUPERIEUR ET DE
LA RECHERCHE SCIENTIFIQUE Un Peuple–Un But–Une Foi
***************
UNIVERSITÉ DE BAMAKO
FACULTÉ DE MÉDECINE, DE PHARMACIE ET D’ODONTO –
STOMATOLOGIE
ANNEE UNIVERSITAIRE : 2008-2009 N°………/
THÈSE
Présentée et soutenue publiquement le ……/……/2009
Devant la Faculté de Médecine, de Pharmacie et d’Odontostomatologie
Par
Mme SISSOKO Rokiatou Cheick dite Bassira TRAORE
Pour obtenir le Grade de Docteur en Médecine
(DIPLOME D’ETAT)
Jury
PRESIDENT : Professeur Abdoulaye DIALLO
MEMBRES: Professeur TRAORE Jeannette THOMAS
Docteur Seydou BAKAYOKO
DIRECTEUR DE THESE : Docteur Lamine TRAORE
I
IN
NC
CI
ID
DE
EN
NC
CE
E
D
DU
U
G
GL
LA
AU
UC
CO
OM
ME
E
P
PR
RI
IM
MI
IT
TI
IF
F
A
A
A
AN
NG
GL
LE
E
O
OU
UV
VE
ER
RT
T
A
A
L
L’
’I
IO
OT
TA
A
D
DE
E
J
JU
UI
IL
LL
LE
ET
T
2
20
00
06
6
A
A
J
JU
UI
IL
LL
LE
ET
T
2
20
00
07
7

2
DEDICACES
Hommage à Dieu
Je rends grâce au Tout Puissant, l’Etre Suprême, l’Omnipotent
et l’Omniscient « Allah Soubahana Wata Allah (SWA). Je me
prosterne devant Toi pour implorer votre miséricorde, pour la vie
d’ici bas et surtout pour la vie d’au-delà.
Il a été, est, et sera toujours mon compagnon dans toutes mes
entreprises. Paix et Salue soit sur le prophète Mohamed (SAW).
Je Dédie ce travail
A tous ceux qui souffrent de GPAO
A tous ceux qui oeuvrent pour le meilleur traitement de cette affection

3
A mon père : Cheick Oumar Traoré
Homme de principe et de loyauté, ton humour, ta tolérance et ton
autorité de père ont fait de moi ce que je suis aujourd’hui. Tu nous as
appris le sens de la responsabilité, de devoir et de travail. C’est toi qui
m’as appris à aimer le bien et à fuir le mal. Tu as été pour moi un modèle
de courage. Grâce à cette qualité, tu m’as toujours soutenu dans mes
études (nous ne te remercierons jamais assez pour nous avoir donner
une éducation et avoir orienté notre carrière).
Sans tes sacrifices, tes conseils et encouragements, tes prières et
bénédictions, ce travail n’aurait jamais pu être réalisé. Je promets, avec
l’accord de Dieu, de ne jamais faillir à mon devoir de fille. Très cher père,
les mots me manquent en ce moment solennel pour te remercier,
trouves ici dans ce témoignage les manifestations de mon affection
profonde et de ma reconnaissance indéfectible à ton égard. Puisse Dieu
te garder encore longtemps auprès de tes enfants. Amen !
A ma mère : Kinty Diallo
Femme courageuse, infatigable, patiente, tu as guidé mes premiers pas.
Tu es pour moi un modèle de courage et de bonté. Ton dévouement
pour la réussite de tes enfants est certain. J’ai toujours bénéficié de ton
affection qui m’a beaucoup consolé dans la vie, surtout dans les
moments difficiles. Sans tes sacrifices, tes conseils et encouragements,
tes prières et bénédictions, ce travail n’aurait jamais pu être réalisé.
Très chère mère, nous ne te remercierons jamais assez, trouves ici dans
ce témoignage les manifestations de mon affection profonde et de ma
reconnaissance indéfectible à ton égard. Puisse Dieu te garder auprès
de tes enfants encore longtemps.

4
A ma Tante Néné Touré
Votre générosité et votre bonté font de vous une femme remarquable.
Veuillez retrouver ici l’expression de ma grande considération.
A mon très cher époux : Douga Sissoko
Je n’ai pas trouvé des mots pour décrire ce que vous aviez enduré
pendant mes années d’études. Ce travail est le résultat de votre profond
amour et un encouragement à mieux faire. Que Dieu t’accorde une très
longue vie et beaucoup de bonheur.
A mes enfants : Mariam, Kinty et N’Faly.
Vous aviez souffert durant mes années d’étude, mais cela en valait la
peine. Que ce travail soit pour vous un exemple à suivre et faites mieux.
Avec tout mon amour.
A mon Oncle : feu Hamet Traoré
J’ai voulu que tu sois là aujourd’hui pour partager avec nous la joie de ce
jour tant attendu. Mais la mort t’a prématurément arraché à notre
affection. Dans votre repos éternel, nous avons toujours besoin de votre
bénédiction. Que ton âme repose en paix.
A ma Tante : feue Coumba Diallo
Plus qu’une tante, tu étais une mère pour moi. Ta disparition a créé un
grand vide dans ma vie que j’ai cherché à combler par le travail bien fait.
A travers ce modeste travail, je te rends un sincère hommage, tu
resteras toujours vivant dans mon cœur. « Puisse Allah t’accueille dans
son paradis ». Amen !

5
A mon Oncle Mamadou , dit Mamy Traoré
Votre soutien, votre simplicité, votre apport, durant tout notre parcours
scolaire ne nous ont jamais fait défaut. Je vous en serai toujours
reconnaissante.
A mon Oncle Diguidjan Diallo dit Vieux
Ce travail est l’aboutissement de plusieurs années d’éducation. Votre
soutien moral et matériel ne m’a jamais fait défaut. Soyez assuré de mon
profond respect.
A mes frères et sœurs
En témoignage de l’affection qui nous a toujours uni sous le toit paternel.
Je voudrais que vous trouviez dans ce travail le fruit des efforts que vous
avez consentis à mon égard. Gardons l’esprit de la cohésion familiale et
le sens de devoir, que nos parents nous ont inculqués. Ce travail est
aussi le vôtre. Que le Tout Puissant préserve et renforce notre affection
fraternelle.
A tonton Mamadou Koniba Coulibaly
Vous n’avez ménagé aucun effort pour m’accueillir chez vous au cours
de ce travail. Votre soutien a abouti au succès dont vous avez tant rêvé.
Je vous suis très reconnaissante durant toute ma vie. Recevez du fond
de mon cœur tous mes remerciements et soyez rassuré de mon profond
attachement.
A tous les malades souffrants de GPAO
A tous ceux qui s’intéressent à la lutte contre la cécité
A tous ceux qui m’ont aidé de loin ou de près à l’élaboration de ce
travail.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
 57
57
 58
58
 59
59
 60
60
 61
61
 62
62
 63
63
 64
64
 65
65
 66
66
 67
67
 68
68
 69
69
 70
70
 71
71
 72
72
 73
73
 74
74
 75
75
 76
76
 77
77
 78
78
 79
79
 80
80
 81
81
 82
82
 83
83
 84
84
 85
85
 86
86
 87
87
 88
88
 89
89
1
/
89
100%