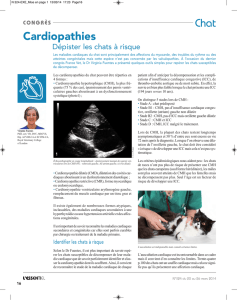
La Cardiomyopathie hypertrophique

La Cardiomyopathie hypertrophique
par le Docteur Vétérinaire C. Blandin
Selon les Nouvelles de février 2006
La cardiomyopathie hypertrophique (CMH) est aujourd'hui l'affection cardiaque la plus diagnostiquée chez le
chat : selon les auteurs, entre 12 et 15 % des chats nord-américains seraient atteints de CMH. L'affection est
caractérisée par des altérations myocardiques biochimiques et histologiques conduisant à une hypertrophie
concentrique primaire de la paroi libre des ventricules et/ou du septum interventriculaire. Plusieurs anomalies
cardiaques sont souvent associées à l'hypertrophie ventriculaire, comme une dilatation secondaire des atria,
l'hypertrophie du muscle papillaire et des dysfonctionnements cardiaques d'abord diastoliques puis parfois
systoliques.
De nombreuses affections peuvent conduire à une hypertrophie concentrique des ventricules mais le
diagnostic de CMH n'est établi que lorsque l'affection est primaire. Toutes les causes de CMH secondaire
doivent donc être écartées avant que l'on puisse parle de CMH.
Incidence de la maladie :
Les chats atteints de cardiomyopathie hypertrophique sont en général des chats à poils courts : Bristish,
chartreux, siamois, burmese mais certaines races à poils longs sont aussi touchées par cette affection. C'est le
cas du Maine Coon, du persan et de l'Himalayen.
Les premières symptômes apparaissent en moyenne vers l'âge de 7 ans, avec des variations entre 3 mois et
17 ans. La forme familiale chez le Maine Coon a un développement plus rapide : chez la plupart des Maine
Coon, la maladie se déclenche entre 6 mois et 2,5 ans avec une espérant de vie de 4,8 ans.
La CMH atteint plus fréquemment les mâles que les femelles : jusqu'à 87 % de mâles selon les études.
Le milieu de vie semble également avoir une influence sur cette cardiopathie puisqu'elle serait surtout
rencontrée en milieu urbain. Il semblerait que les chats de la côte Est des Etats-Unis soient plus touchés que
dans le reste du pays.
La première famille de chat atteinte de CMH qui fut identifiée et étudiée est une famille de Maine Coon. En
1993, aux Etats Unis, l'équipe de Kittleson a étudié une famille atteinte de CMH.

La maladie a été reproduite en accouplant des individus apparentés atteints avec des individus sains ou en
accouplant des chats malades entre eux.
Il a été prouvé que la maladie se développait plus rapidement chez les chats issus de l'accouplement de deux
parents malades (symptômes dès l'âge de 6 mois et augmentation du nombre de mort-nés dans la portée
(33%). Ces données étaient fortement en faveur d'une transmission génétique de la cardiomyopathie
hypertrophique dans cette famille de Maine Coon. L'étude du pedigree a ensuite montré qu'il s'agissait,
comme chez l'homme, d'une affection à déterminisme génétique autosomique dominant.
Selon les auteurs, la maladie est à dominance complète ou incomplète chez le chat. Pour Kittleson, la
pénétrance est de 100 % et les morts nés seraient les homozygotes qui ne seraient pas viables. Mais pour
d'autres, il existerait des chats asymptomatiques qui possèderaient la mutation et un ou plusieurs gènes
facilitateur serait mis en jeu pour que le phénotype soit exprimé.
Quoiqu'il en soit, Kittleson affirme que dans la famille de Maine Coon qu'il a étudié, tous les chats porteurs
d'une mutation sont atteints de cardiomyopathie hypertrophique. Des études sont en cours aux Etats-Unis
pour déterminer si une mutation spécifique dans un gène codant pour une protéine du sarcomère est présente
dans cette famille de Maine Coon.
Cependant, la composante génétique de la CMH féline ne suffit pas à expliquer d'autres modifications
structurelles rencontrées dans le phénotype des animaux malades, comme des anomalies des vaisseaux
coronaires intramuraux ou un mauvais arrangement des matrices de collagène. Ceci laisse à penser que
l'expression phénotype de la mutation est également dépendante de facteurs liés à l'environnement.
L'influence de l'hormone de croissance est une autre piste étudiée actuellement. En effet, Kittleson a
remarqué que 60 % des chats atteints de cardiomyopathie hypertrophique ont une concentration d'hormone
de croissance élevée dans le sang. Or, l'hormone de croissance est connue pour induire des hypertrophies du
myocarde.
Par exemple, les chats atteints d'acromégalie peuvent développer une hypertrophie importante du myocarde
du ventricule gauche. Mais on ne sait pas encore si l'augmentation de la concentration en hormone de
croissance est la cause, la conséquence ou est indépendante de la cardiomyopathie hypertrophique.
Mécanismes physiopathologiques :
Hypertrophie du ventricule gauche :
Le cœur est soumis à une activité périodique. On désigne sous le terme de "révolution cardiaque" l'ensemble
des phénomènes se produisant pour une période.
Le remplissage des ventricules s'effectue pendant la diastole ventriculaire. Ce remplissage est d'abord passif
du fait du retour vaineux, puis le systole auriculaire complète le remplissage. L'hypertrophie concentrique du
ventricule gauche empêche donc le ventricule gauche de se remplir correctement : d'abord en raison de la
perte de souplesse des parois pendant la diastole ventriculaire. Et cela, même si ce manque de souplesse est
dans un premier temps compensé par une hypertrophie réactive de l'atrium gauche. Puis comme le ventricule
gauche se remplit mal, le débit cardiaque diminue, ce qui stimule le système sympathique d'où une
augmentation de la fréquence cardiaque. Malheureusement, lorsque la fréquence cardiaque augmente, les
diverses phases de la révolution cardiaque sont modifiées. La diastole est la phase du cycle cardiaque la plus
affectée. De ce fait, le remplissage passif des ventricules diminue : un cercle vicieux démarre.
Le ventricule n'étant pas remplit correctement, le volume d'éjection systolique est faible. Et ce volume est
encore plus faible lorsqu'un fonctionnement anormal de la valve mitral créé un obstacle à l'éjection du sang
dans la circulation générale ou permet un reflux de sang dans l'atrium gauche pendant la systole ventriculaire
Ce manque de sang dans la circulation générale entraîne une hypoperfusion du rein. Et la baisse de pression
de perfusion dans les artérioles rénales stimule le système rénine-angiotensine.

Remaniement de l'atrium gauche :
La contraction de l'atrium gauche augmente chez les animaux touchés pour lutter contre l'hypertension dans
le ventricule en fin de diastole. Cela permet dans un premier temps de compenser partiellement la baisse du
remplissage ventriculaire. Mais le développement, par la suite, d'une fibrillation atriale a des conséquences
hémodynamiques graves et constitue un pronostic sombre dans le suivi de la maladie.
De plus, l'augmentation de la contraction atriale et de la pression dans l'atrium gauche favorisent la
congestion des veines pulmonaires puis l'installation d'un œdème pulmonaire et/ou d'un épanchement pleural.
Enfin la dilatation de l'atrium est à l'origine d'une stase sanguine qui favorise la formation de thrombi pouvant
ensuite s'emboliser dans la circulation artérielle.
Anomalie de la valve mitrale :
L'évolution hypertrophique souvent asymétrique des muscles papillaires peut créer une déformation de la
valve mitrale. Selon un étude récente menée par Kittleson, jusqu'à 67 % des Maine Coon atteints de CMH
seraient touchés par cette anomalie. Cette anomalie est dénommée : mouvement antérieur systolique (SAM)
de la valve mitrale. Ce SAM a deux conséquences potentielles. La valvule antérieure peut être attirée dans le
ventricule gauche pendant la systole et plaquée contre le septum interventriculaire, pouvant ensuite
représenter un obstacle à l'éjection du sang dans l'aorte. En seconde conséquence, la valvule septale étant
déplacée, la SAM peut s'accompagner de régurgitation mitrale. Les chats souffrant de SAM, bien que souvent
asymptomatiques, ont des risques de décompensation et de mort subite lors de stress, de douleur ou de
médication inadaptée.
Troubles du rythme :
La fibrose myocardique peut être responsable de phénomènes de réentrées, plus particulièrement lorsque le
myocarde est ischémique. L'athérosclérose des artères coronaires est un facteur d'ischémie myocardique de
CMH.
Complications :
Les altérations anatomiques et fonctionnelles de myocarde peuvent conduire à de nombreuses complications :
œdème pulmonaire, épanchement pleural, thromboembolie, syncopes et mort subite.
Diagnostic :
L'examen clinique : Les symptômes de CMH peuvent être variés ou inversement, l'affection peut passer
inaperçue, avec en général une dégradation de l'état clinique lorsque les mécanismes compensateurs sont
dépassés. Anorexie et apathie, parfois vomissements la veille de la décompensation sot souvent les seuls
éléments de l'anamnèse. La plupart des chats restent totalement asymptomatiques jusqu'au développement
d'une insuffisance cardiaque congestive suraiguë avec arythmies, œdème pulmonaire, épanchement pleural et
parfois thrombose artérielle associée. La détresse respiratoire et la dyspnée sont les seuls symptômes
présents chez le chat lors d'œdème pulmonaire ou d'épanchement pleural, la toux n'étant présente chez le
chat que lors d'atteinte de l'appareil respiratoire lui-même. La cardiomyopathie hypertrophique peut être
découvert fortuitement grâce à l'audition d'un souffle cardiaque systolique apexien gauche et/ou d'un bruit de
galop.
Des signes liés à l'existence d'une thrombo-embolie artérielle peuvent également être présents, associés ou
non aux symptômes cités ci-dessus. Ces troubles apparaissent en général brutalement et dépendent de
l'endroit où s'est logé le thombus.
Symptômes pouvant accompagner une thrombo-embolie artérielle féline : parésie ou paralysie du train
postérieur parfois seule une boiterie intermittente est présente ; parésie d'un membre antérieur ; vocalises
dues à la douleur et au stress ; les membres affectés sont douloureux, froids surtout en région distale, les
coussinets sont pales voire cyanosés comme peuvent être les griffes ; des signes d'insuffisance cardiaque
peuvent aussi être présents.
1
/
3
100%