CINÉTIQUE DE LA PYROLYSE DU DIMÉTHYL ÉTHER 1)On étudie

CINÉTIQUE DE LA PYROLYSE DU DIMÉTHYL ÉTHER
1)On étudie la pyrolyse d'un composé A effectuée à température et volume constants.
Soit a la molarité de A à la date t = 0 et a - x la molarité de A à la date t.
La réaction est supposée d'ordre m par rapport à A.
a. Exprimer la vitesse de cette réaction.
On appellera k la constante de vitesse de la réaction relative aux molarités.
Soit a la molarité de A à la date t = 0 et a - x la molarité de A à la date t.
La réaction est supposée d'ordre m par rapport à A.
b. Déterminer la relation existant entre x et t dans les deux cas: m =1 et m ≠1.
c. Dans le cas où A est un gaz parfait, la cinétique peut être suivie en mesurant la pression partielle PA de A.
Exprimer alors −dPA
dt en fonction de PA.
La constante de vitesse relative aux pressions sera notée kp et on donnera son expression en fonction de k.
La constante des gaz parfaits est R =8,31 J K-1 mol-1 .
d. Exprimer PA en fonction de t et déterminer le temps de demi-réaction dans les deux cas précédents.
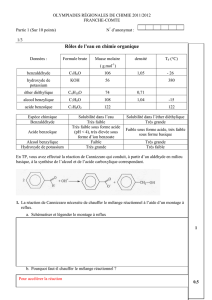
2)On étudie à 504°C la pyrolyse du diméthyl éther CH3−O−CH3.
a. Les mesures de la pression de CH32O , exprimée en kilopascals, à différents instants ont donné les résultats
suivants:
tmn0 5 9 15 20,5 25 32,5 38 46 70 90
PAkPa32,9 29,6 27,2 24,2 21,2 19,7 17,4 15,9 13,8 10,0 8,16
Déterminer graphiquement la valeur de la vitesse initiale, v0, de la réaction.
b. Dans les mêmes conditions expérimentales θ=504 °C, on a déterminé la vitesse initiale v0 pour
différentes valeurs de la pression initiale P0 du diméthyl éther:
P0kPa8,55 13,7 27,6 39,5 55,3
v0Pa mn-182,1 170 477 830 1 350
En déduire la constante de vitesse kp. Calculer k que l'on exprimera en mol
−1
2L
1
2s-1 .
Déterminer l'ordre de la réaction par rapport au diméthyl éther.
c. En étudiant la pyrolyse à différentes températures on obtient:
θ°C477 497 517 537
103kmol−1
2L
1
2s-11,23 3,17 7,74 18,1
Déterminer l'énergie d'activation de cette réaction.
1
/
1
100%