Lire l`article complet

M
I S E A U P O I N T
La Lettre du Rhumatologue - n° 306 - novembre 2004
19
Immunopathologie de la polyarthrite rhumatoïde
Pathogeny of rheumatoid art h r i t i s
●
J. Morel*, B. Combe*
* Service d’immunorhumatologie, CHU Lapeyronie, Montpellier et unité
Inserm U454.
La physiopathologie de la polyarthrite rhumatoïde
(PR) a connu ces vingt dernières années des progrès
considérables marqués, entre autres, par :
■
La découverte des cytokines, en particulier de
l’IL-1 et du TNFα, qui a permis une meilleure com-
préhension de l’inflammation et le développement
de traitements ciblés très efficaces.
■
Une prédisposition génétique à la PR, en parti-
culier avec les gènes HLA DRB1*04. La présence de
ces allèles est associée à la PR et représente un fac-
teur de mauvais pronostic de la maladie.
■
La présence dans le sérum des patients du facteur
rhumatoïde et d’anticorps très spécifiques de la
maladie, dirigés contre les peptides citrullinés (anti-
CCP). La spécificité des anti-CCP suggère que l’on
s’approche de l’antigène responsable de la PR.
■
Le démembrement des mécanismes impliqués
dans la transduction du signal soulignant l’impor-
tance des molécules lymphocytaires de costimulation
et des voies intracellulaires de signalisation dans le
contrôle de l’inflammation et l’avènement de nou-
veaux traitements (CTLA4-Ig).
■
Les théories actuelles sur la pathogénie de la PR
font intervenir l’immunité innée indépendante des
lymphocytes T, mais responsable de la libération
d’une cascade de cytokines pro-inflammatoires, l’im-
munité acquise antigène spécifique médiée par les
lymphocytes T ou encore le comportement pseudo-
tumoral des synoviocytes rhumatoïdes.
M o t s - c l é s :
Physiopathologie - PR - Immunité
innée - Immunité acquise - Cytokines - Voies de
signalisation - HLA D R B 1 * .
K e y w o r d s : Pathogeny - RA - Innate immunity -
A c q u i r ed immunity - Cytokines - Signaling path-
ways - HLA D R B 1 * .
P o i n t s f o r t s
L
a polya rt h rite rhumatoïde est un rhumatisme infl a m m a-
t o i re re s p o n s a ble d’une destruction de l’art i c u l ation qui
contribue à une impotence fonctionnelle parfois majeure.
Même si des progrès considérables ont été faits dans la compré-
hension physiopathologique de cette maladie,son origine reste
t o u j o u rs inconnu e. Plusieurs fa c t e u rs interviennent dans le
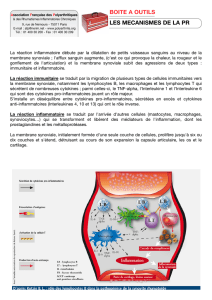
Figure 1. Le déclenchement de la PR pourrait faire intervenir l’immunité
innée et/ou l’immunité acquise. L’activation des récepteurs Toll likesti-
mule les cellules dendritiques, les synoviocytes, les macrophages. L’acti-
vation des lymphocytes T dépendrait de la reconnaissance d’un antigène
présenté par les CPA. Dans les deux cas, cela aboutirait à l’activation des
lymphocytes T en lymphocytes Th1. Ces lymphocytes stimuleraient, par
l ’ i n t e r m é d i a i re de cy t o k i n e s , les synov i o cytes et les macro p h ages. Les molé-
cules (cy t o k i n e s , enzymes) produites par ces cellules active raient les ostéo-
clastes. Ces ostéoclastes, sous l’effet de RANKL, seraient activés et inter-
viendraient dans la destruction ostéoarticulaire.
HEV: high endothelial veinule,veinule postcapillaire.
Syno. F: synoviocytes fibroblastiques.
λ
: lymphocyte.

La Lettre du Rhumatologue - n° 306 - novembre 2004
20
M
I S E A U P O I N T
d é cl e n chement de la maladie : des fa c t e u rs horm o n a u x , le ter-
rain génétique prédisposé et des facteurs environnementaux (1).
L o r sque tous ces fa c t e u rs sont réunis, ils activent une réponse
immunitaire innée et acquise incontrôlée qui se traduit par une
réaction infl a m m a
t o i r e ex ag é r é e, en particulier de la membra n e
synoviale (2) (figure 1, voir p. 19).
Cette synoviale est une struc-
t u re habituellement paucicellulaire avec une couche bord a n t e,
c ’ e s t - à - d i re pro che de la cavité art i c u l a i re qui est mince. La syno-
viale rhumatoïde est, en revanche, infiltrée par des cellules com-
prenant principalement des lymphocytes T CD4+, des lympho-
cytes B et des macro p h a ges qui s’organisent en agr é gat s
lymphoïdes, avec parfois des centres germinaux dont la structure
rappelle celle d’un ganglion. Elle se caractérise également par
une pro l i f é ration de la couche bordante qui est composée de syno-
v i o cytes et de macro p h a ges mais aussi par une pro l i f é rat i o n
importante de néovaissaux. La PR est classée parmi les maladies
a u t o - i m m unes en raison de nombreux signes d’autoréactivité ave c
la présence d’auto-anticorps, comme les facteurs rhumatoïdes,
mais aussi les anticorps antifillagrine. La physiopathologie de la
PR pourrait être comparée à un puzzle dont certaines pièces sont
a u j o u rd’ hui identifiées mais dont l’agencement final reste encore
mal connu. Nous aborderons successivement la participation de
l ’ i m mun ité innée, des cytokines et de l’immunité acquise, l e s
synoviocytes et, enfin, les voies intracellulaires de signalisation
impliquées dans la PR.
L’IMMUNITÉ INNÉE
L’immunité innée est une réponse immunitaire non spécifique en
réaction à un élément étra n ge r. Les cellules dendri t i q u e s , l e s
m o n o cy t e s / m a c ro p h age s , les poly nu cl é a i res neutrophiles (PNN)
mais aussi les mastocytes, interviennent dans l’activation de la
réponse innée. Lee et al. suggèrent que les mastocytes seraient
le chaînon entre les autoanticorps, le système du complément et
les médiat e u rs de l’infl a m m ation (3). En effe t , les souris défi-
cientes en mastocytes ne développent pas d’arthrite après injec-
tion de sérum arthritogénique tandis que la greffe de mastocytes
les rend à nouveau suscep t i bles à une art h ri t e. Les diff é rentes cel-
lules impliquées dans l’immunité innée sont attirées dans la mem-
brane synoviale par des chimiokines. Les chimiokines MCP-1,
MIP-1 et RANTES attirent les cellules dendritiques tandis que
l’IL-8 at t i r e surtout les PNN. Des agents infectieux vira u x
(Epstein-Barr), bactériens (Escherichia coli) et mycobactériens
ont été incriminés dans le déclenchement de la PR par activation
de l’immunité innée. Les agents infectieux peuvent en effe t
induire une réponse immunitaire innée par activation des récep-
teurs Toll like(TLR) (4). Ces TLR reconnaissent des molécules
exprimées par les micro-organismes : TLR4 est activée par les
composants lipopolysacchari
diques de la membrane bactérienne
et TLR9 interagit avec les oligo
nucléotides CpG présents dans
l’ADN bactérien. Ces dérivés bactériens pourraient déclencher
une réaction inflammatoire mais aussi faciliter la pérennisation
de l’infl a m m ation en favo risant une stimu l ation récurrente de
l’immunité innée. Cette réponse immunitaire innée déclenche la
libération en cascade de nombreuses cytokines et, en particulier,
d’IL-1 et de TNFα.
LES CYTOKINES
(figure 2)
Leur découve rte a été d’une importance pri m o r diale dans la
compréhension de la physiopathologie de la PR et de l’inflamma-
tion en général. Les cytokines sont des messagers intercellulaires
qui permettent aux cellules de communiquer entre elles sans qu’il
y ait un contact cellulaire. Il existe quat re grandes familles de
cy t o k i n e s : les interl e u k i n e s , les interféro n s , les fa c t e u rs de cro i s-
sance et les chimiokines. Dans la PR, il existe un déséquilibre
e n t re les cytokines pro - i n fl a m m at o i r es et les cytokines anti-
i n fl a m m a t o i res. Les cytokines pro - i n fl a m m at o i r e s , comme le
T N Fα,l ’ I L - 1 , l ’ I L - 1 5 , l ’ I L - 1 7 , l ’ I L - 1 8 , l ’ I L - 6 , mais aussi les fa c-
t e u rs de croissance et les chimiokines sont présents à des concen-
t rations élevées dans le liquide synovial et dans le sérum des
p atients atteints de PR ( 5 ) . Les monocy t e s , les ly m p h o c ytes T
activés, les macrophages et les synoviocytes sont les principaux
p ro d u c t e u rs de ces cytokines. L’IL-1ß et le T N Fαsont deux
cytokines clés de l’inflammation articulaire(6). Ils contrôlent
la production de nombreuses autres cytokines comme le fibro-
blast growth factor,le vascular endothelial growth factor et les
ch i m i o k i n e s , mais aussi des molécules d’adhésion qui inter-
viennent également dans la réaction inflammatoire en favorisant
l’angiogenèse et le recrutement des cellules dans la synoviale.
Les cellules endothéliales stimulées avec du TNFα,de l’IL-1
ou de l’IL-18 ex p riment des molécules d’adhésion, d ’ a b o rd des
sélectines (E-sélectine,L-sélectine) puis des intégrines (αEβ7,
α4β7 , α4β1) qui interagissent entre elles. L’ i n t e raction des
cellules circulantes avec les cellules endothéliales permet la dia-
pédèse de ces cellules qui passent alors dans la membrane syno-
viale. Les cellules circulantes migrent ensuite dans la synoviale
en exprimant à leur surface membranaire des récepteurs aux chi-
m i o k i n e s , comme CCR5, qui reconnaissent des chimiokines telles
Figure 2. Les lymphocytes T activent les cellules synoviales résidentes par
les cytokines IFNγet IL-17. Les synoviocytes, les macrophages et les cel-
lules dendritiques produisent des cytokines capables de stimuler ou d’in-
hiber les cellules résidentes présentes dans la synov i a l e . Les cytokines pro -
et anti-inflammatoires sont respectivement indiquées par les signes + et –.
IL = interleukine ; GM-CSF = granulocyte-macrophage colony-stimulating factor ; IL-1Ra
= antagoniste du récepteur de l’IL-1, STNFR = récepteur soluble du TNF
α
; Mø : macro -
phage ; Syno. F : synoviocytes fibroblastiques.
λ
:lymphocyte.

La Lettre du Rhumatologue - n° 306 - novembre 2004
21
M
I S E A U P O I N T
que RANTES,produites dans la synoviale (7). Le rôle central du
TNFαet de l’IL-1βdans la pathogénie de la PR a été confirmé
ces dernières années avec l’utilisation des traitements capables
de les neutraliser (8). Les agents modulant le TNFαont montré
une efficacité anti-inflammatoire remarquable en réduisant l’an-
giogenèse et l’infiltrat inflammatoire dans la synoviale (9). Ces
t r aitements ont également montré l’importance de ces deux cy t o-
kines dans la destruction ostéoarticulaire observée dans la PR.
Des données récentes sugg è rent l’implication de la cy t o k i n e
RANKL dans la résorption osseuse sous-chondrale des patients
atteints de PR. Le Receptor Activator of NFκB ligand (RANKL)
est exprimé à la surface des cellules de la lignée ostéoblastique,
mais aussi des lymphocytes activés et des cellules endothéliales
( 1 0 ) . La production de RANKL est régulée par les cytokines pro -
i n f l a m m a t o i r es telles que IL-1, T N Fαet IL-17. RANK est le
r é c ept eur membra n a i re de RANKL et l ’ o s t é o p r o t é g é rine (OPG)
est la forme soluble du récepteur. La liaison de RANKL à son
récepteur membranaire RANK, présent sur les préostéoclastes,
favo rise la diff é r e n c i ation et l’activation des ostéocl a s t e s .
RANKL est trouvé à des concentrations élevées dans le sérum et
le liquide synovial des patients atteints de PR. Le rôle de RANKL
dans la destruction articulaire est fortement suggéré par l’effet
antirésorptif de l’OPG dans différents modèles d’arthrites expé-
rimentales.
D’autres cytokines, comme l’IL-15, l’IL-17, l’IL-18 et l’IL-6,
participent également à la physiopathologie de la PR. L’IL-18 et
l’IL-15 sont produites par les monocytes/macrophages et favo-
risent l’ex p ression de T N Fα( 1 1 ) . L’IL-6 est une cytokine qui
cumule à la fois des propriétés pro- et anti-inflammatoires (12).
En effet, l’IL-6 induit, d’une part, les protéines de la phase aiguë
de l’inflammation et, d’autre part, elle est capable de freiner la
production de l’IL-1, du TNFαet des chimiokines. Son rôle dans
la pathogénie de la PR est encore mal connu mais indiscutable.
La neutralisation de l’IL-6 par un anticorps monoclonal dirigé
contre le récepteur de l’IL-6 (MRA) donne,en effet, des résul-
tats très encourageants dans le traitement de la PR.
L’IMMUNITÉ ACQUISE
L’ i m munité acquise est une réponse immu n i t a i re spécifi q u e
contre un antigène.Les cellules présentant l’antigène,les lym-
phocytes T et les lymphocytes B en sont les principaux acteurs
cellulaires.
Cellules présentant l’antigène et HLA de classe II
Les macrophages, les lymphocytes B et les cellules dendritiques
sont capables de présenter un antigène aux lymphocytes T. Les
cellules dendritiques (CD) sont les cellules présentatrices pro-
fessionnelles du système immu n i t a i re et elles sont supposées être
les cellules présentant initialement l’antigène aux lymphocytes
T dans la PR (13). Dans la synoviale rhumatoïde,les CD sont
trouvées principalement au niveau des agrégats lymphocytaires
et en péri p h é rie des va i s s e a u x , s u gg é rant qu’elles proviennent du
sang périphérique. Les cellules présentant l’antigène expriment
à la surface de leur membrane des molécules HLA de classe II
qui sont indispensables au déclenchement d’une réponse immu-
n i t a i re médiée par les ly m p h o cytes T. Ces molécules ont une
s t r u c t u re dimérique composée de chaînes peptidiques αet β, ave c
un site de liaison pour les peptides antigéniques. Dans nos popu-
l at i o n s , la PR est associée aux allèles HLA D R B 1 * 0 4 0 1 ,
DRB1*0404, DRB1*0101. Les molécules HLA codées par ces
allèles se caractérisent par une séquence commune d’acides ami-
nés (QKRAA) située entre les positions 70 et 74 de la chaîne β
et qui correspond également au site impliqué dans la reconnais-
sance antigénique ( 1 4 ) . Cette séquence commu n e,é ga l e m e n t
appelée “épitope partagé”, pourrait être au cœur de la réaction
auto-immune médiée par les lymphocytes T. L’implication des
allèles HLA DRB1*04 et DRB1*01 dans la PR est éga l e m e n t
soulignée par l’association étroite entre ces allèles et la sévérité
de la maladie. L’allèle HLA DRB1*04 est pratiquement constam-
ment re t rouvé dans les PR agre s s ive s , avec des dégra d a t i o n s
o s t é o - a r t i c u l a i res plus précoces et plus importantes ( 1 5 ) . L e
nombre d’allèles à risque dans le génotype du patient est corrélé
avec la sévérité de la PR (16).
Lymphocytes B
Le rôle des lymphocytes B dans la PR est à nouveau envisagé
depuis les résultats des essais cliniques montrant l’efficacité du
ri t u x i m ab, un anticorps dirigé contre le marqueur CD20 des ly m-
phocytes B,responsable de la déplétion des lymphocytes B chez
les patients atteints de PR (17). Les lymphocytes B extraits de
la synoviale rhumatoïde expriment les marqueurs CD20, mais
pas CD38 (18). Ces lymphocytes B synoviaux ont conservé leur
c apacité à pro d u i re des immu n o g l o b ulines mais ils ont, e n
reva n ch e,p e rdu leur capacité de pro l i f é ration. Leur contri bu t i o n
dans la pat h ogénie de la PR se situe à plusieurs niveaux. Les
lymphocytes B peuvent se comporter comme de véritables cel-
lules présentatrices de l’antigène (CPA) car ils sont capables de
présenter des antigènes aux lymphocytes TCD4+ par l’intermé-
d i a i r e des molécules HLA de classe II ou des immu n og l o bu l i n e s
qu’ils expriment à leur membrane. Les lymphocytes B produi-
sent également des cytokines comme le TNFαou encore l’IL-
10 (19). Les lymphocytes B produisent aussi certains autoanti-
corps détectés dans la PR tels que les facteurs rhumatoïdes et
les anticorps antiprotéines citrullinées. La production de fac-
teur rhumatoïde par les lymphocytes B peut être induite par la
liaison entre le TLR9 et l’ADN bactérien ( 2 0 ) . Les anticorp s
dirigés contre des protéines citrullinées, produites par déimina-
tion de résidu arginine par une peptidylarginine déiminase, sont
très spécifiques de la PR (21).Les anticorps anti-CCP (citrulli-
nated cyclic peptide) reconnaissent également les résidus citrul-
linés de protéines comme la filagrine, le collagène ou la fibrine.
Le rôle phy s i o p a t h o l ogique de ces peptides citrullinés re s t e
maintenant à démontrer.
Le rôle des ly m p h o cyt es B a également été souligné par le modèle
K / B x N. Ces souris générées fo rtuitement développent sponta-
nément une art h rite directement liée à des anticorps dirigés contre
un antigène ubiquitaire : la glucose-6 phospho-isomérase (GPI).
Le transfert du sérum de ces souris induit en effet une arthrite
( 2 2 ) . Dans ce modèle ex p é r imental d’art h ri t e, les mastocytes sem-
blent jouer un rôle essentiel. Si l’effet pathogène des anticorps
anti-GPI est démontré dans ce modèle animal, ces anticorps ne
sont que rarement retrouvés dans la PR et ne sont pas spécifiques

La Lettre du Rhumatologue - n° 306 - novembre 2004
22
M
I S E A U P O I N T
de cette maladie. Ces anticorps anti-GPI sont plutôt observés dans
les PR associées à des signes extra-articulaires (23).
Lymphocytes T
Le rôle des lymphocytes T dans la PR est fortement suggéré par
l’abondance des lymphocytes Th1 dans la synoviale rhumatoïde
( 2 4 ) . Les ly m p h o cytes naïfs, après reconnaissance d’un anti-
gène, se différencient en lymphocytes T producteurs d’interfé-
ron γ(IFNγ), d’interleukine 2 (IL-2), ou encore d’IL-17. Cette
réponse est dite de type Th1, par opposition à une réponse “de
type Th2”, qui se traduit plutôt par une production d’IL-4. Ces
ly m p h o cytes T sont re c rutés à partir du sang péri p h é rique et s’or-
ganisent en agrégats qui ressemblent, par leur morphologie, à
l’architecture folliculaire des ganglions lymphoïdes. La plupart
des lymphocytes T synoviaux expriment à la fois les marqueurs
CD4 et CD45RO et sont donc des ly m p h o cytes T auxiliaire s
mémoires. Ces lymphocytes T peuvent être à nouveau activés
par les CPA par engagement des molécules du TCR (T cell re c ep-
t o r ),des molécules HLA D R , mais aussi des molécules de costi-
mulation comme CD28 et B7. L’activation des lymphocytes T
est sous le contrôle des lymphocytes T régulateursCD4+ et
CD25+. Ces ly m p h o cytes T régulat e u rs (T reg) sont cap abl e s
d’inhiber l’expansion clonale des ly m p h o cytes T CD4+. La
molécule C T L A 4 , ex p rimée sur les T reg 1 , i n t e ragit avec la pro-
téine CD28, exprimée sur les lymphocytes T CD4+, et induit un
message inhibiteur. Ces T reg pourraient intervenir dans la phy-
siopathologie de la PR (25). Une anomalie de la régulation des
lymphocytes T est démontrée dans un nouveau modèle murin
de PR. Des souris possédant une mutation du gène codant pour
la molécule de signalisation ZAP 70 développent spontanément
une art h rite qui re s s e m bl e,par plusieurs aspects,à la PR humaine
(26). Cette mu t ation favo ri s e rait anormalement une sélection
positive des lymphocytes T auto-immuns, qui ne devraient pas
survivre lors de son passage dans le thymus. Les lymphocytes
T sont capables d’interagir ensuite avec les cellules résidentes
comme les synoviocytes.
RÔLE DES SYNOVIOCYTES DANS LA PR
Les synoviocytes constituent le principal composant cellulaire
de la couche bordante de la membrane synoviale et sont de deux
types : les macrophages et les synoviocytes fibroblastiques. Les
p r e m i e rs ap p a r t i e n n e n t , comme les cellules dendri t i q u e s , à la
lignée monocytaire, tandis que les seconds ont plutôt une origine
mésenchymateuse. Les macrophages se distinguent des syno-
viocytes fibroblastiques par l’expression de marqueurs de diffé-
re n c i a tion tels que CD68 et CD14, des molécules HLA de
classe II et des récepteurs Fc des immunoglubulines. Les syno-
v i o c ytes m a c ro p h agi q u e s a c t i vés seraient les véri t ables moteurs
de la réaction inflammatoire en produisant deux types de média-
teurs : des médiateurs “primaires” ne nécessitant pas de synthèse
protéique tels que les prostaglandines, les leucotriènes, les radi-
caux libres et les enzymes contenus dans les granules et qui par-
ticipent de façon importante à la destruction tissulaire ; des média-
teurs “secondaires” requérant une synthèse protéique constituée
p rincipalement par les cytokines pro - i n fl a m m at o i res IL-1 et
T N F αqui induisent la synthèse de médiat e u rs “ p r i m a i re s ” d e
l’inflammation (PGE2, NO, radicaux libres) par une action auto-
c rine et para c r ine sur les cellules avoisinantes comme les
ch o n d ro cy t e s , les cellules endothéliales et les synov i o cyt es fi b r o-
blastiques. Ces dern i e rs produisent de nombreuses cytokines pro -
inflammatoires, parmi lesquelles l’IL-6, l’IL-8, l’IL-16, l’IL-18,
mais aussi des métalloprotéinases ( 2 7 ) . Les synov i o cytes ont une
c a pacité de pro l i f é rat ion qui re s s e m b le par certains aspects à celle
des cellules cancéreuses. Ils possèdent des caractéristiques qui
se rapprochent des cellules tumorales par leur morphologie, la
perte d’inhibition de contact, avec une capacité à adhérer,à enva-
hir et à détruire le cartilage, mais aussi par l’activation de plu-
s i e u r s oncogènes (27). La pro l i f é ration anormale des synov i o-
cytes de PR pourrait s’ex p l i q u e r, comme pour les tumeurs
c a n c é re u s e s , par un d é faut d’ap o p t o s e ( 2 8 ) . Les phénomènes
d ’ apo ptose sont en effet ra res dans la synoviale et pourra i e n t
résulter d’une surex p r ession de fa c t e u rs antiapoptotiques. L’ ap o p-
tose induite par le système Fas/FasL ne concerne qu’un pour-
centage limité de synoviocytes (20 %) et la majorité des cellules
sont résistantes à l’apoptose. Cette résistance des synoviocytes
pourrait donc résulter d’une surexpression de facteurs antiapop-
t o t i q u e s , qui restent à identifi e r. Dans les synov i o c ytes de PR
comme dans les cellules tumorales il existe une augmentation de
p l u s i e u r s pro t o - o n c ogènes tels que Bcl 2 , M y c,R a s , fos ou encore
phospho-inositide 3 kinase (PI-3 kinase). L’intérêt s’est donc
naturellement porté sur certains gènes suppresseurs des tumeurs
(tumor suppressor ge n e s ) , comme le gène codant pour la pro-
téine p53. Une mu t ation dans la séquence amino-acide de la
protéine p53, qui est observée dans certaines tumeurs, est éga-
lement trouvée dans les synoviocytes de PR. Cette mutation de
la protéine p53 contribuerait au prolongement de la durée de vie
des cellules.
VOIES INTRACELLULAIRES DE SIGNALISATION
IMPLIQUÉES DANS LA PR
Les connaissances physiopathologiques deviennent plus précises
avec le démembrement des mécanismes intracellulaires aboutis-
sant à l’activation des gènes (29). Lorsqu’un ligand se fixe sur son
récepteur membranaire, il provoque une modification de confor-
mation du récepteur qui aboutit à la phosphorylation du récepteur
lui-même ou d’une enzyme associée à ce récep t e u r. Cette pre-
mière phosphorylation entraîne l’activation en cascade d’autres
enzymes appelées les protéines kinases, qui activent à leur tour
les facteurs de transcription (figure 3, voir p. 25). Ces facteurs
de tra n s c r iption régulent la synthèse de protéines en agissant dire c-
tement sur le promoteur des gènes. L’activation des facteurs de
t ra n s c ription est induite par des protéines kinases qui ont une acti-
vité phosphorylante. Cette phosphorylation du facteur de trans-
cription permet sa translocation du cytoplasme vers le noyau ou,
e n c o r e,augmente son affinité pour l’ADN par ch a n g ement confo r-
mationnel. Les principales voies de signalisation impliquées dans
l’inflammation sont TRAF/IκBK/
NFκB, la voie des mitogen acti-
vated protein kinases (MAPK)/AP-1,
la voie de la phospho-inosi-
tide PI-3 kinase et la voie JAK/STAT. NFκB est activé lorsqu’il
est dissocié de IκB. La dissociation de ces deux molécules est
. . . / . . .

La Lettre du Rhumatologue - n° 306 - novembre 2004
25
M
I S E A U P O I N T
favorisée par la phosphorylation de IκB par la kinase IκB (IKK).
Pour les MAP kinases, il existe trois fa m i l l e s :p 3 8 , E r k1/2 et JNK.
Toutes les trois sont exprimées dans le tissu synovial des patients
atteints de PR. L’ a c t ivation de p38 induit la
synthèse des cy t o-
kines pro-inflammatoires comme le TNFα, l’IL-1,
l’IL-6 et l’IL-8
soit par activation directe de la transcription des gènes, soit par
stabilisation de l’ARNm. La p38 MAP kinase contrôle également
la synthèse d’autres molécules impliquées dans
l’inflammation,
comme les chimiokines et les molécules d’adhésion, mais aussi
dans la synthèse des métalloprotéinases re s p o n s abl e s
de la des-
truction cartilagineuse ou de la synthèse des prostaglandines. La
P I 3 kinase est une enzyme induisant la phosphory l ation de lipides
membranaires, phospho-inositides (PI). La PI 3 kinase est impli-
quée dans la prolifération et l’adhésion cellulaire, mais aussi
dans
l’apoptose et l’angiogenèse. Les facteurs de transcription, AP-1
et
NFκB, semblent particulièrement impliqués pour deux raisons.
Premièrement, ils sont surexprimés dans les synoviocytes extra-
its d’une synoviale rhumatoïde par rapport à ceux de la synoviale
d’arthrose et cette expression est corrélée à l’activité de la mala-
die. Deuxièmement, AP-1 et NFκB interviennent dans des voies
de signalisation qui contrôlent la synthèse de protéines part i c i-
pant à
l’inflammation de la synoviale et à la destruction articu-
laire.
NFκB et AP-1 régulent l’activation des gènes codant pour
les métalloprotéinases (MMP), mais aussi pour les cytokines pro -
inflammatoires, comme l’IL-6 et le TNFα,ou des médiateurs de
l ’ i n f l a m m a tion (pro s t ag l a n d i n e s ) , de l’angi ogenèse (VEGF, F G F,
ch i m i o k i n e s ) , et du re c rutement cellulaire dans la synov i a l e
(molécules d’adhésion et chimiokines). Ces molécules de signa-
lisation représentent de nouvelles cibles thérapeutiques dans le
traitement de la PR. Des inhibiteurs de p38 MAPK sont actuel-
lement en essai thérapeutique chez l’homme.
Figure 3. Lorsqu’une cytokine se fixe sur un récepteur membranaire, elle
provoque une modification de conformation du récepteur qui aboutit à la
p h o s p h o ry l atio n du récepteur lui-même ou d’une enzyme associée à ce
r é c e p t e u r. Cette pre m i è re phosphory l ation entraîne l’activation en cas-
cade d’autres enzymes appelées les protéines kinases, qui activent à leur
tour les facteurs de transcription.
MAPK = mitogen activated protein kinase ; PI 3K = phospho-inositide 3 kinase ; IKK =
I kappa B kinase ; NF
κ
B = nuclear factor kappa B ;AP-1 = activating protein 1 ; STAT =
signal transducer and activator of transcription ; RTK = récepteur des protéines tyrosines
kinases ; PK = protéine kinase ; ATP = adénosine triphosphate ;ADP = adénosine diphos -
phate ; P = phosphore; FT = facteur de transcription.
Figure 4. Immunopathologie de la PR.
La PR serait décl e n ché e au début par
une activation de l’immunité innée par les cel-
lules présentant l’antigène (cellules dendri-
t i q u e s , m a c r o p h ages ) qui favo r i s e rai ent le
recrutement des cellules impliquées dans l’in-
fl a m m a tion de la synov i a l e. Une réponse
immunitaire plus élaborée impliquant un anti-
gène présent dans l’art i c u l ation (pep t i d e s
c i t r ullinés?) et un terrain génétique part i c u-
lier (HLA DRB*04) induirait une réponse
immunitaire adaptée (Th1) avec une produc-
tion d’autoanticorps (anticorps anti-CCP, fa c-
teur rhumatoïde). Cette réponse immunitaire
se tra d u i rait par une réaction infl a m m a t o i re
avec libération de cytokines telles que le T N Fα
ou l’IL-1. Ces cytokines favoriseraient la pro-
duction d’autres cytokines impliquées dans
la destruction osseuse et cartilagineuse, mais
aussi la pro l i f é rati on des synov i o c ytes fi b ro-
blastiques. Ce pannus envahit et détruit le car-
tilage et l’os. Au cours de la PR, il existe des
possibilités d’intera c t ivation (soulignées par
les flèches bidirectionnelles) entre la réponse
immunitaire innée et adaptée qui favoriserait
la pérennisation de la maladie.
. . . / . . .
 6
6
1
/
6
100%