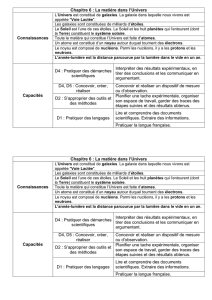
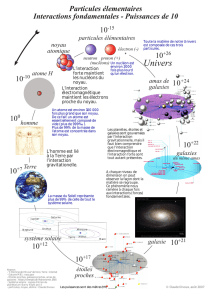
structure noyau l1s2

Pr. S.SECK
– GASSAMA
STRUCTURE DU NOYAU
ATOMIQUE

INTRODUCTION
Un atome est un ensemble électriquement
neutre avec en son centre un noyau autour
duquel gravitent des électrons.

STRUCTURE
Mise en évidence :
expérience de Rutherford : Bombardement
d’une feuille d’or avec des noyaux d’hélium

STRUCTURE
Interprétation :
structure lacunaire de l’atome
Présence de charges positives

STRUCTURE
Caractéristiques
Forme sphérique
Volume incompressible: 4/3pr3
r = 1,4 fermi (10-15m)
= m = m nucleons =
V 4/3pr3
1,67 10 – 27
4/3p (1,4 10-15 )3
= 230 10 15 Kg / m3
230 millions tonnes / cm3
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
1
/
21
100%