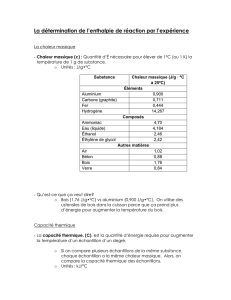
Capacité thermique massique d`un polyéthylène On se propose de

Avant toute mesure, il est indispensable de connaître la capacité thermique du calorimètre et de
ses accessoires. On doit donc déterminer cette capacité thermique (notée) Cc dans des conditions
aussi proches que possible de l'expérience. Pour cela :
On a placé une masse de 200 g d'eau dans le calorimètre.
On a mesuré la température que l’on a trouvée égale à 15 °C.
On a alimenté la résistance chauffante pendant 5 minutes.
On a mesuré la température atteinte par l’eau, que l’on a trouvée égale à 20°C.
Capacité thermique massique de l’eau : 4,18 J.g-1.K-1
On se propose de mesurer la capacité thermique
massique d'un polyéthylène.
L'appareil de mesure utilisé est un calorimètre qui
fonctionne à pression constante.
La mesure de la température se fait avec un
thermomètre à dilatation assez long.
Le chauffage dans l’enceinte du calorimètre est
réalisé à partir d’une résistance électrique.
Le système est parfaitement isolé.
Détermination de la capacité thermique massique du polyéthylène :
On a placé une masse de 500 g de polyéthylène dans le calorimètre. On a ajouté une quantité
d’eau de masse 250g. La mesure de la température initiale a donnée θi = 15 °C. Après un apport
d'énergie par la résistance de chauffage, qui a fonctionnée pendant 25 minutes ; on a mesuré une
température à l'intérieur du calorimètre θf = 25 °C.
La résistance électrique a une valeur de 38,4 et est alimentée en 24 V.
Le volume utile du calorimètre est de 1 l.
Si l’on utilise la résistance électrique de chauffage, celle-ci doit être immergée.
Résistance de
chauffage
Echantillon
Thermomètre
Enceinte isolée.
Document 1 : Le calorimètre.
Le calorimètre est un système thermodynamique isolé qui ne peut échanger aucune énergie avec
le milieu extérieur (ni travail, ni chaleur). Sa paroi est indéformable et adiabatique. Donc W = 0 et
Q = 0 ( si il n’y a pas de système de chauffage ou de réfrigération ). Il y a des transferts de chaleur
( à l’intérieur ) entre les différentes parties du calorimètre : substances étudiées, accessoires,
paroi….
Si il n'y a aucun échange de chaleur avec l'extérieur, cela implique que la somme des chaleurs
échangées Qi au sein du calorimètre est nulle. On écrira ∑ Qi = 0.
Si il y a apport de d’énergie par l’extérieur, cela implique que la somme des chaleurs échangées
Qi au sein du calorimètre est égale à la chaleur ( énergie ) amenée par l’extérieur Qext. On écrira
alors : ∑ Qi = Qext
Capacité thermique massique d’un polyéthylène

Document 6 : Le Kelvin (échelle utilisée en thermodynamique pour les températures).
Cette échelle est basée sur la dilatation des gaz parfaits. Elle part du zéro absolu. Un intervalle
de température de 1K correspond à un intervalle de 1°C.
Si l’on nomme T la température en Kelvin et la température en degré Celsius on écrit :
273,15Tθ
Document 5 : Relation énergie E, puissance P et temps t.
Cette relation s’écrit :
P.tE
s
W
J
Document 4 : Alimentation d’une résistance en courant continu.
La relation entre la tension et le courant dans une résistance :
La relation donnant la puissance P dans une résistance R parcourue par un courant électrique
d’intensité I s’écrit :
R.IU
A
V
R.I²P
W
A
Document 3 : Changement de température d’une substance en fonction de la chaleur.
La chaleur Q en J reçue par un corps pur de masse m dont la température varie se calcule par la
relation : Q = m C ( Tf - Ti )
m : masse du corps en g si C est en J.°C-1.g-1 :
Ti : température initiale du corps en °C Tf : température finale du corps en °C
C : capacité thermique massique du corps J.°C-1.g-1 :
Document 2 : La capacité thermique.
La capacité thermique (ou capacité calorifique) d'un corps est une grandeur permettant de
quantifier la possibilité qu'a un corps d'absorber ou de restituer de l'énergie par échange
thermique au cours d'une transformation pendant laquelle sa température varie. La capacité
thermique est l'énergie qu'il faut apporter à un corps pour augmenter sa température d'un kelvin.
Elle s'exprime en joule par kelvin (J/K).
Capacité thermique massique de l’eau : 4185 J.Kg-1. K-1
Travail demandé :
On fournit la même quantité de chaleur à deux échantillons de masses identiques, l'un en
polyéthylène et l'autre en acier.
Déterminer l'échantillon dont la température s'élèvera le plus.
Donnée : capacité thermique massique de l'acier: Ca = 0,45 kJ.kg-1.K-1.
1
/
2
100%