Document 6 : Dépistage de la drépanocytose

DREPANOCYTOSE
Document 1 : les symptômes associés à la drépanocytose
La drépanocytose, également appelée anémie
falciforme, est une maladie génétique très courante en
particulier en Afrique et en Inde. Elle toucherait plus de 50
millions de personnes, ce qui en fait la première maladie
génétique au monde. Cette maladie est provoquée par une
mutation sur le gène de la β-globine qui est présent sur le
chromosome 11.
Les individus atteints de drépanocytose
présentent des symptômes caractéristiques, notamment
un essoufflement chronique, des palpitations cardiaques et
leurs lèvres présentent une couleur bleutée. Au niveau
tissulaire, les capillaires sanguins sont souvent obstrués par
des globules rouges, ce qui provoque des accidents vasculaires. Ces accidents provoquent des lésions tissulaires
au niveau des muscles, du foie, des poumons, des os … Ces lésions s’accompagnent de douleurs. On constate
également que les individus malades sont très fortement anémiés, ce qui nécessite régulièrement des
perfusions.
Document 2 : Défauts cellulaires de la drépanocytose
Les globules
rouges (hématies) des
sujets sains ont une
forme biconcave et sont
souples (a). Malgré leur
taille de 8µm, elles
peuvent se tordre afin de
passer dans des
capillaires de 2 µm. A
l’inverse, les sujets
atteints de
drépanocytose présentent une forme de faucille (Sickle en anglais) et sont très peu déformables et cassantes
(b). Ces hématies ont une durée de vie plus faible et transportent difficilement le dioxygène
Document 3 : Séquences nucléotidiques et peptidiques des β-globines (individu sain en haut,
drépanocytaire en bas)

Document 4 : Défauts moléculaires de la drépanocytose
Document 5 : La transmission de la drépanocytose
L’arbre généalogique montre les relations entre les membres de la famille (rond = femme, carré =
homme ; losange = enfant à naître). Le couple 5 et 5’ se demandent si leur enfant (7) est malade. Au moyen du
document 4, vous préciserez si l’enfant est malade.
1
2
3
4
6
5
5’
7
?

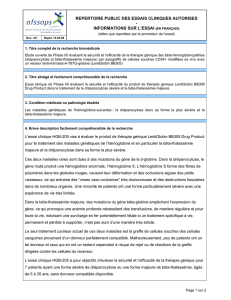
Document 6 : Dépistage de la drépanocytose
La drépanocytose peut être dépistée par électrophorèse. Cette méthode permet de séparer les
molécules HbA et les dimères HbS (qui migrent moins loin).
Document 7 : La thérapie génique des hémoglobinopathies
En 2001, un travail franco-américain publié dans la prestigieuse revue « Science » montre que des souris
génétiquement modifiées pour accueillir le gène « normal » de la β globine retrouvent un phénotype normal. En particulier,
les tissus tels que le foie, les reins et les poumons sont alors normaux (Pawliuk et al.Science 2001;294:2368-71).
En 2005, le promoteur Genetix France a soumis à l’Afssaps une demande d’autorisation d’essai clinique de
thérapie génique. Après évaluation par le groupe d’experts sur les recherches biomédicales en thérapie génique, l’Afssaps a
autorisé l’essai en décembre 2005. Cet essai consiste à évaluer la sécurité et l’efficacité d’une stratégie de thérapie génique
chez 10 patients. Ceux-ci doivent présenter une forme sévère de drépanocytose, être âgés de 5 à 35 ans, et ne pas avoir de
donneur de moelle compatible.
La stratégie thérapeutique repose sur le transfert de gène ex-vivo. Le gène normal de la protéine déficiente est
intégré au moyen d’un vecteur dans les cellules souches issues de la moelle osseuse des patients. Ce transfert de gène a
pour objectif de faire exprimer aux globules rouges la protéine normale (la b-globine). Le vecteur utilisé est issu d’un
lentivirus modifié dans lequel a été inséré le gène de la b-globine.
Les cellules souches de la moelle osseuse des patients sont prélevées sous anesthésie générale, purifiées, mises
en contact avec le vecteur lentiviral pour le transfert de gènes, puis ré-administrées au patient par voie intraveineuse.
[Source : http://www.inserm.fr/espace-journalistes/premier-succes-d-un-essai-clinique-en-therapie-genique-pour-la-v-thalassemie]
1
2
3
4
7
-
+
départ
membres de
la famille
1
/
3
100%