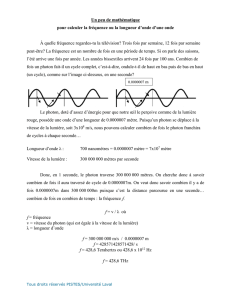
Thème III : La lumière

- 1 -
Thème III : La lumière
Le rayonnement lumineux :
La lumière est une onde transversale de direction de vibration perpendiculaire à
la direction de propagation. MAIS sans direction de vibration privilégiée
(direction aléatoire).
La polarisation est la sélection d’une direction de vibration.
Une onde lumineuse est une onde électromagnétique
= combinaison d’un champ magnétique et d’un champ
électrique qui s’auto entretiennent mutuellement.
400nm 700nm
Rayon Gamma : rayonnement émis par la désintégration des noyaux.
Rayon X : découvert par Röntgen, produit de la transition électronique des e-
entre les différents niveaux d’énergie.
Rayonnement ultraviolet : il est à l’origine du bronzage et permet la synthèse de
la vitamine D mais il provoque des cancers de la peau.
Rayonnement visible : il est produit par les transitions des e- entre les
différents niveaux d’énergie et il impressionne la rétine.
Rayonnement infrarouge : il fait ressentir la chaleur car il a une longueur d’onde
proche de la fréquence de rotation des molécules. Son énergie est donc
transformée en chaleur.
Micro-ondes : ce sont des ondes de f= 2450 Hz qui sont produites en faisant
osciller des e-. Les molécules polaires sont mises en rotation par l’énergie de ces
ondes, les chocs entres les molécules dégagent alors de la chaleur (micro-ondes).
Effet photoélectrique :
La lumière arrache des e- au métal et induit ainsi un courant électrique.
Son intensité varie en fonction de : 1° l’intensité de la lumière.
2° la fréquence de la lumière (couleur)
Il existe une fréquence seuil (fs) qui varie en fonction du métal. Si f fs
alors il n’y a pas de courant.
Einstein :
Einstein propose la théorie des quanta d’énergie appelés photon.

- 2 -
La lumière est composée de quantités discrètes, de particules d’énergie
appelées photons. Chacun de ces photons a une énergie qui dépend de la
fréquence de la lumière : E=hf
W est le travail d’extraction de l’e- par le photon incident:
1. Si h.f=E W alors : pas de courant
2. Si h.f = W alors l’e- est arraché mais il n’y a plus d’énergie pour le
lancer dans le circuit donc il n’y a pas de courant
3. Si h.f W alors l’énergie E du photon est « divisée » entre l’énergie
d’extraction de l’e- et l’énergie cinétique de l’e- dans le circuit.
2².
.vm
wfh
Remarques: - La constante de Planck = 6,63.10-34 J.S
- Un photoélectron = un e- arraché par un photon
- Un eV (électronvolt) = 1 ,6.10-19 J
= énergie cinétique acquise par un e-
lorsqu’il est accéléré par une DDP de 1
Volt.
Emission de lumière par les atomes : théorie de Bohr
Quantité de mouvement d’un objet = grandeur physique qui est le produit entre
la masse de l’objet et la vitesse de celui-ci.
n = nombre quantique principal et correspond à l’orbitale de l’e-.
1
².
..4²... ²². rn
meZk hn
r
e
n
²²
1
.
²²..4.².².
.
211
4
n
E
nh meZk
Ee
n
Où Z=n° atomique de l’élément
me=masse de l’e-=9,1.10-31 kg
e=charge de l’e-

- 3 -
Avec r1= 0,053 nm POUR l’hydrogène
E1 = -13,6 eV
Remarque :
1. pour trouver le rayon d’une orbitale d’un élément a qcq :
a
h
az
r
r
1
pour trouver l’énergie d’une orbitale d’un élément a qcq :
h
a
aEZE .
2
1
2. pour calculer la vitesse d’un e- (à partir de la formule de la quantité de
mouvement) :
nne rvmhn ..2...
ne
nrm hn
v..2. .
3. l’atome ne dégage de la lumière que si l’e- passe d’une orbite permise à une
autre orbite permise. Et ce, si l’orbite d’arrivée est – énergétique que
l’orbite de départ. Alors h.f = En’ - En
4. La couleur du rayonnement est définie dans 3 spectres : Lyman (pour
l’infrarouge), Balmer (pour la lumière visible) et Paschen (pour les UV).
Mécanique ondulatoire :
1. On considère la lumière comme un ensemble de corpuscules ET comme une
onde.
C’est la dualité onde- corpuscules.
Ondulatoire car : - se réfracte,
- crée des interférences,
- est diffractée,
- est polarisable.
Corpusculaire car: - est à l’origine de l’effet photoélectrique,
- est à l’origine de l’émission de lumière par les atomes.
2. Le photon comme particule probabiliste :
Le photon a un comportement probabiliste car il n’est pas possible de prévoir le
comportement d’UN photon mais il est possible de prévoir les différents
endroits où arrivent beaucoup de photons.

- 4 -
Le lien onde-photon est donné par une propriété :
La probabilité de détecter un photon à un endroit précis de l’écran est
directement proportionnelle au carré de l’amplitude de l’onde à cet endroit.
Hypothèse de Broglie :
Broglie va généraliser à tout l’univers la mécanique ondulatoire :
Toute matière en mouvement a une onde qui lui est associée.
Avec :
vm
h
.
Où h= cst de Planck
m.v= quantité de mouvement de l’objet (kg.m/s)
Cette hypothèse sera vérifiée en 1925 lorsque l’on observa la diffraction d’un faisceau d’e- dans
un cristal.
En conclusion :
Les particules en mouvement ont un comportement à la fois ondulatoire (f et )
et probabiliste en ce qui concerne le niveau corpusculaire.
P.exp : Le photon avec un comportement
Ondulatoire : caractérisé par T, f, avec f=1/T
Cmh
.
Corpusculaire : caractérisé par E, P (quantité de mvt) avec E = f.h
P = m.v
Les visions corpusculaire et ondulatoire du photon se complètent. C’est le
principe de complémentarité : E.T = P. = h
Corpuscule onde corpuscule onde
Application de la mécanique ondulatoire au modèle de Bohr :
Les e- ne sont pas sur une orbite bien définie mais dans un nuage électronique
dans lequel la probabilité de trouver l’e- est la + grande. = densité de probabilité
de présence.

- 5 -
Le principe des incertitudes :
Broglie : = h/m.v
Pour connaître une particule, il faut l’observer avec un photon et grâce à un
microscope. MAIS si on prend un photon qui a une très petite (pour éviter la
diffraction due à la particule et pour localiser la particule très précisément) sa
fréquence sera très grande (car 1/f). Or, un photon qui a une grande
fréquence aura une grande énergie. Et il va transférer son énergie à la particule
qu’il observe, mais cette énergie va faire varier la vitesse de la particule.
A l’inverse, si on prend un photon qui a une grande, alors la diffraction nous
empêchera de connaître la position de la particule avec précision mais on
connaîtra sa vitesse (en effet, celle-ci ne sera que peu modifiée par l’énergie du
photon).
En conclusion, à cause de ces 2 paramètres qui varient simultanément, il est
impossible de connaître la position d’une particule et sa quantité de mouvement
au même instant et avec une précision suffisante. C’est le principe des
incertitudes d’Heisenberg.
1
/
5
100%