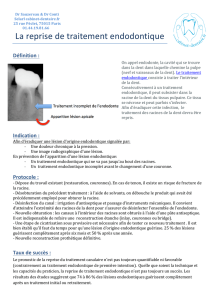
Etude ultrastructurale de l`interface matériaux de coiffage

/1
1
Combattre le mal à la racine : l’endodontie moderne
Y.HAIKEL
Introduction
La thérapeutique pulpaire est l’ultime recours pour pouvoir
conserver une dent sur l’arcade. L’étiologie la plus commune
est la carie dentaire. L’alternative au traitement est l’implant
dentaire mais cette solution n’est pas satisfaisante, n’est pas
toujours possible, ne remplacera jamais l’organe dentaire dans
toutes ses fonctions, n’aura jamais la même pérennité qu’une
dent naturelle et restera un recours lorsque la dent est
absente !
Dans un premier temps, la réalisation d’un diagnostic s’impose
pour envisager le traitement le plus conservateur, autrement
dit, on s’inscrit dans un gradient thérapeutique du moins invasif
et plus conservateur vers des traitement plus complexes
Diagnostic des pulpopathies
Les pulpopathies répondent d’une inflammation ou d’une
nécrose des tissus pulpaires (Figure 2). La démarche diagnostic
repose sur l’anamnèse médicale et dentaire complétée par
l’analyse des symptômes puis des signes cliniques par différents
moyens : l’examen visuel des surfaces dentaires, gingivales et
muqueuses, la palpation, les tests de vitalité pulpaire, le
sondage parodontal, les tests de percussion, l’évaluation de la
mobilité dentaire et l’examen radiologique (Tableau 1, Figure
3). De nouveaux outils de diagnostic sont développés tels que
des tests de la vitalité pulpaire reposant sur l’échographie
doppler.
Le diagnostic de certaines complications de nécrose pulpaire
peut être difficile de part le hiatus pouvant exister entre les
symptômes locaux et les signes généraux. Ainsi certaines
nécroses pulpaires asymptomatiques localement peuvent être
la cause de signes généraux d’infection inquiétants
(augmentation de la vitesse de sédimentation, de la NFS des
leucocytes, fièvre) et de risques d’accidents corono-
vasculaires sans que le diagnostic de pulpopathie n’ait été
envisagé.
Une meilleure connaissance de la biologie et de la pathologie
pulpaire permet actuellement d’adopter des thérapeutiques
plus conservatrices. En effet, la pulpe est un tissu capable de
se défendre et de cicatriser lorsqu’elle est placée dans des
conditions favorables.
Le coiffage pulpaire direct constitue une des attitudes
thérapeutiques de choix des dents pulpées dénudées

/2
2
accidentellement ou suite à une lésion carieuse ayant induit
une inflammation pulpaire réversible.
L’intérêt de la conservation de la pulpe vivante, en plus de
l’aspect résistance mécanique et qualités esthétiques, c est la
possibilité de maintenir une vascularisation normale qui permet
aux odontoblastes d’assurer le rôle de dentinogénèse
réparatrice et primaire d’édification apicale des dents
immatures. Le principe du traitement découle des potentiels
de cicatrisation de la dentine qui conduit à la formation d’un
pont tissulaire calcifié par néoformation dentinaire. L’indication
des coiffages pulpaires directs doit être basée sur un
diagnostic aussi précis que possible de l’état pulpaire. Cette
thérapeutique ne s’applique qu’à une pulpe atteinte de façon
réversible et de préférence en présence d’une dent
monoradiculée jeune.
Le succès clinique va dépendre essentiellement de l’indication
appropriée, de la technique opératoire exigeant une aseptie
stricte avec un scellement coronaire hermétique et du choix
du produit de coiffage pulpaire.
Le choix du produit de coiffage pulpaire est fonction de sa
biocompatibilité et de ses capacités d’induire ou de favoriser
la formation du pont dentinaire ou de permettre d’assurer
l’étanchéité.
Infection endodontique et assainissement canalaire
L’objectif du traitement endodontique est de rendre la dent
affectée au niveau pulpaire, biologiquement acceptable par
l’organisme. Il constitue donc l’ultime recours pour le maintien
de la dent sur l’arcade. Ces dernières années, le progrès
technologique a fait beaucoup évoluer l’endodontie en
termes de mise en forme, de matériaux endodontiques, de
techniques d’obturation mais il ne faut pas oublier que la
désinfection et l’assainissement canalaires sont toujours les
points cruciaux de toute thérapeutique endodontique.
Plusieurs voies de contamination bactérienne peuvent être à
l’origine des pulpopathies : les lésions carieuses ou d’usures, les
poches parodontales qui exposent les canaux latéraux et
accessoires le long de la racine ou au niveau de la furcation,
les microfissures, les fêlures, les traumatismes exposant la pulpe,
les matériaux non étanches ou non biocompatibles. C’est
pourquoi les flores endodontiques et parodontales sont très
proches. Les trois bactéries suivantes sont présentes dans 90 %
des infections endodontiques: Bacteroides forsythus,
Campylobacter showae et Fusobacterium nucleatum vicentii.
A partir de ces voies, c’est tout le réseau endodontique qui va
être rapidement colonisé de part sa complexité et de part la

/3
3
perméabilité de la dentine. En effet, les canalicules dentinaires
d’environ 2µm de diamètre constituent de nombreuses voies
pour la diffusion de l’infection endodontique : 45 000 / mm2 de
dentine. Ainsi, lors de l’infection endodontique, les micro-
organismes se trouvent aussi bien dans le canal principal que
dans les canaux latéraux, secondaires et dans tous les
canalicules dentinaires (Figure 1). Les particularités de la région
apicale rendent l’infection apicale encore plus complexe :
isthme, déviation du cône cémentaire, paquet vasculo-
nerveux, stimulation des immunoglobulines E, interfaces avec
les tissus parodontaux.
Lors du traitement endodontique, l’action mécanique
conjuguée à l’action chimique de désinfection de part cette
complexité anatomique, reste toujours limitée aux zones
mécaniquement accessibles. Il est donc plus juste de parler
d’assainissement canalaire que de désinfection.
L’agent d’irrigation de référence pour cette action chimique
est l’hypochlorite de sodium (NaOCl) à 2,5 à 5 % dont
l’efficacité est majorée par l’agitation (vibrations mécaniques
ou US) et par l’augmentation de la température (37°- 40°C) :
actions anti-bactérienne, anti-fongique et solvante de la
substance organique. Son optimisation se fait également par
l’augmentation du temps de contact, du flux, du diamètre
canalaire, par l’utilisation d’irrigants complémentaires comme
l’EDTA ayant une action sur la phase minérale et d’aiguilles
adaptées. L’action de la solution a une action limitée à
environ 2 mm au-delà de l’extrémité de l’aiguille de la seringue
d’irrigation.
L’action mécanique est réalisée par les instruments
endodontiques. Il a été démontré que la rotation continue
n’apporte pas d’avantage en termes de désinfection
comparativement à l’instrumentation manuelle. En effet, 35%
de la surface endodontique n’est pas en contact de
l’instrument endodontique qu’il soit manuel ou rotatif. De
même, les études microbiologiques montrent qu’il n’y a pas de
différences entre les techniques manuelles et la rotation
continue NiTi dans leur habilité à réduire les bactéries
intracanalaires]. De plus, l’incidence des ruptures
instrumentales est plus importante en utilisant l’instrumentation
rotative que l’instrumentation manuelle, ce qui peut
compromettre considérablement la qualité de l’assainissement
canalaire final.
Parallèlement à la rotation continue, s’est développée toute
une instrumentation ultrasonique endodontique. Cependant, il
n’existe pas aujourd’hui de preuves appuyant l’intérêt de
l’utilisation des ultrasons seuls ou associés à l’instrumentation

/4
4
manuelle, pour améliorer le nettoyage et la mise en forme
canalaires.
Par contre, ces instruments sont très utiles lors de l’irrigation de
pré-obturation. En effet, un rinçage final avec une solution
d’hypochlorite de sodium agitée par les US va permettre
d’augmenter son action et donc l’assainissement final sur
l’ensemble de l’endodonte préparé et prêt à être scellé.
Décisions thérapeutiques endodontiques
Le traitement de l’urgence des pulpopathies a pour but de
soulager le patient par la suppression de la douleur. Ainsi face
à une pulpite aigue, le traitement consistera en la
décongestion vasculaire grâce à l’ouverture de chambre
pulpaire et face à une complication de nécrose pulpaire (AAA
et AR) (Figure 4 et 5) en la réalisation d’une voie de drainage
transcanalaire ou/et transmuqueuse (abcès localisé et
circonscrit).
La prescription médicamenteuse en endodontie est
facultative. L’antibiothérapie est sans avantage par rapport au
drainage. Cependant, des antibiotiques et des anti-
inflammatoires non stéroïdiens sont à prescrire dans ces trois
situations précises : quand le drainage est impossible (infection
diffuse), en présence de complications systémiques ou d’un
patient à haut risque médical. Il n’y a pas de donnée
probante concernant l’utilisation d’un type d’antibiotique par
rapport à l’autre. Quelques soient le diagnostic et la
prescription effectués, la dent ne doit jamais être laissée
ouverte, au risque notamment de rendre l’infection
endodontique plus complexe et virulente.
Si l’obturation canalaire ne peut pas se faire dans la même
séance, l’obturation à l’hydroxyde de calcium est indiquée en
inter-séance. Cette médication canalaire au pH basique
possède de nombreuses propriétés notamment anti-
bactériennes mais s’avère inefficace contre les germes
suivants : Actinobacillus actinomycetem comitans,
Capnocytophaga sputigena, Eikenella corrodens. Dans tous
les cas, il permet de ne pas laisser le canal vide entre deux
séances.
Le traitement étiologique des pulpopathies a pour objectifs
l’élimination de tout le contenu du système canalaire et le
scellement tridimensionnel et hermétique de celui-ci, l’isolant
du reste de l’organisme. Il doit être réalisé le plus rapidement et
si possible dans la même séance quelle que soit la
symptomatologie, à condition que le canal soit cliniquement
propre, inodore et sec (Figure 5). Si ces conditions locales sont

/5
5
présentes, il n’est pas indispensable d’attendre la disparition
des symptômes et des signes locaux et/ou généraux.
Pronostic endodontique
Les critères retenus pour évaluer le résultat des traitements
endodontiques sont cliniques et radiologiques : absence de
douleur et de tuméfaction, disparition de la fistule,
fonctionnalité de la dent, absence de signes radiologiques de
destruction tissulaire, arrêt ou disparition totale radiologique de
la raréfaction osseuse (Figure 5b). Si bien que le résultat du
traitement endodontique peut être qualifié après une période
d’observation de 6 à 24 mois.
Selon des études menées en France, 23 % des racines sont
traitées endodontiquement et seulement 21% des ces
traitements sont acceptables radiologiquement (longueur et
densité); la prévalence des lésions apicales sur les dents
traitées endodontiquement est de 33% (Figure 5a).Le
pourcentage de dents présentant une parodontite apicale
augmente avec l’âge et proportionnellement au pourcentage
de dent traitées endodontiquement. Le fait que le premier
facteur associé à la présence de ces lésions soit l’existence de
traitements endodontiques montre que ceux-ci sont encore
trop iatrogènes. Certains facteurs sont absolument non
significatifs pour le succès du traitement endodontique : l’âge,
le sexe, l’état général du patient, le choix de la technique ou
du matériau d’obturation. De même, le traitement
endodontique est non opérateur-dépendant. D’autres
facteurs sont significatifs et soulignent l’importance du facteur
microbiologique : présence d’une pathologie péri-apicale pré-
opératoire, bactériologie canalaire initiale, anatomie et
configuration canalaires, sur-instrumentation et niveau
d’obturation canalaire, étanchéité de la restauration
coronaire per ou post-opératoire. Dans 14,5 % des échecs
endodontiques, les causes suivantes sont retrouvées : une
perforation, une défaillance de l’obturation canalaire, une sur-
instrumentation ou une fracture instrumentale. L’oubli d’un
canal est absolument déterminant et explique 49% des échecs
(POOR PAST].
Conclusions
Bien que l’endodontie ait intégré de nombreux progrès
technologiques, les traitements endodontiques sont encore
trop iatrogènes. Des perspectives d’avenir apparaissent avec
les cellules souches et la régénération pulpaire. Lors de la
présentation, seront abordés les différents progrès réalisés ces
 6
6
 7
7
 8
8
 9
9
1
/
9
100%