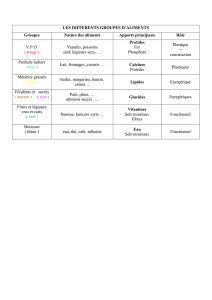
Les évaporites (roches salines)

Les évaporites (roches salines)
Les roches salines naissent de processus chimiques, qui se réalisent dans des conditions voisines de la
normale. La condensation à l’air libre de gaz volcaniques en efflorescences, c’est-à-dire en transformation,
constitue un mode de genèse des roches salines très particulier. Dans tous les autres cas, celle-ci, tout
comme les dépôts réalisés artificiellement dans les salins, résultent d’une cristallisation aux dépens de
solutions aqueuses. Les sels précipitent dans des nappes d’eau, pour sédimenter en séquences stratifiées.
L’étude des séries naturelles permet d’affirmer l’importance du fait sédimentaire, mais les facteurs de la
précipitation sont variés et la diagénèse (transformation progressive d’un sédiment en roche) des dépôts est
précoce. C’est pourquoi, il est préférable pour désigner les roches salines, d’éviter le terme « évaporites »,
qui n’implique que le processus évaporatoire.
La sédimentation des sels obéit à des lois simples, car les facteurs biologiques restent ici modestes. Les
dépôts qu’elle a fournis sont des indices précieux dans les essais de reconstitution des paysages passés. Ils
jouent aussi un rôle important en tectonique et en géologie pétrolière comme couverture de gisements,
facteur de piégeage, indice d’un environnement favorable à la formation des hydrocarbures. Les sels
correspondants présentent, en outre, un intérêt majeur pour l’industrie, avec la fabrication du plâtre,
l’extraction de la halite (sel gemme : chlorure de sodium), et à la production des engrais potassiques.
I/Conditions générales de formation
1. Précipitation des sels et séquences salines :
La précipitation d’un sel s’effectue, lorsque le produit des concentrations de ses composés ioniques atteint
une valeur limite, appelée produit de solubilité qui dépend de la température comme de la pression.
Les processus sont variés, mais toujours plus ou moins associés :
Introduction d’ions nouveaux qui permettent la cristallisation de sels de faible solubilité
Addition de nouveaux ions semblables à ceux qui sont déjà présents
Changements de température
Extraction du solvant
Ce dernier facteur, correspond à l’évaporation des saumures (eau fortement salée dont on extrait le sel par
évaporation), dont la concentration doit atteindre une valeur telle que, les autres facteurs puissent
intervenir.
Lorsqu’un sel précipite, le chimisme de la solution évolue : un autre sel pourra précipiter en constituant le
second terme d’une séquence. Les successions les plus simples se réalisent alors, quand les apports en ions
sont négligeables par rapport au stock piégé dans le bassin. Mais ceci est exceptionnel de trouver de tels
bassins qui correspondent à ce cas idéal, car les apports varient en fonction du climat, et dépendent de la
nature, du chimisme et de la position des tributaires (cours d’eau qui se jette dans la mer) du bassin.
Les dépôts salins les plus communs sont fournis, de nos jours, par des dépressions continentales de faible
portée. Mais on connaît des gisements, estimés à plusieurs centaines de milliers de kilomètres cubes,
occupant des plates-formes, dépourvues d’affleurements (roche constituant le sous-sol se retrouve à la
surface) salins plus anciens, qui étaient susceptibles de les avoir alimentés. Seule une évaporation d’eaux,
d’origine marine, peut expliquer leur présence. On est donc conduit, à choisir comme modèle de séquence
saline, celle qui résulte de l’évaporation de solutions, ayant la composition ionique de l’eau de mer.
2. Sels obtenus par évaporation de l’eau de mer :
La figure 1 schématise le modèle de l’évaporation, à 25° C, d’une colonne d’eau de mer pour que 100m de
chlorure de sodium (halite : sel gemme), se déposent au-dessus de quelques décimètres de carbonates, et de
4,8m de gypse. Pour obtenir ces épaisseurs, il faudrait évaporer une épaisseur de 8,5km d’eau de mer, ce qui
parait peut probable, et empêche la réalisation d’un tel modèle.

Pour une température donnée, la séquence varie par conséquent suivant la stabilité des précipités, et en
fonction des possibilités de réactions entre dépôts. Dans les conditions naturelles, ces réactions sont en

général possibles, et la séquence type des sels d’origine marine, devrait correspondre, après un début de
diagénèse (transformation progressive d’un sédiment en roche), à la colonne b. Au-dessus de 100m de sel
gemme (chlorure de sodium), on rencontrera donc de bas en haut : 7,5m d’un mélange halite-kiésérite ;
23m d’un mélange halite-kiésérite-carnallite ; et 24,5m de bischofite avec des traces des sels précédents.
La figure 2 reproduit diverses séquences obtenues, par évaporation statique d’eau de mer, à des
températures variées. Il convient de noter que la silvine n’apparait qu’aux basses températures, et elle ne
peut se former, qu’à partir d’eaux plus pauvres en magnésium et en sulfate.


II/Principales catégories
1. Les dépôts salins paralique (désigne une zone littorale qui est en contact avec la mer par une
communication étroite)
Les exemples de ces dépôts salins sont toujours limités à des zones restreintes sous climat aride. Le déficit
en au douce est composé, par un apport continu d’eaux marines, et les dépôts correspondent aux sels
fournis par l’eau de mer. Le voisinage du continent peut néanmoins perturber les rapports volumiques entre
sels déposés, car interviennent les cours d’eau, qui importent des ions d’origine continentales. En bordure
des bassins, les dépôts carbonatés s’organisent en associations complexes : outre la présence d’aragonite et
de calcite, la dolomite est fréquente, mais aussi les carbonates magnésiens. Les apports de sulfates
provoquent, dans des eaux sur salées, la formation de sels multiples, dont la poly halite qui, en général
remplace le gypse par épigénèse (remplacement lent d'un minéral par un autre dans une roche).
En fait, ces modèles actuels sont rares. On peut trouver la sebkha côtières du golfe Persique ou des côtes
sud-orientales de la méditerranée (sebkha el Mellah de Zaria en Tunisie), les lacunes de la Californie
mexicaine, Boucana de Virola au Pérou, et les côtes de l’Australie.
Les grands gisements fossiles ne peuvent s'expliquer que par, la dominance des apports d'eau marine:
seule l'étude paléogéographique (discipline de paléontologie dont l'objet est la reconstitution théorique de
la géographie passée des territoires) de ces bassins permet d'imaginer les modèles théoriques de genèse.
Pour qu'un bassin paralique dépose des sels en grande quantité, deux conditions sont nécessaires :
L'évaporation est supérieure aux apports d'eau, qui viennent des pluies et des fleuves voisins, le
déficit étant compensé par des apports d'eau salée, qui vient d'un océan voisin (ou mer).
Les saumures sont piégées, au moins en partie, dans le bassin. La communication entre le bassin
salin et la mer doit être restreinte, car les solutions peuvent migrer vers la mer par un courant. Cela
a donc conduit à la notion de barrière, pour empêcher ces migrations.
Il apparaît alors que, les conditions idéales sont sous un climat aride, dans un bassin, qui était
anciennement une terre continentale, qui a été envahie par l'océan, faiblement ouvert sur l'océan.
Le facteur climatique, et la configuration du bassin interfèrent dans la création de ces sels. Dans certains
cas, il y a un équilibre, ce qui peut bloquer le chimisme du bassin dans un domaine particulier de salinité.
Par exemple, il peut avoir création de dépôts de gypse important, sans que la sursaturation en chlorure de
sodium soit atteinte. Par conséquent, toute modification de l’un des facteurs entrainent l’augmentation ou
la diminution du courant, ce qui modifie le type des dépôts, soit en favorisant, soit en inhibant la
précipitation de certains sels. C’est ainsi, qu’il est impossible d’obtenir les sels de potassium et de
magnésium, si les saumures ne sont pas totalement piégées.
 6
6
 7
7
1
/
7
100%