ACTIVITÉ N°1 : Que se passe-t-il pendant la combustion du carbone

/3
/1
/1
/1
/1
/1
/1
/1
/2
/1
/1
/1
/1
/1
/1
/1
/1
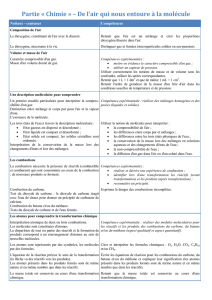
Activité n°1 : Que se passe-t-il pendant la combustion du carbone ?
1. Complète :
Nom
Atome ou molécule ?
symbole
Modèle
Carbone
..................................
.......................
....
2. Écris le bilan en toutes lettres de la combustion du carbone dans le dioxygène (1ère
ligne du tableau n°1).
3. Construis les réactifs avec les modèles moléculaires dont tu disposes.
Appelle le professeur et vérifiez ensemble les constructions.
4. Construis le produit à partir des atomes utilisés pour construire les réactifs.
5. Que dois-tu faire pour cela :..................……………………………………………….………
Appelle le professeur et vérifiez ensemble les réponses.
6. Reprends le bilan de la réaction en remplaçant les noms par les modèles. (2ème ligne)
Appelle le professeur et vérifiez ensemble les réponses.
7. L’équation chimique est l’écriture symbolique de la réaction chimique. Replace les
modèles par les symboles et les formules. Complète le tableau (3ème ligne).
Appelle le professeur et vérifiez ensemble les réponses.
8. Fais l’inventaire des atomes de carbone présents dans les réactifs et dans les produits
(4ème ligne). Fais le même compte pour les atomes d’oxygène.
9. Sachant que la masse d’un atome reste toujours la même, quelle conservation est-elle
traduite par l’équation-bilan ? …………….............................................….……..…………
Appelle le professeur et vérifiez ensemble les réponses.
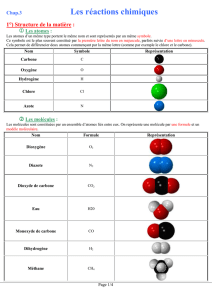
Activité n°2 : Que se passe-t-il pendant la combustion du méthane ?
1. D’après le modèle des particules de méthane, remplis le tableau suivant :
Nom
Atome ou molécule ?
Formule
Modèle
Méthane
..................................
.........................
Appelle le professeur et vérifiez ensemble les réponses.
2. Écris le bilan en toutes lettres de la combustion du méthane (1ère ligne du tableau n°2).
3. Construis les réactifs avec les modèles moléculaires dont tu disposes.
4. Construis les produits en utilisant seulement les atomes des réactifs.
Quel est le problème qui se pose ? ...................................................................................….
Appelle le professeur et vérifiez ensemble les réponses.
5. Si tu ne peux pas construire les produits à partir des réactifs, c’est qu’il faut rajouter
des molécules soit de méthane, soit de dioxygène. Faut-il rajouter des molécules de
méthane ou des molécules de dioxygène ?…………………………………………………..
Combien ? ……..…………..…………………………..………...………………………………
Appelle le professeur et vérifiez ensemble les réponses.
6. Complète la 2ème ligne du tableau en dessinant les molécules manquantes, de manière
à respecter la conservation des atomes lors de la réaction chimique.
7. Écris l’équation chimique de la réaction en indiquant, devant chaque formule chimique,
le nombre de molécules nécessaires (3ème ligne).
8. L’équation chimique doit traduire la conservation des atomes. Vérifie que c’est bien le
cas (4ème ligne) sinon corrige.
Appelle le professeur et vérifiez ensemble les réponses.

Tableau n°1 :
les réactifs réagissent pour former les produits
Bilan
………………. + ………………….. …………………………………
Modèle
+
Équation chimique
………………. + ………………….. …………………………………
nombre d’atomes
de carbone :
dans les réactifs : ....................
dans les produits : ....................
d’oxygène :
dans les réactifs : ....................
dans les réactifs : ....................
Tableau n°2 :
Bilan
……………. + ……………….. ……… + ………………………
Modèles
+
+
Équation chimique
… ………. + … ………….. … ………… + … …………
nombre d’atomes
de carbone :
dans les réactifs : ....................
dans les produits : ....................
d’hydrogène :
dans les réactifs : ....................
dans les produits : ....................
d’oxygène :
dans les réactifs : ....................
dans les réactifs : ....................
Tableau n°1 :
les réactifs réagissent pour former les produits
Bilan
………………. + ………………….. …………………………………
Modèle
+
Équation chimique
………………. + ………………….. …………………………………
nombre d’atomes
de carbone :
dans les réactifs : ....................
dans les produits : ....................
d’oxygène :
dans les réactifs : ....................
dans les réactifs : ....................
Tableau n°2 :
Bilan
……………. + ……………….. ……… + ………………………
Modèles
+
+
Équation chimique
… ………. + … ………….. … ………… + … …………
nombre d’atomes
de carbone :
dans les réactifs : ....................
dans les produits : ....................
d’hydrogène :
dans les réactifs : ....................
dans les produits : ....................
d’oxygène :
dans les réactifs : ....................
dans les réactifs : ....................
1
/
2
100%