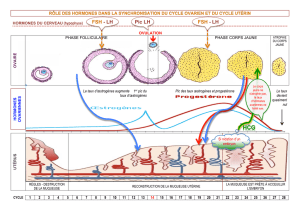
Cycle du tractus génital

D. Cycle du tractus génital
A partir de la puberté jusqu’à la ménopause, des phénomènes cycliques vont se mettre à
fonctionner. Le but est de préparer le tractus génital à un éventuel début de gestation.
La plupart du temps, la gestation n’a pas lieu, le cycle recommence alors. S’il y a nidation, le cycle
s’arrête, le tractus génital se réorganise pour permettre la gestation.
Chez la femme, le cycle est classiquement de 28 jours, l’ovulation ayant lieu le 14ème jour. IL y a
cependant des variations individuelles.

Il y a une très grosse variabilité en termes de durée de cycle et en termes de répartition des phases
du cycle, selon les espèces. La durée du cycle est variable selon les espèces et l’ovulation n’a pas
forcément lieu au milieu du cycle. Par exemple chez la brebis ou chez la vache, la phase folliculaire
est courte et la phase lutéales longue. Chez les rongeurs, le cycle dure 4 jours et l’ovulation a lieu au
milieu.
Les follicules peuvent commencer tout au long du cycle. Seuls ceux qui commenceront pendant la
phase folliculaire (3 cycles avant) auront une chance de finir leur développement.
Le corps jaune reste en activité une dizaine de jour. Il met ensuite un certain temps pour dégénérer.
Lors de cette dégénération, le corps jaune émet des hormones qui vont inhiber le développement
folliculaire de l’ovaire dans lequel il est présent : permet l’alternance entre l’ovaire droit et l’ovaire
gauche pour la production folliculaire.
Faux jumeaux : dérèglement au niveau de l’ovulation. Soit les deux ovaires ovulent en même temps,
ce qui signifie que le corps jaune n’a pas inhibé le développement folliculaire dans l’un des deux ; soit
le même ovaire produit 2 ovules.
L’ovaire est durant tout le cycle une glande endocrine extrêmement performante. C’est
essentiellement le follicule concerné par l’ovule qui sécrète des hormones. On a l’habitude de dire :
1ère partie du cycle = œstrogènes ; 2ème partie du cycle = progestérone. Attention : nuances
Corps jaune : les cellules folliculaires deviennent des cellules lutéales (hypertrophie des cellules). Les
cellules accumulent des gouttelettes lipidiques, ce qui donne la coloration jaunâtre à ces cellules
(contiennent cholestérol).

Le pic d’activité des cellules lutéales survient 4 ou 5 jours après la formation du corps jaune. (temps
de la mise en activité des cellules)

E. Hormones stéroïdes sexuelles
1. Structures

Elles dérivent toutes du cholestérol. On a hydrolyse du cholestérol, puis ajout de groupements
radicalaires. Différentes hormones vont en résulter selon le nombre de carbone et la nature des
groupements ajoutés.
On a d’abord coupure du cholestérol, ce qui forme un noyau prégnane à 21C, le prégnénolole. Celui-
ci peut évoluer soit directement en progestérone, soit est modifier et perd des carbones : on a alors
formation d’un noyau Androstane à 19C (androsténidium). Celui-ci peut soit être convertit
directement en testostérone (19C également). Androstane peut perdre un carbone et on a alors
formation d’un noyau Œstrane à 18C. Œstrane peut donner les œstrogènes : soit l’œstradiol (E2,
O2), soit l’œstrone (E1, O1).
Pour les œstrogènes on a un cycle aromatisé. L’aromatisation se fait grâce à une enzyme appelée
aromatase.
2. Transport
Ce sont des hormones : par définition elles circulent donc dans le sang. Cependant, ce sont des
lipides, elles ne peuvent pas circuler librement dans le sang, qui est un milieu aqueux.
Nécessite des protéines de transports : « Binding protéins ». Elles vont transporter les hormones
dans toute la circulation. On retrouve donc les Hormones sexuelles sous forme lié dans le sang
Voici les différentes protéines :
- ABP : Androgene BP, qui transporte les androgènes
- SBP : Steroïd BP, qui transporte toute les stéroïdes
- SSBP : Sex Steroïd BP, qui transporte toute les hormones sexuelles
- Albumine : transport non spécifique, mais une petite partie des hormones sexuelles est
transportée par l’albumine.
Toutes ces protéine spécifiques de transport (sauf albumine) sont synthétisées par le foie et on une
concentration plasmatique d’environ 3 mg / L.
Chez les rongeurs, il n’y a pas de SBP mais l’α-fœtoprotéine est présente.
3. Catabolisme
Si toutes les hormones ne sont pas utilisées, celle-ci subissent des hydroxylations et des réductions,
visant à les rendre hydrosolubles. On a ensuite conjugaison avec l’acide glucuronique au niveau du
foie. Cet ensemble conjugué se retrouve dans le sang et pourra passer la barrière de filtration rénale.
Ils se retrouvent dans les urines. On dose ces conjugués dans les urines lors de contrôle antidoping.
4. Récepteur cellulaire au Hormones sexuelles
Les Hormones sexuelles, passent par diffusion passive les membranes biologiques et se fixent à des
récepteurs cyto-nucléaires.
Tout n’est pas lié dans le sang : seules les hormones libres peuvent diffuser. il y a toujours une
fraction libre constante d’hormones sexuelles, à un instant t. Les protéines de transport jouent le
rôle de tampon, et libèrent des hormones quand d’autres diffusent à travers les membranes
(dynamique chimique).
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
1
/
29
100%