1 - aaemr

1/15
Le Coadou Laure
Leroy Céline
25/01/2011
Physio-pharmaco , électrophysiologie cardiaque, Dr Lessard
ELECTROPHYSIOLOGIE CARDIAQUE
INTEGREE :
Relation activité cellulaire et globale
Mécanisme cellulaire des arythmies
I – Rôle des courants ioniques transmembranaires
cardiaques dans les propriétés électriques globales du
cœur.
A- Rappel :
1- Potentiel de repos (Er)
Le potentiel de repos est mesuré en utilisant des microélectrodes
introduites dans la cellule cardiaque au repos, c’est à dire en diastole.
- microélectrode interne
- microélectrode externe
Ce potentiel diastolique / de repos est négatif, et varie suivant les
différents tissus cardiaques.
Le potentiel électrique à l’intérieur de la cellule étant inférieur à celui de
l’extérieur, il y a une polarisation diastolique. Elle représente l’énergie
électrique emmagasinée à l’intérieur de la cellule.
Ce potentiel membranaire est du à des gradients ioniques
- surtout du K+ : [K+] ic >> [K+]ec
- + gradient du Na+ : [Na+] ic < [Na+]ec
Au repos, la membrane est surtout perméable au K+ . Les mouvements du K+ sont :
- dû au gradient : sortie de K+
- dû au potentiel : entrée de K+
Le potentiel de repos qui s’établit a une valeur proche du potentiel d’équilibre du K+.
Les potentiels d’équilibre peuvent être établis par l’équation de Nernst

2/15
Equation de Nernst : E1 – E2 = - (zRT)/n * ln(C1/C2)
Avec : E1 = énergie à l’intérieur de la cellule avec une concentration C1.
E2 = énergie à l’extérieur de la cellule avec une concentration C2.
E1-E2 = différence de potentiel entre deux compartiments
z = signe de la balance, -1 pour les ions négatifs et +1 pour les ions positifs.
R = constante des gaz parfaits.
T = température absolue en kelvin.
n = nombre d’électrons échangés.
Si on applique cette équation aux différents ions, en connaissant leurs concentrations intracellulaire et
extracellulaire, on obtient le potentiel électrique de repos pour chaque ion :
EK = -94 mV
ECa = +130 mV
ENa = +60 mV
ECl = -40 mV
Le potentiel d’une cellule cardiaque au repos est à peu près égal au potentiel d’équilibre du potassium.
Mais le potentiel varie selon le type de cellule cardiaque (car les concentrations ioniques et les
perméabilités varient selon les tissus).
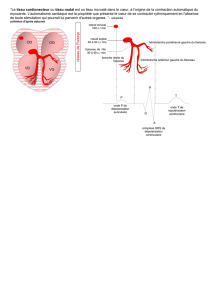
- Cellules des nœuds sinusal (SA) et atrio-ventriculaire (AV) : Potentiel de repos Er= -60 mV.
- Cellules du myocarde ventriculaire et auriculaire : Er = -80 mV.
- Cellules du faisceau de His et du réseau de Purkinje ventriculaire : Er = -95 à -100 mV.
Certaines cellules sont automatiques, elles se contractent sans stimulation extérieure : ce sont les cellules
des nœuds SA et AV, et certaines cellules du faisceau de His et du réseau de Purkinje.
• Dans ces cellules, il y a une dépolarisation diastolique spontanée lente, c’est à dire que Er augmente (il
est moins négatif avec le temps). La propriété de dépolarisation spontanée dépend de cette variation de
Er.
• L’automatisme est lié à cette pente de dépolarisation spontanée pendant la diastole.
2- Potentiel d’action (PA) et courants ioniques (ix)
Il y a une énergie électrique dans la cellule au repos, elle est libérable par un petit apport d’énergie
électrique externe. Il suffit d’apporter des charges négatives (apport à l’extérieur de la cellule) =
stimulation électrique
- soit par des électrodes
- soit par activation via les cellules voisines (préalablement activées)
Ces charges provoquent une légère dépolarisation de la membrane. Si on atteint le seuil d’automatisme,
on déclenche une dépolarisation beaucoup plus rapide et irréversible (phénomène de tout ou rien) :
apparition d’un PA.
Toutes les cellules cardiaques sont excitables. Mais les cellules automatiques arrivent toutes seules, sans
stimulation, au seuil d’automatisme. Les autres sont stimulées de proche en proche.
Parmi les cellules automatiques, les plus rapides sont appelées les cellules pace maker. Ce sont elles qui
arrivent le plus vite au seuil d’automatisme. Les pace maker physiologiques sont dans le nœud SA. Les

3/15
autres cellules automatiques sont des pace maker latents qui peuvent devenir pace maker dans des
conditions pathologiques.
A partir du seuil d’automatisme, il y a une ouverture des canaux ioniques qui permet une dépolarisation
rapide. Le PA se décompose en plusieurs phases :
Rmq : Les numéros des phases ne correspondent pas
aux numéros indiqués sur le schéma.
la phase 0 : (correspond a la phase 1 sur le schéma) dépolarisation rapide irréversible : entrée de Na+
en masse par ouverture des canaux sodiques = dépolarisation.
la phase 1 : entrée de Cl- → phase de repolarisation initiale + rapide.
la phase 2 : plateau dû à l’entrée de Ca++ .
la phase 3 : sortie de K+ → repolarisation de la cellule. Le courant K+ est retardé au niveau de la
phase 2 par l’entrée dépolarisante de Ca+ qui s’oppose à la repolarisation.
la phase 4 : période isoélectrique après le PA. Le potentiel reste plat : potentiel de repos (-90 mV) ou
présente une dépolarisation lente dans les cellules automatiques.
Il existe différentes sortes de PA selon les différents tissus cardiaques
- Dans les cellules myocardiques ventriculaires et auriculaires (tissu cardiaque pur) : le PA est
légèrement différent dans le myocarde ventriculaire et dans le myocarde auriculaire.
La phase 0 est rapide (montée rapide) dans les 2 types de cellules.
Mais le plateau est beaucoup plus large dans les cellules myocardiques ventriculaires (plateau trapézoïdal)
que dans les cellules auriculaires (plateau triangulaire).
- Dans le tissu nodal (= nœuds SA et AV), les cellules sont peu contractiles. La phase 0 est lente car il
n’y a pas de courant sodique rapide.
La dépolarisation est due au courant Ca++ qui donne aussi le plateau. Le plateau est large.
- Dans les tissus de His et de Purkinje (tissu conducteur rapide)
la phase 0 est très rapide
Le plateau est bas et très large (le plus large).
Il peut y avoir des dépolarisations spontanées.

4/15
Remarque : le tissu conducteur rapide ventriculaire correspond au faisceau de His et au tissu de Purkinje
mais tous les tissus cardiaques sont conducteurs (mais plus lents).
B – Courants ioniques et automatisme
Les courants ioniques sont des flux d’ions à travers des canaux ioniques spécifiques.
Certains canaux sont toujours ouverts : le flux d’ions est plus ou moins fort en fonction du gradient
électrique et du gradient de concentration.
D’autres canaux ont des portes d’activation qui s’ouvrent lors d’une dépolarisation. Il y a aussi des portes
d’inactivation qui se ferment lors d’une dépolarisation.
L’automatisme est dû à une dépolarisation spontanée lente, due à une entrée d’ions positifs pendant la
phase 4 dans les cellules automatiques par 2 types de canaux et courants.
1- Courants if et iCa
Dans les cellules automatiques, il existe un courant de pace maker que l’on appelle if (avant appelé iP). Ce
courant est dû aux ions Na+ et il est activé lors des hyperpolarisations (ouverture de canaux spécifiques).
Cette dépolarisation lente est renforcée par une entrée de Ca2+ par un courant appelé iCa t (= courant
calcique transitoire).
Par if et iCa t , le seuil d’automatisme est atteint.
Cette entrée de courant (sodium puis calcium) est un peu plus rapide dans les cellules du nœud SA: ces
cellules atteignent les premières le seuil d’automatisme, elles constituent le pacemaker physiologique.
Le pacemaker physiologique commande la dépolarisation de toutes les cellules voisines et du cœur
entier.

5/15
2- Courant iK
iK = courants potassiques (K+).
Dans les cellules automatiques, la dépolarisation lente spontanée est favorisée par la diminution des
courants sortants repolarisants (diminution des courants potassiques iK ).
Les cellules pace maker, dans le nœud SA, arrivent en premier au seuil d’automatisme pour 4 raisons
possibles :
- la pente de dépolarisation lente est la moins lente
- le potentiel de repos (Er) est le moins négatif.
- le seuil d’automatisme est le plus négatif.
- le PA est plus court et donc la repolarisation est plus rapide (la cellule va pouvoir se
redépolariser plus vite).
C- Courants ioniques et conduction
La conduction de l’influx cardiaque dépend de la rapidité de propagation de la dépolarisation de la phase
0 le long des fibres et d’une fibre à l’autre.
Cette phase 0 est due à 2 courants selon le type de cellule : iNa et iCa.
1- iNa et iCa
• Dans les cellules à dépolarisation rapide (myocarde ventriculaire et auriculaire, faisceau de His, tissu
de Purkinje) : la phase 0 est due à un courant sodique rapide entrant iNa
• Dans les cellules à dépolarisation lente (cellules des nœuds SA et AV) : la phase 0 n’est pas due à iNa
mais à iCa l (composante lente du courant calcique) qui donne une dépolarisation plus lente en phase 0.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
1
/
15
100%