Les accélérateurs pour l`hadonthérapie

Article hadronthérapie
pour le site « Groupe accélérateur » de la SFP
Jean-Michel Lagniel
Hadonthérapie
Les hadrons sont des particules composites formées de quarks qui, contrairement aux leptons, sont
sensibles à l'interaction forte. Il y a deux sortes de hadrons : les baryons (protons, neutrons…) et les
mésons (pions, kaons…).
Dans cet article, seul le domaine du traitement des cancers par faisceaux de protons ou d’ions sera
abordé, on ne présentera pas les techniques de traitement utilisant d’autres types de hadrons
(utilisation de neutrons – neutronthérapie - ou de pions par exemple). Les protons et les ions carbone
sont en effet les deux ions de référence pour les projets en Europe et dans le reste du monde.
Présentation de l’hadonthérapie par faisceaux de protons ou d’ions
Le traitement du cancer par irradiation des tumeurs avec des protons ou des ions plus lourds
(principalement des ions carbone) est une thérapie particulièrement prometteuse en raison de sa
précision balistique et de ses effets biologiques spécifiques.
Avantages balistiques
Les protons et les ions, en se ralentissant dans la matière, perdent la plus grande partie de leur
énergie en fin de parcours (pic de Bragg). On peut ainsi irradier seulement la tumeur en préservant les
tissus sains qui l’entourent.
Par rapport aux faisceaux de protons, les faisceaux d’ions plus lourds (carbones) ont l’avantage
supplémentaire d’une plus faible diffusion radiale, leur précision balistique est donc meilleure dans le
plan perpendiculaire à l’axe de propagation du faisceau.

Pour traiter le volume de la tumeur, on fait varier l’énergie des ions de telle sorte que leurs parcours
englobent l’épaisseur de la tumeur et on « balaie » le faisceau par un champ magnétique variable
pour couvrir, dans les deux directions transverses, l’ensemble du volume de la tumeur. Tout ceci peut
être réalisé avec une grande précision (environ 1 mm).
Avantages biologiques
L’énergie déposée dans le pic de Bragg à la fin de la trajectoire de l’ion est très élevée : le taux de
destruction des cellules malades est très important. A même dose, les ions carbone sont entre deux et
cinq fois plus efficaces que les rayonnements classiques ou que les protons.
En conclusion, les tissus et les organes critiques autour de la tumeur sont préservés, les cellules
cancéreuses sont détruites plus efficacement : la tumeur est mieux contrôlée. Il en résulte pour le
patient un accroissement de sa durée de vie et une amélioration notable de sa qualité de vie puisque
les effets secondaires de l’irradiation sont limités.

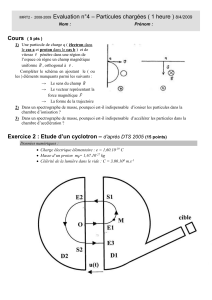
Comparaison entre un traitement IMRT 4 champs (à gauche) et un traitement carbone 2 champs (GSI,
à droite)
Le volume cible est entouré en rouge
Doses : rouge = 90 % … bleu = 10 %
Nerf optique = OAR
Parler de l’historique et des résultats obtenus

Les accélérateurs pour l’hadonthérapie
Pour les deux types de particules, l’énergie maximale de l’accélérateur est choisie pour permettre le
traitement de tumeurs jusqu’à 20 - 25 cm de profondeur (profondeur du pic de Bragg) et le flux de
particules à délivrer doit permettre des traitements les plus courts possible (temps d’immobilisation
des patients maximum de l’ordre de 10 minutes). Le tableau ci-dessous donne des valeurs typiques.
Protons
Carbones
Energie maximale
200 - 250 MeV
400 – 430 MeV/u
Nombre de particules par seconde
1 – 4 1010
5 108 - 1 109
Ce sont des caractéristiques standard, voire relativement modestes, pour les accélérateurs construits
pour la recherche en physique nucléaire dans le passé.
Accélérateurs pour les faisceaux de protons (protonthérapie)
Avec une énergie maximale des faisceaux de protons de 250 MeV, les centres de protonthérapie
utilisent des synchrotrons ou des cyclotrons. Les synchrotrons, moins compacts que les cyclotrons,
ont cependant l’avantage de permettre un ajustement aisé de l’énergie du faisceau produit. Les
cyclotrons fonctionnent à énergie fixe (l’énergie maximale), il faut installer un dégradeur d’énergie et
un spectromètre pour produire le faisceau à l’énergie désirée.
Le premier centre dédié à la protonthérapie a été construit à Loma Linda en Californie (Proton
Treatment Center, Loma Linda University Medical Center). L’accélérateur est un petit synchrotron
(environ 6 m de diamètre) dessiné, construit et mis en service par l’équipe accélérateur du Fermilab.
Plus de 10000 patients ont été traités depuis son premier fonctionnement en 1990.
Le synchrotron de Loma Linda (USA)
Pour les centres construits plus récemment aux USA, c’est un cyclotron qui est utilisé au
Massachusetts General Hospital de Boston, à l’université de l’Indiana et à l’université de Floride, c’est
un synchrotron qui a été choisi au MD Anderson Cancer Center de l’université du Texas (Houston).

Le cyclotron de Boston (USA)
Au Japon, 5 centres dédiés permettent des traitements avec des protons. Un synchrotron est utilisé à
Hyogo (centre protons et carbones), à l’université de Tsukuba, à Shizuoka et au Wakasa Wan Energy
Research Center. Un cyclotron est utilisé à Kashiwa.
Le synchrotron du centre de Shizuoka (Japon)
Parler Chine et Corée
Wanjie Proton Therapy Center, Zibo, Chine
Wanjie Irradiation Co LTD
Protons 230 MeV, Cyclotron IBA, 3 gantries + 1 H
Premier patient en décembre 2004
China-Japan Friendship Hospital, Beijing, Chine
Protons 230 MeV, Cyclotron IBA, en attente de livraison
Xian, Shanxi Province, Chine, Chang An Group (privé)
Protons 230 MeV, Cyclotron IBA,
National Cancer Center, Goyang-Si, Corée
Protons 230 MeV, Cyclotron IBA
2 gantries + 1 H + 2 lignes recherche
 6
6
 7
7
 8
8
 9
9
1
/
9
100%