TP : Conservation de l`élément cuivre

2 Bac Pro date :
Ph.Georges Sciences 1/2
TP : CONSERVATION DE L'ÉLÉMENT CUIVRE
Avant de manipuler, écoutez avec attention les précautions à prendre et les règles de sécurité
rappelées par le professeur.
I. Objectif
Mettre en évidence la conservation de l'élément cuivre au cours de quelques transformations.
II. Matériel
• Des gants et des lunettes.
• Un cristallisoir et une pissette.
• 3 tubes à essai sur un support.
• 3 béchers de 100 mL.
• 1 pipette.
• 1 erlenmeyer de 100 mL.
• 1 entonnoir et du papier filtre.
• 1 appareil de chauffage et son alimentation électrique.
• Une pince en bois et une spatule.
• Solution de sulfate de cuivre de concentration 5.10 – 2 mol/L.
• Solution d'hydroxyde de sodium de concentration 2 mol/L.
• Du carbone végétal, de l'oxyde de cuivre (II) et 2 spatules (pour
la classe).
• De la tournure de cuivre et de la laine de fer.
• Solution d'acide nitrique de concentration 8 mol/L.
III. Manipulations
Pour chaque étape :
• Faire un schéma de l'expérience.
• Noter vos observations (aspect, couleur, état physique, etc...) concernant l'élément cuivre
avant et après la réaction.
1. Action de l'acide nitrique sur le cuivre
Il est préférable que le professeur réalise lui-même cette expérience.
• Placer un morceau de tournure de cuivre d'environ 1cm dans un tube à essai.
• Sous la hotte, munis de gants et de lunettes, ajouter avec précaution environ 1 mL de la solution
d'acide nitrique.
• Observer.
2. Action du fer sur une solution contenant des ions Cu 2 +
• Dans un tube à essai, introduire de petits morceaux de laine de fer.
• Ajouter 2 cm de la solution contenant des ions Cu 2+ (solution de sulfate de cuivre).
• Observer.
3. Obtention de l'hydroxyde de cuivre (II)
• Dans un bécher, verser environ 25 mL de la solution de sulfate de cuivre.
• Ajouter une dizaine de gouttes de la solution aqueuse d'hydroxyde de sodium.
• Recueillir le précipité d'hydroxyde de cuivre obtenu dans un tube à essai propre.

Ph.Georges Sciences 2/3
4. Chauffage de l'hydroxyde de cuivre (II)
• Muni de lunettes, chauffer doucement le précipité d'hydroxyde de cuivre (II) (attention aux
projections).
• Observer.
5. Action du carbone sur l'oxyde de cuivre
• Plier un morceau de papier carré suivant ces diagonales.
• Mélanger intimement, sur le morceau de papier, une spatule de poudre d'oxyde de cuivre (II) et
environ un dixième d’une spatule de poudre de carbone.
• Plier délicatement la feuille pour placer le mélange dans un tube à essai.
• Chauffer.
• Observer.
IV. Exploitation
• Représenter l'ensemble des transformations précédentes en complétant le cycle suivant.
• Justifier le titre du TP
Cu
Cu(OH)2
Cu2+
CuO

2 Bac Pro date :
Ph.Georges Sciences 3/2
TP : CONSERVATION DE L'ÉLÉMENT CUIVRE
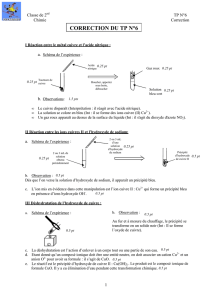
1. Action de l'acide nitrique sur le cuivre
Le cuivre disparaît. La solution se décolore. Un gaz roux (NO2) apparaît ; il est plus lourd que l'air.
2. Action du fer sur une solution contenant des ions Cu 2 +
Un dépôt de cuivre sur le tampon de laine de fer apparaît. La solution se décolore (disparition des Cu2+).
3. Obtention de l'hydroxyde de cuivre (II)
Solution d'hydroxyde de sodium versée dans une solution de sulfate de cuivre.
Un précipité bleu surnage (le filtrage a été abandonné car le précipité disparaît au contact du filtre).
4. Chauffage de l'hydroxyde de cuivre (II)
Le précipité d'hydroxyde de cuivre noircit (obtention de CuO)
5. Action du carbone sur l'oxyde de cuivre
• Mélanger intimement une spatule de poudre de carbone et une spatule de poudre d'oxyde de
cuivre (II) sur un morceau de papier.
En fait, il faut 159 g de Cu0 pour 12 g de C ; soit un rapport de 1 à 13
Le mélange devient incandescent (600°). Dépôt de cuivre sur les parois du tube.
• Justifier le titre du TP
L'élément cuivre représente ce qui est commun, au métal cuivre, à l'ion cuivre II, à l'hydroxyde de
cuivre II et à l'oxyde de cuivre, malgré la diversité de tous ces composés chimiques.
Au cours de ces différentes transformations chimiques, l'élément cuivre s'est conservé.
Cu
action du carbone action de l'hydroxyde de
sodium
Cu(OH)2
Cu2+
chauffage
action du fer
action de l'acide nitrique
CuO
1
/
3
100%