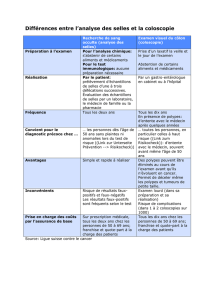
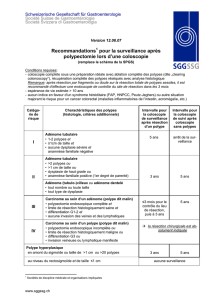
Prospective Results of Surveillance Colonoscopy in

GASTROENTROLOGY 2006
Computed Tomographic Colonography: Assessment of Radiologist Performance
With and Without Computer-Aided Detection. Halligan S, Altman DG, Mallett S,
Taylor SA, Burling D, Roddie M, Honeyfield L, McQuillan J, Amin H, Dehmeshki J.
Gastroenterology 2006;131: 1690-1699 (Abstract)
L’utilisation de logiciel dédié permet-elle d’obtenir une efficacité analogue à la coloscopie
conventionnelle ? C’est la question à laquelle ont essayé de répondre S Halligan et al.
(Londres). Dix radiologues entraînés à la lecture des scanners mais pas à celle des colo-
scanners ont interprétés les examens de 107 patients qui avaient subi des coloscopies et
dont 60 avaient des polypes (142). La lecture a été réalisée d’abord sans l’aide du logiciel
puis avec le logiciel. Avec le logiciel, des polypes ont été détectés chez 41/60 patients. Le
logiciel permet d’augmenter significativement la sensibilité de l’examen chez 70 % des
radiologues. La détection du nombre de polypes est également améliorée par l’utilisation
du logiciel, 12 polypes supplémentaires sont détectés par chaque lecteur. Les polypes
d’une taille inférieure à 5 mm et entre 6 et 9 mm sont plus facilement détectés à l’aide
du logiciel. Toutefois la performance globale reste médiocre, même avec le logiciel, les
lecteurs n’ont détecté que 10 polypes (51 %) de plus de 10 mm et 24 (38,2 %) des
polypes de plus de 6 mm. Le logiciel permet également de réduire la durée de
l’interprétation.
Yield of Advanced Adenoma and Cancer Based on Polyp Size Detected at
Screening Flexible Sigmoidoscopy. Schoen RE, Weissfeld JL, Pinsky PF, Riley.
Gastroenterology 2006;131: 1683-1689 (Abstract)
Quelle valeur apporter aux petits polypes ? La question est d’importance depuis que de
nouvelles techniques de dépistage observationnel permettant la détection de polype mais
pas leur exérèse qu’il s’agisse de la coloscopie virtuelle, de l’Aer-O-Scope voire de la
capsule. C’est à cette question qu’ont essayé de répondre RE Schoen et al. en analysant
les résultats du PLCO Cancer Screening Trial, un essai randomisé multicentrique qui avait
pour objectif d’évaluer l’efficacité de la détection des cancers de la prostate, du poumon,
du côlon et de l’ovaire à un stade précoce.
Dans cette étude 154 000 patients âgés de 55 à 74 ans ont été inclus. Sur les 77 565
patients du groupe « interventionnel » (participant à un dépistage), 64 658 ont subi une
sigmoïdoscopies. Au cours de la sigmoïdoscopie, réalisée souvent par une infirmière,
aucun geste (biopsie, exérèse n’était réalisé, une coloscopie était réalisée dans un second
temps. Dans 15 150 cas (23,4 %) un polype ou une masse a été détectée. Les auteurs
n’ont toutefois pu obtenir des renseignements complets que pour 10 850 polypes
détectés par sigmoïdoscopie. Les auteurs ont ensuite comparé les résultats de la
sigmoïdoscopie et les résultats de la pièce de polypectomie.
Chez les femmes ayant un polype de plus de 1 cm, 6,3 % avaient un cancer et
54,2 % un adénome avancé, pour les hommes les chiffres sont respectivement de
6,5 % et 54,8 %.
Chez les femmes ayant un polype de 0,5 à 0,9 cm dans 0,6 % il s’agissait d’un
cancer dans 14,5 % des cas d’un adénome avancé. Chez les hommes les résultats
sont similaires, respectivement 0,7 % et 15,9 %.
Pour les lésions de moins de 0,5 cm, il est intéressant de noter chez les femmes
que 0,1 % avaient un cancer et 4,1 % un adénome avancé, pour les hommes les
chiffres sont respectivement de 0,3 % et 4,9 %.
Chez les patients porteurs de polype de 0,5 à 0,9 cm dans le côlon distal, 5,5 % avaient,
dans le côlon proximal, des adénomes avancés de moins de 1 cm mais qui avaient des
compartiments villeux ou une dysplasie de haut grade, et 9,9 % avaient des adénomes
de plus de 1 cm.
Ainsi cette étude montre que des polypes même de petite taille peuvent être
d’authentique adénome avancé voire des cancers. C’est un point important à signaler à
un moment où la société américaine de radiologie a publié en 2005 dans Radiology une
proposition de consensus (Consensus) dans lequel on insiste sur l’importance de la taille

des polypes car « les lésions de petite taille peuvent être laissées en place et
surveillées » !!!!!
AGA Institute Technical Review on the Use of Endoscopic Therapy for
Gastroesophageal Reflux Disease. Falk GW, Fennerty MB, Rothstein RI.
Gastroenterology 2006;131: 1313-1314 (Abstract)
L’avis très réservé de l’association américaine de gastro-entérologie sur la place des
techniques de traitement endoscopique du RGO.
Will Screening Colonoscopy Disappear and Transform Gastroenterology
Practice? Threats to Clinical Practice and Recommendations to Reduce Their
Impact: Report of a Consensus Conference Conducted by the AGA Institute
Future Trends Committee. Clinical Practice and Economics Committee.
Gastroenterology 2006;131:1287-1312 (Abstract) (Article en PDF)
Le résumé d’une conférence de consensus qui s’est tenue en avril 2006 à Washington sur
l’avenir du gastro-entérologue. Un article très intéressant, éclairant sur l’avenir de notre
discipline.
L’avancement en âge, l’augmentation de la fréquence de l’obésité, le traitement de
l’hépatite, des d’affections chroniques ou difficiles à prendre en charge vont occuper
largement les gastro-entérologues. Par contre la place des « non-gastro-entérologues »
dans le dépistage des affections néoplasiques va augmenter compte tenu de l’émergence
de nouvelles technologies de maniement plus facile. Nos collègues américains pensent
que dans les 5 années à venir, le nombre d’endoscopies diagnostiques va diminuer de
façon considérable et que ceci ne fera que s’accentuer dans les décades à venir avec
l’apparition d’analyses protéomiques, épigénétiques et génétiques. La coloscopie
virtuelle, la vidéo-capsule pour explorer le tube digestif haut et bas (équipée de
dispositifs permettant des « biopsies optiques » voire des gestes thérapeutiques avec
éclats de laser et radiofréquence…) vont transformer la gastro-entérologie. L’endoscopie
sera essentiellement thérapeutique s’aidera de technologie telle que le FICE, le NBI, la
microscopie confocale, la tomographie par cohérence optique et la fluoroscopie. On
évoque des endoscopes simplifiés qui pourront permettre au médecin généraliste de
réaliser des gestes diagnostiques et de surveillance.
La prise en charge de l’obésité, les cancers digestifs et le traitement des hépatites vont
être au centre des préoccupations des gastro-entérologues. La mise en place de
ballonnet intragastrique pour le traitement de l’obésité, voire l’application d’électrodes
intragastrique ou de divers dispositifs intra-gastriques deviendra un travail quotidien pour
l’endoscopiste.
Prospective Results of Surveillance Colonoscopy in Dominant Familial Colorectal
Cancer With and Without Lynch Syndrome. Dove–Edwin I, de Jong AE, Adams J,
Mesher D, Lipton L, Sasieni P, Vasen HFA, Thomas HJW Gastroenterology
2006;130:1995-2000 (Abstract)
L’équipe du St Marks’Hospital a réalisé une étude prospective à partir de familles ayant
une histoire clinique de cancer colorectal à forme autosomale dominante ont été inclues.
En fonction du résultat immunohistochimique MSI de la tumeur du phénotype, les
familles étaient classées Lynch si plus de 50 % de la tumeur montrait la présence de
MSI-H ou si il y avait une mutations sur les gènes MSI, la mutation étant définie comme
une instabilité du locus BAT26.
Les familles sans mutation connue et si moins de 50 % de la tumeur montrait la
présence de MSI était classées non Lynch.
Des coloscopies de dépistage ont été réalisées chez tous les apparentés du 1er degré de
tout patient touché. Les coloscopies ont été réalisées tous les 5 ans pour les patients à
partir de 25 ans et tous les 3 ans en cas de détection d’adénome.
Ainsi 125 patients issus de 97 familles ont été testés et 288 apparentés à risque ont été
dépistés.
Vingt neuf familles ont été déclarées porteuses d’un syndrome de Lynch.
Chez les apparentés, 776 coloscopies ont été réalisées :

7/91 (7,7 %) adénomes à haut risque ont été détectés dans les familles Lynch
4/91 (4,4 %) cancers ont été détectés dans les familles Lynch
Des adénomes multiples ont été détectés chez 13/197 (6,6 %) des familles non
Lynch
En conclusion, les patients ayant une histoire clinique de cancer colorectal à forme
autosomale dominante, qu’il s’agisse ou non d’un syndrome de Lynch, ont un risque
équivalent d’adénome à haut risque mais les cancers ne surviennent que dans les
syndromes de Lynch. Ainsi la surveillance des patients n’ayant pas de syndrome de
Lynch peut être espacées compte tenu du risque faible de cancer d’intervalle tandis que
les syndromes de Lynch doivent être surveillés de façon plus étroite comme cela est
recommandé (tous les ans).
Guidelines for Colonoscopy Surveillance After Cancer Resection: A Consensus
Update by the American Cancer Society and the US Multi-Society Task Force on
Colorectal Cancer. Rex DK, Kahi CJ, Levin B, Smith RA, Bond JH, Brooks D, Burt RW,
Byers T, Fletcher RH, Hyman N, Johnson D, Kirk L, Lieberman DA, Levin TR, O’Brien MJ,
Simmang C, Thorson AG, Winawer SJ Gastroenterology 2006;130:1865-1871
(Abstract)
Mise au point des Recommandations américaines sur la surveillance post-opératoire des
cancers du côlon. On insiste sur la nécessité d’une coloscopie totale préopératoire pour
détecter et traiter les lésions synchrones. En cas de sténose il est nécessaire de réaliser
en pré-opératoire un lavement baryté en double contraste ou un colo-scanner. Une
coloscopie devra être réalisée dans les 3 à 6 mois suivant l’intervention.
Une coloscopie systématique est préconisée 12 mois après l’intervention. Si celle-ci est
normale, le prochain contrôle a lieu 3 ans plus tard. Si ce contrôle est égalemnt normal,
une autre coloscopie est réalisée à 5 ans. Des intervalles plus courts dans la surveillance
sont préconisés lorsqu’un adénome est décelé lors d’un examen de contrôle. Des
coloscopies plus rapprochées sont également préconisées en fonction de l’âge du patient,
des antécédents familiaux, d’arguments en faveur de cancer colique familiaux sans
polypose.
Les patients ayant subi une résection antérieure du rectum étant à plus fort risque de
récidive précoce, on peut envisager chez ces patients, bien qu’il n’y ait pas de niveau de
preuve, une échoendoscopie ou une sigmoïdoscopie tous les 3-6 mois durant les deux
premières années afin de déceler précocement une récidive.
Guidelines for Colonoscopy Surveillance After Polypectomy: A Consensus
Update by the US Multi-Society Task Force on Colorectal Cancer and the
American Cancer Society. Winawer SJ, Zauber AG, Fletcher RH, Stillman JS,
O’Brien MJ, Levin B, Smith RA, Lieberman DA, Burt RW, Levin TR, Bond JH, Brooks D,
Byers T, Hyman N, Kirk L, Thorson A, Simmang C, Johnson D, Rex DK
Gastroenterology 2006;130:1872-1885 (Abstract) (Texte complet en PDF)
Les guidelines américains concernant la surveillance après polypectomie dans lesquels
sont abordées 3 situations :
Les patients à risque ayant 3 adénomes ou plus, une dysplasie de haut grade, des
compartiments villeux, ou un adénome de plus de 1 cm qui doivent subir un
contrôle au bout de 3 ans,
Les patients à faible risque qui ont un ou 2 adénomes tubulleux de moins de 1 cm
sans dysplasie de haut grade qui doivent subir un contrôle après 5 à 10 ans,
Les patients qui ont un polype hyperplasique qui doivent avoir un contrôle après
10 ans.
Toutes les différentes situations sont abordées et on insiste sur la bonne qualité de
l’examen initial et des contrôle compte tenu du nombre non négligeable de polypes
manqués.
Thirty-Year Analysis of a Colonoscopic Surveillance Program for Neoplasia in
Ulcerative Colitis. Rutter MD, Saunders BP, Wilkinson KH, Rumbles S, Schofield G,

Kamm MA, Williams CB, Price AB, Talbot IC, Forbes A Gastroenterology
2006;130:1030-1038 (Absract)
MD Rutter et al.(1) rapportent l’expérience du St Mark’s Hospital après 30 ans de
dépistage du cancer rectocolique (CRC) au cours de la RCH. Durant cette période 600
RCH dépassant l’angle colique gauche ont participé à ce dépistage : le programme étant
débuté après 8 ans d’évolution de la RCH et la coloscopie étant renouvelée tous les 2
ans. Deux mille six cent vingt sept coloscopies ont été réalisées, aucun accident n’est à
signaler. Chez 111 RCH (18,5 %) 215 lésions ont été décelées dont 52 adénomes
sporadiques, 78 dysplasies de bas grade (DBG) et 30 dysplasies de haut grade (DHG), 28
DALM et 30 cancers (8 cancers supplémentaires sont survenus chez des patients ayant
abandonné le programme de dépistage). Il est intéressant de noter que le diagnostic de
cancer n’a été fait en pré-opératoire que dans 17 cas, le diagnostic étant fait sur
l’examen de la pièce opératoire chez 1es 13 autres patients colectomisés pour DBG (3),
DHG (6), pour RCH résistant au traitement ou compliquée (4). Il est important de
signaler que 16/30 sont des cancers d’intervalle.
Durant cette période de 30 ans, 89 RCH ont été opérées : 44 pour des raisons en rapport
avec la résistance ou l’aggravation de la maladie, chez les 45 autres RCH, des CRC ont
été découvert sur la pièce chez 3/14 DBG, 6/16 DHG, 14/14 CRC, 0/1 adénome.
Plusieurs éléments sont surprenants dans cet article :
la faible incidence de CRC, les auteurs évoquent la possibilité de la
chimioprévention par le 5-ASA qu’ils utilisent systématiquement depuis de
nombreuses années,
un faible nombre de cancers proximaux avec une stabilité des cancers distaux : là
aussi les auteurs évoquent un rôle possible du 5-ASA dont la concentration est
plus élevée que dans le côlon distal,
l’absence d’influence de l’âge d’apparition de la RCH sur la survenue du cancer,
une stabilité de l’incidence des cancers au delà d’une évolution de la maladie de
plus de 40 ans ne justifiant pas d’intensification des programmes de dépistage
avec le temps
le nombre élevé de cancers d’intervalle (16/30), cela s’explique certainement par
le faible nombre médian de biopsies réalisées au cours de ces coloscopies (8)
alors que la plupart des auteurs recommandent une biopsie par quadrant tous les
10 cm avec un nombre plus élevé dans le côlon gauche conduisant à un minimum
de 32 biopsies.
Ainsi, il apparaît que le bénéfice d’un dépistage tel qu’il est réalisé au St Marks est faible
1 RCH sur 21 bénéficie de ce lourd programme 131 coloscopies pour une révélant une
anomalie
The Aer-O-Scope: Proof of Concept of a Pneumatic, Skill-Independent, Self-
Propelling, Self-Navigating Colonoscope. Vucelic B, Rex D, Pulanic R, Pfefer J,
Hrstic I, Levin B, Halpern Z, Arber N Gastroenterology 2006;130:672-677 (Abstract)
(Texte complet en PDF)
Etude pilote réalisée chez 12 volontaires sains avec l’Aer-O-Scope, coloscope composé
d’une gaine jetable sans canal opérateur dont la progression s’effectue par de l’air
insufflé dans le recto-côlon entre un ballon bloqué dans la partie inférieure du rectum et
un autre ballon situé à l’extrémité de la gaine. La lumière est fournie par des LED. La
vision peut être frontale et circulaire. La progression est guidée à partir d’un clavier.
L’examen a été réalisé sans sédation. Le cæcum a été atteint chez 10 sujets en un temps
moyen de 10,0 ± 7 minutes. Chez 2 patients il n’a pas été possible de dépasser l’angle
droit. Deux sujets ont eu besoins d’antalgiques, 4 ont se sont plaint de ballonnements et
de transpiration.
1
/
4
100%