Brucella sp est une bactérie pathogène

Université des Sciences et Technologies du Languedoc – Montpellier II
Année universitaire 2003-2004
Diplôme d’Etudes Approfondies (DEA) Biologie – Santé
Développement d'une stratégie de traitement
anti-infectieux par ciblage d'un facteur de
virulence du pathogène Brucella suis.
Emeline LAURENT
Responsable de Stage : Stephan KÖHLER
Microbiologie, Pathologie Cellulaire et Infectieuse
INSERM U 431
Place Eugène Bataillon, 34095 Montpellier Cedex 5

Brucella sp est une bactérie pathogène à
développement intracellulaire facultatif, dont les
cellules-cibles sont les macrophages ; elle est
responsable d’une anthropozoonose : la brucellose.
Chez l’homme, la maladie se caractérise par une
septicémie, puis une fièvre ondulante pouvant
conduire à une maladie chronique. Actuellement, il
existe un traitement antibiotique efficace contre la
brucellose, mais qui se limite au stade aigu.
Cependant, des mutations spontanées peuvent
apparaître, produisant des souches résistantes aux
antibiotiques. De plus, il est relativement simple de
produire ces souches résistantes, notamment dans
le cadre du terrorisme bactériologique. Il est donc
important de développer de nouveaux agents anti-
infectieux non antibiotiques.
Récemment, lors d’une étude effectuée au
laboratoire, des mutations ont été induites dans les
différents gènes de Brucella suis, par insertion du
transposon Tn5, afin d’étudier l’influence de ces
mutations sur la multiplication des bactéries au
sein des macrophages THP-1 (réf. 1). Ainsi, 131
mutations dans 59 gènes différents ont été
sélectionnées. Une des mutations qui montre la
plus grande atténuation de la multiplication des
bactéries après 48h d’infection, par rapport à la
souche sauvage, est une mutation au sein du gène
codant pour la protéine DsbB. Cette protéine est
spécifique aux bactéries et semble, pour cela, être
un bon candidat pour la recherche d’agents qui
inhiberaient sa fonction, et donc la multiplication
des bactéries au sein des macrophages, lors d’une
infection.
DsbB est une protéine qui possède des
homologues dans la plupart des bactéries gram
négatives. Elle fait partie des protéines Dsb,
responsables de la formation et de l’isomérisation
des ponts disulfures au sein des protéines en
maturation dans le périplasme. Chez Escherichia
coli, il existe six protéines impliquées : DsbA, B,
C, D, E et G. Le mécanisme principal responsable
de la formation des ponts disulfures dans le
périplasme met en jeu les protéines DsbA et DsbB
(ref. 2). Dans ce processus, DsbA est l’oxydant
primaire : elle possède une séquence active CXXC
inclue dans un domaine thioredoxine-like. In vivo,
DsbA est à l’état oxydé, et se réduit en catalysant
la formation d’un pont disulfure à partir d’une
paire de cystéines d’une protéine substrat. Ensuite,
la forme réduite de DsbA revient à son état oxydé
natif par l’intermédiaire de DsbB. Cette dernière
est insérée dans la membrane cytoplasmique ; elle
possède quatre segments transmembranaires et
deux domaines périplasmiques contenant chacun
une paire de cystéines actives. Ces deux paires de
cystéines sont oxydées à l’état natif. La première
paire de cystéines réoxyde DsbA, et transfère les
deux électrons obtenus à la deuxième paire de
cystéines de DsbB. Finalement, les deux électrons
sont transférés vers la chaîne respiratoire via des
quinones ; et DsbB revient à l’état oxydé.
Mon travail, au cours de ce stage, a été de
développer un modèle permettant de tester des
inhibiteurs de la voie de formation des ponts
disulfures sur les protéines sécrétées dans le
périplasme, via DsbA, DsbB et les quinones ; puis
de tester certains inhibiteurs potentiels. Afin de
s’affranchir des contraintes imposées par la
manipulation de bactéries comme B. suis, nous
avons décidé de développer notre modèle à partir
de souches d’E. coli : CA 8000 sauvage et mutée
sur le gène dsbB. Ce modèle est rendu possible par
l’homologie entre les gènes dsbB d’E. coli et de B.
suis. Nous avons transfecté la souche mutante
dsbB- d’E. coli à l’aide du plasmide pBBR1MCS
contenant le gène dsbB de B. suis homologue au
gène muté (pBBR dsbB).
Afin de nous assurer de la validité de notre
modèle, nous avons testé la complémentation de la
souche mutée dsbB- d’E. coli par le gène
homologue de B. suis en étudiant la croissance des
différentes souches en présence de différentes
concentrations de dithiothreitol (DTT).
0
0,2
0,4
0,6
0,8
1
1,2
1,4
1,6
1,8
2
0 5 10 15 20 25 30
temps (heures)
abs orbance
CA 8000
CA 8000 dsbB-
CA 8000 dsbB- + pBBR dsbB (B. suis)
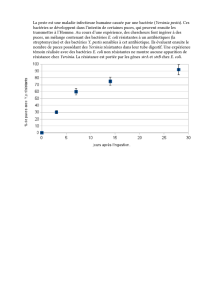
fig 1. Courbe de croissance type des différentes souches d’E.
coli en présence de 4mM de DTT.

Le DTT est un puissant agent réducteur qui
est connu pour réduire de nombreuses protéines ;
ce qui se traduit par le mauvais repliement de
protéines requérant la présence de ponts disulfures.
Ainsi, en présence de concentrations importantes
de DTT, les souches bactériennes n’exprimant pas
les composants cellulaires impliqués dans la
formation des ponts disulfures, comme la protéine
DsbB, peuvent être dans l’incapacité de se
multiplier (ref. 3). Les courbes de croissance que
nous avons obtenues (fig. 1) montrent qu’en
présence de DTT, la croissance de la souche
sauvage est affectée, mais elle parvient tout de
même à se multiplier jusqu’à une concentration de
8mM en DTT. Par contre, les bactéries de la
souche dsbB- sont dans l’incapacité de se
multiplier, dès une concentration en DTT de 4mM.
Les courbes montrent également que la
transfection par le gène dsbB de B. suis, restaure
en partie le phénotype sauvage pour des
concentrations en DTT comprises entre 4 et 6mM.
Aussi, nous avons testé plusieurs agents
anti-infectieux potentiels sur les différentes
souches, en présence d’une concentration de 4mM
de DTT.
Le premier composé que nous avons utilisé
pour pouvoir inhiber la voie de synthèse des ponts
disulfures, via DsbB, est l’acide kojique.
O
O
OH
CH2OH
O
O
CH2OH
O
O
(A)
(B)
fig 2. Formules chimiques de l’acide kojique (A) et de
l’acide kojique modifié (B).
Il s’agit d’un composé dont la structure (fig
2.) ressemble à celle des quinones, lesquelles, in
vivo, transfèrent les électrons de DsbB réduit vers
la chaîne respiratoire.
Ainsi, l’acide kojique ne devrait réoxyder
DsbB que partiellement et interrompre son
recyclage via la chaîne respiratoire. Ceci devrait
donc bloquer la formation des ponts disulfures au
sein du périplasme en présence de DTT, et donc la
croissance des bactéries.
0
0,2
0,4
0,6
0,8
1
1,2
1,4
1,6
1,8
2
0 5 10 15 20 25 30
temps (heures)
abs orbance
CA 8000 (DTT)
CA 8000 (DTT + acide kojique)
dsbB- (DTT)
dsbB- (DTT + acide kojique)
dsbB- + pBBR dsbB (B. suis) (DTT)
dsbB- + pBBR dsbB (B. suis) (DTT + acide kojique)
fig 3. Courbe de croissance type des différentes souches de
bactéries en présence de DTT (4mM) et / ou d’acide
kojique (10 µM).
Les expériences que nous avons réalisées (fig
3.) montrent que l’acide kojique n’a pas
d’influence sur la croissance des bactéries, quelque
soit la concentration utilisée (de 1 à 100µM). Ce
résultat peut être expliqué par le fait que, l’acide
kojique étant très hydrophile, il ne parvient peut-
être pas à franchir la membrane des bactéries. En
collaboration avec le laboratoire du professeur
Montero (UMR 5032, ENSCM), nous avons donc
étudié l’effet de la greffe d’une chaîne hydrophobe
(chaîne d’acide palmitique) sur l’acide kojique,
afin de faciliter sa pénétration dans les bactéries.
Néanmoins, nous obtenons le même type de
résultats que pour l’acide kojique simple.
Bien que les résultats obtenus avec l’acide
kojique et son dérivé montrent que ces molécules
n’inhibent pas l’activité Dsb, le modèle mis en
place lors de mon stage devrait permettre de tester
de nouveaux produits, à plus grande échelle et de
manière plus systématique.
1- Köhler et al., PNAS (2002), 99(24) pp 15711-15716
2- S. Raina & D. Missiakas, Annu. Rev. Microbiol. (1997),
51 pp 179-202
3- Missiakas et al., Proc. Natl. Acad. Sci. USA (1993), 90 pp
7084-7088
1
/
3
100%