Réactions des composés aromatiques

Joelle Pelletier 1 Réactions des conposés aromatiques
CHM-2302B
Les réactions des composés aromatiques
Les réactions de substitution électrophile aromatique:
Cette réaction d'addition de Br2 n'est pas favorisée:
+ Br2addition
Br
Br
Réaction endothermique:
comprend la perte de
152 kJ/mol de
stabilisation aromatique
Mécanisme réactionnel:
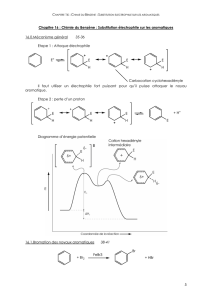
1-formation de l'électrophile (activation du Br2)
Br Br + FeBr3Br Br FeBr3
2-substitution
Br Br Fe
Br
Br
Br
lent
Br
HBr
HBr
HFeBr4_
3-déprotonation

Joelle Pelletier 3 Réactions des conposés aromatiques
CHM-2302B
Nitration:
1-formation de l'électrophile
HNO3 + H2SO4ON
O
OH2
HSO4
O N O + H2O
cation nitronium
2, 3- substitution et déprotonation
+O N O
Sulfonation:
S
O
OO

Joelle Pelletier 4 Réactions des conposés aromatiques
CHM-2302B
Les explosifs: le TNT
Toluène
HNO3/ H2SO4
CH3
CH3NO2
NO2
O2N
2,4,6-trinitrotoluène
(TNT)
L'alkylation de Friedel-Crafts:
Réaction globale:
RX
Halogénure
d'alkyle
1 équivalent
d'acide de Lewis
(activateur)
++ HX
R
ROH
Alcool tertiaire
++ H2O
R
H2SO4
H
CH
C
Alcène
+CH
H2SO4
R R RCH2
R
Formation du carbocation (électrophile):
i-halogénure d'alkyle

Joelle Pelletier 5 Réactions des conposés aromatiques
CHM-2302B
ii-alcool
iii-alcène
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
1
/
17
100%