Recommandations récentes françaises et européennes sur le

Recommandations pour les troubles du métabolisme glucidique
RECOMMANDATIONS
씰Cœur et diabète de type 2
Le texte de l’HAS (actualisation des recommandations
professionnelles dans le traitement médicamenteux
du diabète de type 2, novembre 2006) est axé sur le trai-
tement du diabète avéré, le texte est remarquablement clair,
simple et synthétique ; celui de l’ESC (diabète, prédiabète et
maladies cardiovasculaires, janvier 2007), établi en associa-
tion avec l’Association Européenne d’Etude du Diabète,
porte plus particulièrement sur le diagnostic du diabète et des
troubles du métabolisme glucidique en général et sur le risque
lié au diabète et aux états prédiabétiques en insistant sur la
valeur diagnostique et pronostique essentielle de la glycémie
2 heures après charge orale en sucre.
Dans cet article, nous rapportons les principales nouveautés en
insistant sur les aspects de pratique quotidienne. Les textes
complets représentent des mises au point quasi exhaustives sur
le sujet et sont consultables aux adresses internet suivantes :
– ESC : 72 pages dont 15 de références bibliographiques,
texte disponible en anglais à http://www.escardio.org/know-
ledge/guidelines/ (Ces recommandations sont publiées dans
l’EHJ 2007 ; 28 : 88-136),
– HAS : disponible en français à http://www.has-sante.fr/por-
tail/display.jsp?id=c_459270. Il s’agit de l’actualisation des
recommandations de l’Agence du Médicament “Traitement
médicamenteux du diabète de type 2” (1999) et des recom-
mandations de l’Anaes “Stratégie de prise en charge du
patient diabétique de type 2 à l’exclusion de la prise en charge
des complications” (2000).
❚❚ POINTS FORTS DES RECOMMANDATIONS ESC
1. – Définitions du diabète et des états prédiabétiques
selon l’ESC
Ces définitions reprennent les définitions OMS et sont résu-
mées dans le tableau I.
2. – Deux messages clés
>>> Hyperglycémie provoquée per os (HGPO) chez tous les
patients cardiovasculaires: recommandation de classe Ia
Recommandations récentes françaises et
européennes sur le diagnostic, le pronostic et le
traitement des troubles du métabolisme glucidique
M. GENEST
Service de Cardiologie, Centre Hospitalier, PROVINS.
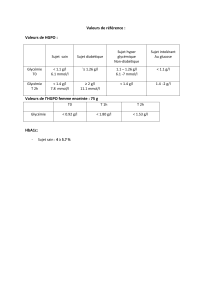
OMS HGPO :
2 états intermédiaires groupés Glycémie à jeun Glycémie à 2 h Nombre de critères
en anomalie du métabolisme
glucidique
Normal G < 1,1 g/L G < 1,4 g/L Les deux
Anomalie de la glycémie à jeun 1,1 ≤ G < 1,26 g/L G < 1,4 g/L Les deux (c’est la glycémie à
jeun qui est en cause)
Anomalie de la tolérance Les deux, c’est de plus la
au glucose G < 1,26 g/L 1,4 ≤ G < 2 g/L glycémie à 2 h qui est aussi
en cause
Diabète G ≥ 1,26 g/L ≥ 2 g/L L’un ou l’autre
Tableau I : Définitions selon l’ESC.

씰Cœur et diabète de type 2
Il semblerait que tous les coronariens devraient avoir une
HGPO pour préciser leur statut glucidique, la glycémie à
jeun ne suffisant jamais, ni à titre diagnostique, ni à titre pro-
nostique.
●L’étude DECODE (BMJ, 1998; 317 : 371-5 ; Lancet, 1999 ;
354 : 617-21) a montré que seuls 28 % des patients présen-
taient les deux critères diagnostiques de diabète (glycémie à
jeun et glycémie à 2 heures), 40 % le critère glycémie à jeun
seul et surtout 31 % le critère glycémie à 2 h seul. Ainsi donc,
se contenter de la glycémie à jeun c’est manquer le diagnos-
tic de près d’un tiers des diabétiques (pour mémoire,
DECODE analysait les données de 10 cohortes prospectives
européennes regroupant 2 200 patients).
●Dans l’Euro Heart Survey tout récemment publié (M. Bart-
nik et al. Heart, 2007 ; 93 : 72-7), il apparaît qu’un test de
tolérance au glucose après charge orale est nécessaire à la
détermination correcte du risque des coronariens. 110 centres
issus de 25 pays ont prospectivement enrôlé 4 961 patients
chez lesquels une glycémie à jeun a été mesurée et, chez les
3 362 patients n’ayant pas d’anomalie connue du métabo-
lisme glucidique, une glycémie a été prélevée 2 h après l’ad-
ministration per os de 75 g de glucose. Les patients ont alors
été répartis selon la classification OMS entre patients nor-
maux, glycémie à jeun altérée, tolérance au glucose altérée
ou diabète.
Les données des prélèvements à jeun et après HGPO ont été
disponibles pour 1 867 patients dont 47 % avaient une régula-
tion normale du glucose, 5 % une glycémie à jeun altérée,
32 % une tolérance au glucose altérée et 17 % un diabète.
Si le classement avait eu lieu en fonction des critères 1997 de
l’ADA, 39 % auraient été classés à tort comme “plus nor-
maux” qu’avec les critères actuels et, avec les critères 2004 de
l’ADA, 8 % auraient été surévalués et 33 % sous-évalués, soit
41 % d’erreurs.
>>> C’est la glycémie à 2 heures qui détermine le pronos-
tic bien plus que la glycémie à jeun
On rappellera ici que la glycémie à jeun peut être normale
bien que la glycémie à 2 h soit élevée, témoignant donc d’un
pronostic déjà aggravé comme dans les anomalies de la tolé-
rance au glucose.
Dans l’étude japonaise Funagata, seule l’intolérance au glucose
était un facteur de risque, mais pas l’anomalie de la glycémie à
jeun (la différence entre les deux portant bien évidemment sur
la glycméie à 2 h). Dans une étude finlandaise, le caractère
péjoratif de l’intolérance au glucose n’était pas modifié par
l’apparition secondaire ou non d’un diabète. La Chicago Heart
Study portant sur 12 000 hommes confirmait la différence de
pronostic entre les patients ayant des anomalies de la glycémie
après charge en glucose et les patients ayant une anomalie de la
glycémie à jeun mais sans anomalies après charge. Enfin, sur
une population mauricienne, les anomalies isolées de la glycé-
mie à 2 h doublaient le risque cardiovasculaire tandis que celles
isolées de la glycémie à jeun ne le modifiaient pas.
Enfin, dans DECODE, on rapporte que :
– la mortalité toute cause et les pathologies cardiovasculaires
étaient plus fréquentes chez les diabétiques dont le diagnostic
était porté par la glycémie à 2 h que chez les autres,
– les patients ayant des anomalies de la tolérance au glucose
avaient une mortalité plus élevée que ceux n’ayant pas d’ano-
malie glucidique ou une simple anomalie de la glycémie à jeun,
– en analyse multivariée, après ajustements aux autres fac-
teurs de risque, la glycémie à 2 h altérait le pronostic, mais pas
la glycémie à jeun, l’altération du pronostic en cas d’aug-
mentation de la glycémie à jeun n’était finalement liée qu’à
l’éventuelle augmentation associée de la glycémie à 2 h,
– la plus grande partie du surcroît de mortalité cardiovascu-
laire associée à l’élévation de la glycémie à 2 h était observée
chez ceux dont la glycémie à jeun était normale,
– l’augmentation de mortalité avec la glycémie à 2 h était
linéaire.
3. – Remarques
>>> On rappelle que l’hémoglobine glyquée n’a aucun inté-
rêt diagnostique car elle est trop imprécise pour les niveaux de
glycémie peu élevés.
>>> Les seuils diagnostiques pour le diabète ont été établis
pour des valeurs glycémiques à partir desquelles apparaît une
rétinopathie (après plusieurs années d’exposition et donc après
le risque cardiovasculaire), c’est-à-dire une microangiopathie,
et non par rapport à l’apparition d’une macroangiopathie. Une
révision des critères OMS pourrait advenir dans ce sens.
>>> Les patients ayant des anomalies de la tolérance au glu-
cose tirent parti des interventions par des mesures hygiéno-
diététiques qui retardent ou réduisent l’apparition du diabète.
>>> Le syndrome métabolique identifie des patients à
risque plus élevé que la population générale, mais il n’est

씰Cœur et diabète de type 2
pas prouvé que le syndrome métabolique l’appréhende
mieux que les facteurs de risque classiques. Il est par
ailleurs d’autant plus difficile de se servir de ce concept que
depuis sa description initiale par Reaven en 1988, pas
moins de cinq définitions officielles ont été proposées
(OMS en1998 puis 1999, EGIR en 1999, NCEPIII en 2001,
AACE en 2003, IDF en 2005…).
❚❚ POINTS FORTS DES RECOMMANDATIONS HAS
1. – Définition OMS du diabète (reprise ni plus ni moins
par l’HAS)
Le diabète est défini par une glycémie > 1,26 g/L (7 mmol/L)
après un jeûne de 8 heures et vérifiée à deux reprises, ou bien
par la présence de symptômes de diabète (polyurie, polydip-
sie, amaigrissement) associés à une glycémie (sur plasma vei-
neux) ≥ 2 g/L (11,1 mmol/L), ou encore par une glycémie
≥ 2 g/L (11,1 mmol/L) 2 h après une charge orale de 75 g de
glucose (critères proposés par l’OMS).
2. – Objectifs idéaux du traitement du diabète de type 2
La prévention et le traitement de la microangiogathie et de la
macroangiopathie diabétiques reposent sur :
>>> Des mesures hygiénodiététiques, l’exercice physique,
une perte de poids et l’arrêt du tabac.
>>> La recherche de la normalisation glycémique définie
par une hémoglobine glyquée (HbA1c) inférieure à 6,5 %
(norme du sujet sain allant jusqu’à 5,5 ou 6 %).
>>> Pression artérielle < 130/80 mmHg : chacune des
5 classes thérapeutiques (IEC, ARA2, thiazidique, bêtablo-
quant cardiosélectif, inhibiteur calcique) peut être utilisée en
première intention en monothérapie ; le plus souvent une
polythérapie incluant un thiazidique est nécessaire. On peut
remarquer que l’accent n’est pas particulièrement mis sur les
antagonistes du SRAA (NDLR).
>>> LDL-cholestérol
●L’objectif de LDL-cholestérol < 1,9 g/L n’est réservé qu’au
petit nombre de patients sans autre facteur de risque addition-
nel, dépourvus de microangiopathie (rétinienne ou rénale,
cette dernière sous forme de microalbuminurie) et dont le dia-
bète évolue depuis moins de 5 ans.
●L’objectif de LDL-cholestérol < 1,6 g/L est indiqué
chez les autres patients ayant au plus un facteur de risque
additionnel.
●L’objectif de LDL-cholestérol < 1,3 g/L est validé chez ceux
ayant au moins 2 facteurs de risque additionnels à un diabète
évoluant depuis moins de 10 ans.
●L’objectif de LDL-cholestérol < 1 g/L est recommandé en
prévention secondaire ou chez les patients à risque équiva-
lent, c’est-à-dire en cas d’atteinte rénale (albuminurie
> 300 mg/j ou DFG < 60 mL/mn), ou de diabète évoluant
depuis plus de 10 ans et au moins 2 facteurs de risque addi-
tionnels parmi les suivants :
– antécédents familiaux de maladie coronaire précoce, c’est-
à-dire infarctus du myocarde ou mort subite avant 55 ans chez
le père ou chez un parent du 1er degré de sexe masculin ou
avant 65 ans chez la mère ou chez un parent du 1er degré de
sexe féminin,
– antécédents familiaux d’AVC constitué avant 45 ans,
– tabagisme actuel ou arrêté depuis moins de 3 ans (on
remarque qu’ici on considère que 3 ans de sevrage normali-
sent donc le risque, tout au moins sur le plan cardiovascu-
laire, NDLR),
– hypertension artérielle permanente traitée ou non (on
remarque qu’ici on considère que la normalisation des
chiffres ne normalise donc pas le risque, NDLR),
– HDL-cholestérol < 0,40 g/L (1,0 mmol/L) quel que soit le
sexe,
– microalbuminurie > 30 mg/24h (on remarque donc qu’ici
on considère qu’un diabétique sans microalbuminurie n’est
pas encore vraiment à risque, NDLR),
– homme ≥ 50 ans ou femme ≥ 60 ans ou plus (le fait d’avoir
plus de 50 ans pour un homme est un facteur de risque, pas 2,
NDLR),
– le HDL-cholestérol ≥ 0,60 g/L (1,5 mmol/L) est protecteur
(on soustrait “1 risque” au score, NDLR).
>>> Il est recommandé, au vu des essais réalisés chez les
diabétiques (HPS, CARDS) ou comportant des sous-
groupes de diabétiques, d’introduire, quel que soit le LDL-
cholestérol, une statine ayant démontré une efficacité sur
la réduction du risque de complication ischémique (ator-
vastatine, simvastatine).
>>> L’administration de faibles doses d’aspirine (75 mg à
300 mg) est recommandée chez le diabétique à haut risque
cardiovasculaire en prévention primaire, en association au
traitement hypolipémiant.

Recommandations pour les troubles du métabolisme glucidique
3. – Traitement médicamenteux du diabète de type 2
>>> Education thérapeutique
C’est un volet fondamental de la prise en charge, elle doit être
mise en œuvre dès la découverte du diabète par des profes-
sionnels médecins ou paramédicaux formés à cette activité.
>>> Les médicaments destinés à normaliser la glycémie
dans le diabète de type 2
●La metformine
Elle peut normaliser ou réduire l’hyperglycémie, indépen-
damment du niveau pondéral, de l’âge et de l’ancienneté du
diabète (diminution de l’HbA1c de l’ordre de 1 à 1,5 %).
C’est le seul antidiabétique oral à avoir prouvé en monothé-
rapie une réduction de la mortalité cardiovasculaire. Elle n’in-
duit pas d’hypoglycémie par elle-même et ses effets secon-
daires les plus fréquents sont digestifs.
●Les insulinosécréteurs
* Les sulfamides hypoglycémiants : Ils sont capables de nor-
maliser ou de réduire l’hyperglycémie des diabétiques de
type 2 sans surpoids et avec surpoids (diminution de l’HbA1c
de l’ordre de 1 à 1,5 %).
* Les glinides : Le répaglinide est un insulinosécréteur d’ac-
tion rapide et de courte durée. Son pouvoir hypoglycémiant
est proche de celui des sulfamides hypoglycémiants.
* Prévention des hypoglycémies sous insulinosécréteurs : La
prévention des épisodes d’hypoglycémie est un objectif thé-
rapeutique important pour les diabétiques de type 2 traités par
sulfamide hypoglycémiant ou par glinides.
●Les glitazones (thiazolidinediones)
Elles réduisent l’insulinorésistance musculaire et hépatique et
ont fait la preuve de leur effet hypoglycémiant en monothéra-
pie (baisse de l’HbA1c de l’ordre de 1 %) ainsi qu’en bithé-
rapie, en association à la metformine ou aux sulfamides hypo-
glycémiants, et en trithérapie avec la metformine et un
insulinosécréteur. Elles n’induisent pas d’hypoglycémie par
elles-mêmes. Les antécédents d’insuffisance cardiaque
(classes I à IV) sont une contre-indication formelle aux glita-
zones, il existe des observations d’œdème maculaire survenu
ou aggravé sous rosiglitazone et pioglitazone.
●Les inhibiteurs des alphaglucosidases intestinales
Ils ralentissent l’absorption intestinale des glucides alimen-
taires complexes, ils réduisent l’HbA1c de l’ordre de 0,5 à
1 % et sont surtout actifs sur la glycémie post-prandiale (celle
qui est le meilleur marqueur du pronostic, NDLR). Leurs
effets secondaires sont digestifs et fréquents, sans gravité.
●L’insulinothérapie du diabète de type 2
L’insuline est capable de réduire, voire de normaliser les glycé-
mies des diabétiques de type 2 avec ou sans surpoids. Elle est
capable de diminuer au long cours la survenue des complications
microangiopathiques oculaires et rénales (étude UKPDS). L’hy-
poglycémie est l’effet secondaire le plus fréquent. La prise de
poids sous insuline est très variable et en général proche de celle
observée avec les sulfamides hypoglycémiants et les glitazones.
4. – Stratégie thérapeutique (tableau II)
La stratégie décrite ci-dessous concerne plus particulièrement
le diabète découvert précocement, dont la glycémie initiale et
l’HbA1c ne sont pas très élevées :
>>> HbA1c comprise entre 6 % et 6,5 % après 6 mois de
mesures hygiénodiététiques
La metformime est recommandée, donc avant le seuil de
6,5 %.
>>> HbA1c > 6,5 % malgré 6 mois de mesures hygiéno-
diététiques : monothérapie au choix
Ce délai de 6 mois peut être ramené à 3 mois si l’hyperglycé-
mie est plus importante. Quand l’HbA1c est > 6,5 %, on débu-
tera en priorité par une monothérapie : metformine et, en cas
d’intolérance ou de contre-indication, inhibiteurs de l’alpha-
glucosidase (surtout si hyperglycémie post-prandiale). Si l’in-
dice de masse corporelle est inférieur à 27, on pourra opter en
première intention pour un insulinosécréteur (sulfamide ou
glinide), et en particulier si l’hyperglycémie est plus marquée
et le risque hypoglycémique plus faible.
>>> HbA1c > 6,5 % après 6 mois de monothérapie : bithé-
rapie
Les propositions sont les suivantes :
– metformine + insulinosécréteur,
– metformine + glitazone,

씰Cœur et diabète de type 2
– metformine + inhibiteur des alphaglucosidases,
– insulinosécréteur + glitazone, en cas d’intolérance ou
contre-indication à la metformine,
– ou encore insulinosécréteur + inhibiteurs des alphaglucosidases
(en cas d’hyperglycémie post-prandiale importante mais avec une
moindre efficacité sur l’HbA1c que les autres associations).
Le rapport bénéfice/risque est moins bien évalué pour les
nouveaux hypoglycémiants comme les glitazones, compara-
tivement aux anciens.
>>> HbA1c > 7 % après 6 mois de bithérapie: trithérapie
On proposera :
– soit un essai d’une trithérapie orale : metformine + insulino-
sécréteur + glitazone, bien que cette association demande à
être évaluée dans la durée. L’objectif est une HbA1c < 7 %,
– soit d’opter d’emblée (hors bithérapie incluant une glita-
zone) pour l’adjonction d’insuline, injection unique d’une
insuline intermédiaire (NPH) ou d’un analogue lent le soir.
L’autosurveillance glycémique devra alors être introduite si
elle ne l’était pas encore.
>>> HbA1c ≥ 8 % : insulinothérapie du diabète de type 2
(avec interruption des glitazones devenant contre-indiquées
en association à l’insuline). Ajout à une bithérapie orale au
coucher d’une insuline intermédiaire (NPH) ou d’un analogue
lent. L’insulinothérapie doit faire recourir au diabétologue et
de façon indispensable à l’étape de l’insulinothérapie frac-
tionnée (> 1 injection).
5. – Les situations particulières
>>> Sujet âgé (âge > 75 ans et selon l’âge physiologique)
L’objectif d’HbA1c est plus élevé si le diabète d’apparition
tardive et/ou si l’espérance de vie est réduite.
>>> Diabète découvert plus tardivement
Quel que soit l’âge, en présence d’une glycémie haute, de
complications, et en l’absence d’erreurs diététiques impor-
tantes, on envisage d’emblée une bithérapie metformine
+ sulfamide hypoglycémiant (effet hypoglycémiant plus rapi-
dement atteint), voire une insuline si contre-indication d’une
ou de plusieurs classes d’antidiabétique oral.
6. – Place de l’autosurveillance glycémique
Le groupe de travail recommande l’autosurveillance glycémique:
– chez tous les patients insulinotraités,
– chez les patients traités par insulinosécréteur afin de recher-
cher ou confirmer une hypoglycémie et d’adapter si besoin la
posologie de ces médicaments,
– chez les patients pour lesquels l’insuline est envisagée à
court ou moyen terme. ■
Seuil de prescription Stratégie thérapeutique Objectif
HbA1c > 6 % Etape 1 HbA1c < 6 %
Mesures hygiénodiététiques (MHD)
Si malgré étape 1, HbA1c > 6 % Etape 2 Maintenir l’HbA1c < 6,5 %
(à la phase précoce du diabète) Monothérapie + MHD : Metformine, voire IAG
Si malgré étape 1, HbA1c > 6,5 % Monothérapie au choix + MHD
Metformine ou IAG ou SU ou glinides ou IAG
Si malgré étape 2, HbA1c > 6,5 % Etape 3 Ramener l’HbA1c < 6,5 %
Bithérapie + MHD
Si malgré étape 3, HbA1c > 7 % Etape 4 Ramener l’HbA1c < 7 %
Thrithérapie + MHD ou insuline ± ADO
+ MHD
Si malgré étape 4, HbA1c > 8 % Etape 5 Ramener l’HbA1c < 7 %
Insuline ± ADO + MHD Insuline fractionnée
+ MHD
Tableau II : Tableau synthétique d’après les recommandations (HAS décembre 2006). ADO = antidiabétiques oraux, IAG = Inhibiteurs des alphaglucosidases,
SU = sulfamides hypoglycémiants, insuline + ADO = mise à l’insuline : intermédiaire ou lente le soir ; insuline fractionnée : > 1 injection/j soit 2 à 4.
1
/
5
100%