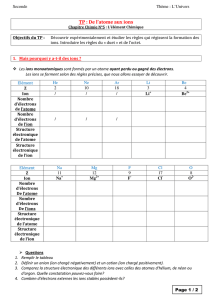
Ion Un ion (du grec iôn, « qui va ») est constitué à partir d`un atome

Ion
Sources : http://fr.wikipedia.org/wiki/Ion - http://phys.free.fr/ions.htm -
Un ion (du grec iôn, « qui va ») est constitué à partir d'un atome ou un groupe d'atomes (molécule) qui a
gagné ou perdu un ou des électrons (charges négatives). Le noyau d'un ion monoatomique a le même
nombre de protons (Z) et le même nombre de neutrons que l'atome correspondant, mais en diffère par le
nombre d'électrons ; c'est pourquoi on le note avec le même symbole mais complété par la charge.
Un anion est constitué d'un atome (ou groupement) ayant gagné un ou plusieurs électron(s) ; il possède
une charge électrique négative car il contient alors plus d'électrons (-) que de protons (+). Par exemple,
l'ion chlorure, noté Cl-, est l'atome de chlore (Cl) ayant gagné un électron. Un anion est un ion négatif.
Un cation est constitué d'un atome (ou groupement) ayant perdu un ou plusieurs électron(s) : il possède
une charge électrique positive car il contient alors moins d'électrons (-) que de protons (+). Par exemple,
l'ion sodium, noté Na+, est l'atome de sodium (Na) ayant perdu un électron. Un cation est un ion positif.
Règle : Tout composé chimique étant électriquement neutre, s'il contient des ions, il contient alors
nécessairement à la fois des cations et des anions. La matière étant globalement neutre, la charge des
cations est compensée par celles des anions.
Solides ioniques
Ces solides sont constitués d'un empilement alterné de cations et d'anions reliés par des liaisons dites
« ioniques » ; la cohésion de l'ensemble est assurée par les forces électrostatiques. Par exemple, le sel de
table : NaCl, (chlorure de sodium) est un empilement d'ions chlorure et d'ion sodium.
Ces solides sont facilement solubles dans l'eau ou d'autres solvants polaires, car les ions y sont facilement
solvatés (dispersés parmi les molécules du solvant). Ces solides sont des solutés.
Ionisation de composés moléculaires
Dans certains corps moléculaires, certains atomes attirent plus les électrons de liaisons que d'autres ; on
dit que les liaisons entre atomes sont polarisées. Au contact d'un solvant polaire, comme l'eau, les
molécules de ces composés tel l'acide sulfurique H2SO4, l'ammoniac NH3 ou le dioxyde de carbone CO2,
se dissocient en ions au cours de la dissolution.
Les solutions ioniques
Un liquide contenant des ions parmi le solvant est appelé solution ionique. Dans la solution, les ions se
déplacent facilement sous l'effet d'un champ électrique, d'où la forte conductibilité électrique des
solutions ioniques. Ainsi, l'eau des océans, qui constituent la plus importante réserve hydrique de la Terre,
est riche en ions :
Concentration approximative des principaux ions dans l'eau de mer normale
Ions Cl– Na+ SO42– Mg2+ Ca2+ HCO3– Br– CO32– Sr2+ F–
mg.L-1 19000 11000 2700 1300 420 110 73 15 8,1 1,3
Noms des ions

Exemples d'ions
Nom Formule
Cations métalliques
Aluminium (I) Al+
Aluminium (III) Al3+
Argent Ag+
Baryum Ba2+
Calcium Ca2+
Chrome (II) Cr2+
Chrome (III) Cr3+
Cobalt (II) Co2+
Cobalt (III) Co3+
Cuivre (I) Cu+
Cuivre (II) Cu2+
Étain (II) Sn2+
Étain (IV) Sn4+
Fer (II) Fe2+
Fer (III) Fe3+
Lithium Li+
Magnésium Mg2+
Manganèse (II) Mn2+
Manganèse (III) Mn3+
Mercure (I) Hg22+
Mercure (II) Hg2+
Nickel (II) Ni2+
Nickel (III) Ni3+
Plomb (II) Pb2+
Plomb (IV) Pb4+
Potassium K+
Sodium Na+
Strontium Sr2+
Zinc (II) Zn2+
Autres cations
Ammonium NH4+
Nitronium NO2+
Hydronium H3O+
Hydrogène H+
Nom Formule
Anions monoatomiques
Bromure Br−
Chlorure Cl−
Fluorure F−
Hydrure H−
Iodure I−
Nitrure N3−
Oxyde O2−
Sulfure S2−
Oxo-anions
Arsénate AsO43−
Arsénite AsO33−
Borate BO33−
Bromate BrO3
−
Carbonate CO32−
Chlorate ClO3
−
Chlorite ClO2
−
Chromate CrO42−
Dichromate Cr2O72−
Dihydrogénophosphate H2PO4
−
Hydrogéno-oxalate HC2O4
−
Hydrogénocarbonate HCO3
−
Hydrogénophosphate HPO42−
Hydrogénosulfate HSO4
−
Hydrogénosulfite HSO3
−
Hypobromite BrO−
Hypochlorite ClO−
Nitrate NO3
−
Nitrite NO2
−
Oxalate C2O42−
Perchlorate ClO4
−
Phosphate PO43−
Phosphite PO33−
Sulfate SO42−
Sulfite SO32−
Thiosulfate S2O32−
Nom Formule
Anions issus d'acides
organiques
Acétate C2H3O2
−
Ethanoate
Formate HCO2
−
Méthanoate
Autres Anions
Amide NH2
−
Cyanate CNO−
Cyanure CN−
Hydrogénosulfure HS−
Hydroxyde OH−
Oxalate C2O42−
Permanganate MnO4
−
Peroxyde O22−
Thiocyanate SCN−
Ou bicarbonate

1
/
3
100%