GENERALITES SUR LES V ENERALITES SUR LES VIRUS

G
GG
GENERALITES SUR LES V
ENERALITES SUR LES VENERALITES SUR LES V
ENERALITES SUR LES VIRUS
IRUSIRUS
IRUS
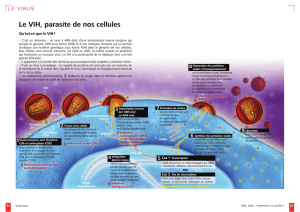
Les maladies d’origine virale ont engendré de grandes épidémies aux cours de l’histoire humaine (rage,
variole, grippes…). Pourtant, les agents infectieux responsables des ces épidémies sont longtemps restés
inconnus des scientifiques.
En 1892, Ivanowski montre que des extraits de feuilles de tabac présentant une maladie appelée
« mosaïque du tabac » induisent la même maladie chez des plants de tabac sains. Ces extraits ayant été
filtrés pour éliminer les bactéries, l’agent infectieux responsable de la maladie fût appelé « virus
filtrant ».
La nature et les propriétés des virus ne furent établies qu’au milieu du XX
e
siècle lorsque Enders montre
que les virus peuvent être cultivés sur des cellules. La production et la purification de grandes quantités
de particules virales permet dès lors l’étude des caractères communs à ce groupe d’agents infectieux.
En 1953, Lwoff propose une définition d’une particule virale complète ou virion :
1. un virion ne possède qu’un seul type d’acide nucléique, soit de l’ADN, soit de l’ARN ;
2. il virion se reproduit à partir de son seul acide nucléique ;
3. il est incapable de croître et de subir des divisions binaires ;
4. il ne possède aucune information génétique concernant les enzymes du métabolisme intermédiaire
producteur d’énergie ;
5. sa multiplication nécessite l’utilisation des structures de la cellule hôte, notamment de ses
ribosomes.
Le virion est donc l’unité structurale des virus, composée d’une molécule d’acide nucléique, d’une
capside, et, dans certains cas, d’une enveloppe. En microscopie électronique, les virions apparaissent
sous forme de figure géométrique simple.
Les virus sont différents des cellules vivantes :
- ils ont une organisation simple et acellulaire ;
- il n’y a jamais présence d’ADN et d’ARN ensemble dans le même virion ;
- ils sont incapables de se multiplier indépendamment en dehors d’une cellule hôte : ce sont des
parasites intracellulaires stricts.

1. Structure des virus
1.1. L’enveloppe
Il s’agit d’une structure facultative, puisque l’on distingue les virus enveloppés et les virus non
enveloppés (« nus »). Cependant, de nombreux virus animaux présentent cet élément structural.
L’enveloppe, ou peplos, provient principalement d’une des membranes de la cellule hôte (membrane
plasmique ou membranes de l’enveloppe nucléaire). Elle est donc principalement constituée de
phospholipides. Mais des protéines (ou des glycoprotéines) codées par le génome viral sont
généralement insérées dans l’enveloppe, formant des à l’extérieur du virion des spicules. Ces molécules
ont des propriétés antigéniques et sont également impliquées dans la reconnaissance des cellules
sensibles.
Figure 1 : Schéma d’un virus Influenza.
1.2. La capside
La capside est une structure protéique qui entoure et protège l’acide nucléique viral. Elle est composée
de sous-unités (identiques ou non) appelées protomères. Le nombre de protomères est constant chez un
virus, et leur assemblage conduit à l’édification de structures cylindriques, polyédriques ou complexes.
1.2.1. Capsides hélicoïdales
Les unités protéiques sont assemblées en hélice autour de l’acide nucléique, formant ainsi une
nucléocapside. La capside du virus de la mosaïque du tabac (TMV) est un assemblage de sous-unités
protéiques identiques (158 acides aminés par sous-unité). L’arrangement en spirale des protomères se fait
par auto-assemblage.

Figure 2
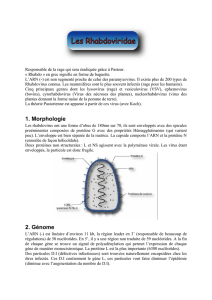
Figure 3 : photographie et schémas d’un Rhabdovirus.
1.2.2. Capsides polyédriques
Dans les capsides polyédriques, les protomères forment des anneaux appelés capsomères. L’assemblage
des capsomères conduit à la formation d’une structure régulière, dont la symétrie est dite cubique. De
nombreux virus présentent une capside icosaèdrique, constituée de 20 faces triangulaires et de 12
sommets. Un assez grand nombre de virus à symétrie cubique possèdent des protéines internes associées à
leur génome et constituant un nucléoïde.

Figure 4
1.2.3. Capsides complexes
Tous les virus ne présentent pas une symétrie définie. Les Poxvirus sont de grands virus animaux d’aspect
ovoïdes tandis que les bactériophages T pairs sont des virus bactériens pourvus d’une structure très
élaborée.
Figure 5

1.3. L’acide nucléique
Le matériel génétique d’un virus peut être :
- de l’ADN ou de l’ARN ;
- simple brin et/ou double brin ;
- linéaire ou circulaire ;
- segmenté ou non segmenté ;
- de taille variable selon les virus (1 000 à 250 000 nucléotides).
1.3.1. Virus à ADN
Figure 6
1.3.2. Virus à ARN
Il existe trois grands types de virus à ARN : les virus à ARN positif, les rétrovirus et les virus à ARN
négatif.
Un ARN positif présente une séquence nucléotidique identique à celle de l’ARN messager viral. Si
cet ARN possède, comme les ARN messagers eucaryotes, une coiffe en 5’ et une queue polyA en 3’,
celui-ci peut être directement traduit en protéines au niveau des ribosomes cellulaires.
Les rétrovirus sont pourvus d’un ARN+, mais celui-ci n’est pas directement traduit : il copié en ADN
qui de plus, s’intègre au génome cellulaire.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
1
/
18
100%