Terminale S3 – M. Salane – Année scolaire: 2014/2015
Visiter le site http://physiquechimie.sharepoint.com
- 1 -
COMPOSITION DU 1er SEMESTRE DE SCIENCES PHYSIQUES
Exercice 1 : (03 points)
On dispose d'un alcool A de formule C4H100
1) A peut donner un corps B pouvant réduire la liqueur de Fehling et donner une
réaction de précipitation avec la dinitrophénylhydrazine (DNPH).
a) Donner le nom et la formule de B sachant que sa chaîne est linéaire. (0,5 pt)
b) Quel est le nom et la classe de l'alcool A ? (0,5 pt)
2) L’oxydation de B peut donner un produit organique D.
Donner la formule semi-développée et le nom de D. (0,5 pt)
3) D réagit avec le chlorure de thionyle (SOCl2) en donnant un corps E.
Quel est le nom du corps E ? Donner l'équation de la réaction ? (0,5 pt)
4) Deux molécules du corps D, en présence d'un déshydratant efficace tel que le P4O10,
peuvent donner un corps F. Quelle est la formule semi-développée de F ? (0,5 pt)
5) On peut obtenir un ester soit :
a) par action de E sur A
b) par action de F sur A
Ecrire les équations des réactions. (0,5 pt)
Exercice 2 : (03 points)
On étudie, à température constante, la cinétique de dismutation de l’eau oxygénée :
2 H2O2 2 H2O + O2
1) A la date t = 0, la solution contient 0,060 mole d’eau oxygénée. Son volume,
constant, est VS = 1 L. On mesure, à pression constante, le volume V(O2) de gaz
dégagé au cours du temps.
a) Exprimer, en mole, la quantité de dioxygène n(O2) formé à la date t en fonction de
V(O2) et de Vm = 24 L.mol-1 (volume molaire d’un gaz à la température de
l’expérience). (0,25 pt)
b) En déduire, à la même date t, la quantité de H 2O2 disparu, puis la concentration C en
eau oxygénée restante. (0,5 pt)
c) Les résultats de l’expérience sont dans le tableau suivant :
t en min
0
5
10
15
20
25
30
35
40
80
V(O
2
) en L
0
0,16
0,27
0,36
0,44
0,50
0,54
0,59
0,61
0,68
C en mol.L
-1
0,06
Compléter la tableau et tracer le graphe C = f (t). (0,75 pt)
d) Définir la vitesse volumique v (t) de disparition de H2O2 à la date t.
Calculer cette vitesse à la date t1 = 10 min puis à la date t2 = 30 min. Quel facteur
cinétique explique la variation de la vitesse de disparition de H2O2 ? (0,75 pt)
2) Une étude complète montre que v(t) est liée à la concentration C par une relation de
type : v = k.C avec k = 7,9.10-4 S.I.
a) Cette relation permet-elle de retrouver v (30 min) de la question 1.d ? (0,25 pt)
b) Prévoir d’après les résultats du cours comment évolue la constante k en fonction de
la température. (0,25 pt)
c) Tracer qualitativement l’allure du graphe si on opérait en présence du catalyseur
Fe2+ ? (Définir un catalyseur). (0,25 pt)

Visiter le site
Exercice 3 : (05
points)
Le dispositif étudié est constitué d'un fil de
masse négligeable et de longueur
dont une des extrémités, C, est fixe. A l'autre
extrémité est attachée une petite boule (B
masse m1
= 40 g assimilable à un point
matériel.
Une autre petite boule (B2
) supposée
ponctuelle, de masse m2
= 20 g est posée sur
le rebord d'une tab
le de hauteur H = 80 cm.
La boule (B1
) est amenée au point A, le fil
occupant la position CA telle que l'angle
= 60°, puis elle est abandonnée à elle
On négligera l'influence de l'air.
1) Avec quelle vitesse v1
la boule (B
au point O ?
2) Calculer la tension T du fil
quand la boule (B
3)
En admettant que le choc est parfaitement élastique, calculer la vitesse
(B2) juste après le choc.
4) Donner, dans le repère (O,
i
choc puis établir l'équation cartésienne de sa trajectoire dans ce même repère et dire
quelle est sa nature ?
5)
Calculer les coordonnées du point I d'impact de la boule (B
la durée de son mouvement entre les points O et I
Exercice 4 :
(04 points)
On considère une planète P de masse M. Le mouvement de l'un de ses satellites S,
assimilé à un point matériel de masse m, est étudié dans un référentiel considéré
comme galiléen, muni d'un repère
P et les trois axes dirigés vers trois étoiles fixes.
On admet que la planète a une distribution de masse à symétrie sphérique et que
l'orbite de son satellite est un cercle de centre O et de rayon r.
1)
Donner les caractéristiques de la force de gravitation
le satellite S. Faire un schéma.
2)
Donner l'expression du champ de gravitation
trouve le satellite S. Représenter ce vecteur de gravitation
précédent.
3) Déterminer la natur
e du mouvement dans le référentiel d'étude précisé
4)
Exprimer le module de la vitesse V et la période de révolution T du satellite S en
fonction
de la constante de gravitation K
de la masse M
de la planète P.
Terminale S3 – M. Salane –
Année scolaire:
Visiter le site
http://physiquechimie.sharepoint.com
points)
Le dispositif étudié est constitué d'un fil de
masse négligeable et de longueur
ℓ = 90 cm
dont une des extrémités, C, est fixe. A l'autre
extrémité est attachée une petite boule (B
1) de
= 40 g assimilable à un point
) supposée
= 20 g est posée sur
le de hauteur H = 80 cm.
) est amenée au point A, le fil
occupant la position CA telle que l'angle
= 60°, puis elle est abandonnée à elle
-même sans vitesse initiale.
On négligera l'influence de l'air.
On donne : g = 10 N.kg
-1
.
la boule (B
1) vient-elle heurter la boule (B2
) placée
quand la boule (B
1
) passe par le point O.
En admettant que le choc est parfaitement élastique, calculer la vitesse
,
j
) l'équation du mouvement de la boule (B
choc puis établir l'équation cartésienne de sa trajectoire dans ce même repère et dire
Calculer les coordonnées du point I d'impact de la boule (B
2
) sur le sol puis calculer
la durée de son mouvement entre les points O et I
sachant que v2
= 4
(04 points)
On considère une planète P de masse M. Le mouvement de l'un de ses satellites S,
assimilé à un point matériel de masse m, est étudié dans un référentiel considéré
comme galiléen, muni d'un repère
dont le centre coïncide avec le centre O de la planète
P et les trois axes dirigés vers trois étoiles fixes.
On admet que la planète a une distribution de masse à symétrie sphérique et que
l'orbite de son satellite est un cercle de centre O et de rayon r.
Donner les caractéristiques de la force de gravitation
⃗
exercée par la planète P sur
le satellite S. Faire un schéma.
Donner l'expression du champ de gravitation
⃗ créé par
la planète P au point où se
trouve le satellite S. Représenter ce vecteur de gravitation
⃗
sur le schéma
e du mouvement dans le référentiel d'étude précisé
Exprimer le module de la vitesse V et la période de révolution T du satellite S en
de la constante de gravitation K, du rayon r de la trajectoire du satellite S et
de la planète P.
Année scolaire:
2014/2015
- 2 -
) placée
(0,75 pt)
) passe par le point O.
(1 pt)
En admettant que le choc est parfaitement élastique, calculer la vitesse
v2 la boule
(0,75 pt)
) l'équation du mouvement de la boule (B
2) après le
choc puis établir l'équation cartésienne de sa trajectoire dans ce même repère et dire
(1,5 pt)
) sur le sol puis calculer
= 4
m.s-1. (1 pt)
On considère une planète P de masse M. Le mouvement de l'un de ses satellites S,
assimilé à un point matériel de masse m, est étudié dans un référentiel considéré
dont le centre coïncide avec le centre O de la planète
On admet que la planète a une distribution de masse à symétrie sphérique et que
exercée par la planète P sur
(0,5 pt)
la planète P au point où se
sur le schéma
(0,5 pt)
e du mouvement dans le référentiel d'étude précisé
. (0,5 pt)
Exprimer le module de la vitesse V et la période de révolution T du satellite S en
, du rayon r de la trajectoire du satellite S et
(1 pt)

Terminale S3 – M. Salane – Année scolaire: 2014/2015
Visiter le site http://physiquechimie.sharepoint.com
- 3 -
états d'immobilité
B
B
B
A
A
A
m
m
x
x’
O
Ω
Ω
M
⃗
figure I
figure II
figure
III
état de mouvement
5) Montrer que le rapport r3
T2 est une constante. (0,5 pt)
6) Sachant que l'orbite du satellite S a un rayon r = 185 500 km et que sa période de
révolution vaut T = 22,6 heures, déterminer la masse M de la planète P. (0,5 pt)
7) Un autre satellite S' de la planète P a une période de révolution T' = 108,4 heures.
Déterminer le rayon r' de son orbite. (0,5 pt)
On donne : la constante gravitationnelle K = 6,67.10-11 SI.
Exercice 5 : (05 points)
Données : b = 3 cm ; m = 100 grammes ; k1 = 10 N.m-1 ; k2 = 5 N.m-1.
On dispose de deux ressorts de masses négligeables et de constantes de raideur k1 et k2.
On suspend le ressort n° 1 à un crochet
A, et le ressort n°2 à un point B du sol
(figure I), les ressorts gardent toujours la
direction verticale.
Sur un axe vertical x’Ox dirigé vers le haut,
on repère par 1 et 2 les positions des
extrémités libres des ressorts n°1 et n°2
(les ressorts ne sont ni étirés, ni comprimés).
On accroche les extrémités libres des
ressorts à une masse m supposée
ponctuelle (figure II).
On repère la position de la masse m, à l'équilibre par le point O sur l'axe x’Ox.
On écarte, vers le haut, la masse m d'une longueur b.
A l'instant t = 0 on le lâche sans vitesse initiale.
On repère la position de la masse durant son mouvement à un instant t par le point M
avec
⃗
= ⃗ (figure III)
1) Trouver l'équation différentielle du mouvement de la masse m. (1,5 pt)
2) Trouver la solution de cette équation x(t) en fonction des paramètres b, k1, k2 et m.
Donner l'expression numérique de x en fonction de t. (0,5 pt)
3) Calculer la période T des oscillations et la fréquence N. (0,5 pt)
4) Exprimer l’énergie potentielle de ce système à un instant t quelconque. On choisira
l'origine de l'énergie potentielle de pesanteur Ep = 0 pour M en O (x = 0). (1 pt)
5) Exprimer l’énergie cinétique du système à un instant t quelconque. En déduire
l’énergie mécanique totale E. Que peut-on en dire ? (1,5 pt)

Terminale S3 – M. Salane – Année scolaire: 2014/2015
Visiter le site http://physiquechimie.sharepoint.com
- 4 -
CORRECTION
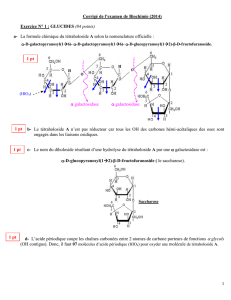
Exercice 1 :
1)
a) B : CH3-(CH2)2-CHO butanal
b) A : butan-1-ol (alcool primaire)
2) D : CH3-(CH2)2-CO2H acide butanoïque
3) E : chlorure de butanoyle;
CH3-(CH2)2-CO2H + SOCℓ2 ⟶ CH3-(CH2)2-COCℓ + HCℓ + SO2
4) CH3-(CH2)2-CO-O-OC-(CH2)2- CH3
5) E + A ⟶ CH3-(CH2)2-CO-O-(CH2)3- CH3 + HCℓ
F + A ⟶ CH3-(CH2)2-CO-O-(CH2)3- CH3 + D
Exercice 2 :
1)
a) =()
b) ()=()
; =−()
=,−()
c)
t(min)
0
5
10
15
20
25
30
35
40
80
C (10
-2
mol.L
-1
)
6
4,7
3,75
3
2,3
1,8
1,5
1,1
0,9
0,3
Echelle : 1 cm pour 5 min et 1 cm pour 0,5.10-2 mol/L.
d) Définition : la vitesse instantanée est l’opposée de la dérivée par rapport au temps de
la concentration de l’eau oxygénée.
Valeurs : graphiquement la vitesse instantanée correspond à l’opposé du coefficient
directeur de la tangente à la courbe à l’instant t considéré.
Ainsi graphiquement on a :
v10 = 1,7.10-3 mol.L-1.min-1 ; v30 = 0,7.10-3 mol.L-1.min-1
La vitesse diminue avec la concentration du réactif.
2)
a) v30 = 7,9.10-4 x 1,5.10-2 = 1,185.10-5 mol.L-1.s-1
Or graphiquement on a : v30 = 0,7.10-3 mol.L-1.min-1 = 1,17.10-5 mol.L-1.s-1
La relation proposée permet bien de trouver la vitesse de disparition de H2O2.
b) Quand la température augmente, la vitesse croit donc k croit.
c) Catalyseur : substance qui augmente la vitesse d’une réaction chimique sans paraître
participer à cette réaction.
Exercice 3 :
1) TEC : =(− )= /
2) TCI :
⃗
+
⃗
=⃗⟹=
+=,
3) Conservation de la quantité de mouvement :
⃗
=
⃗
+
⃗
⟹
=
+
(1)
Conservation de l’énergie cinétique :

Terminale S3 – M. Salane – Année scolaire: 2014/2015
Visiter le site http://physiquechimie.sharepoint.com
- 5 -
=
′
+
(2)
En combinant les équations (1) et (2), on trouve :
=
=/
4) TCI : ⃗=⃗⟹
⃗
=
=
⟹=
=,.
; Nature : parabole
5) =
=,
==, ; =
=,
Exercice 4 :
1) ⃗ s’applique sur le satellite et est centripète.
2)
⃗
=−
⃗
3) TCI : ⃗=⃗ ⟹⃗=
⃗
∶
4) an = G ⟹=
; =
5)
=
=constant
6) =
=,.
7)
=
⟹=
=,.
Exercice 5 :
1) A l’équilibre (au point O) :
⃗
+
⃗
+
⃗
=0
⃗
⟹ −+ −=0 avec =Ω =Ω
En mouvement (au point M), TCI :
⃗
+
⃗
+
⃗
=⃗⟹ − + (−)−(+)=̈
⟹̈+
=
=+
2) =(+ ) =0 (à partir des conditions initiales)
=⟹=
=, ; x(cm) et t(s).
3) =
=0,513s ; N =
=,
4) Ep = Epp + Epe ⟹=+
(−)+
(+)⟹
=
(+)+
+
5) Ec =
̇; E = Ec + Ep ⟹ E =
̇+
(+)+
+
Avec = et ̇=−⟹
E =
(+)+
+
=.
1
/
5
100%