Sciences physiques Devoir De Synthèse N°1 Classes : 4ème Sc – 2-
Lycée de l’Environnement Prof : Mr : khalfi sabeur
Beja Année scolaire : 20019/2020 Durée : 3 Heures
CHIMIE (9 Points) :
EXERCICE N°1 (5,5 Points) :
On désire étudier la réaction d’estérification de l’acide éthanoïque CH3COOH par le méthanol CH3OH.
Pour cela on réalise dans 10 tubes scellés, à l’instant t = 0 , n1 mole d’acide et
n
2 mole d’alcool.(n2<
n
1)
avec deux gouttes d’acide sulfurique concentré. On place immédiatement les tubes dans un bain-marie
maintenu à une température de 80°C .
A divers instants repérés, le contenu d’un tube est versé dans de l’eau glacée puis dosé à l’aide d’une solution
d’hydroxyde de sodium ( Na OH) de concentration CB = 2 mol.L-1.
La courbe du figure 1 traduisant l’évolution du nombre
de mole d’acide éthanoïque présents dans
le mélange en fonction du temps. n(AC)=f(t)
1- a- Ecrire l’équation de la réaction d’estérification, donner ses caractères.
b- Quels sont les effets des actes suivants :
des tubes capillaire?
2- a - Dresser le tableau descriptif d’évolution du système chimique étudié.
b - Déterminer graphiquement
:
- la quantité de matière initiale
n
1 de l’acide
éthanoïque.
- la quantité de matière nf de l’acide éthanoïque présent dans le mélange à la fin de la
réaction.
c - Déterminer l’avancement final xf de la réaction d’estérification.
3- Le taux d’avancement finale de la réaction est f = 0.845
a. Déterminer la valeur de n2 .
b. Exprimer la constante d’équilibre K de la réaction en fonction de n1 , n2 et xf . Calculer sa valeur.
4- Dans une deuxième expérience, on mélange à t=0min n0 mole d’acide et
n
0 mole d’alcool
a. Déterminer la valeur du taux d’avancement final 'f .
b. Comparer 'f à f et en déduire, comment aurait-on pu augmenter le taux d’avancement final de la
réaction d’estérification.
5- On souhaite déplacer l’équilibre c’est à dire faire évoluer le mélange vers un nouvel état d’équilibre où
les proportions des constituants sont 0,1 mol d'acide éthanoïque et 0,1 mol d'éthanol, 0,2 mol
d'ester et n mol d'eau. Déterminer les valeurs de n pour que le système évolue dans le sens de
l’hydrolyse.
tube
capillaire
bain –
marie
à 80°C
1
10

EXERCICE N°2 (3,5 Points)
On considère l’équilibre de dissociation de l’ammoniac représenté par l’équation suivante :
2 NH3 (gaz) 3 H2 (gaz)+ N2(gaz)
1. A une température T, on introduit n0 = 2 mol d’ammoniac (NH3) dans un récipient de volume V =190 L.
a- Dresser le tableau descriptif d’évolution du système chimique étudié
b- Exprimer la constante d’équilibre K en fonction de n0, xf et v (xf étant l’avancement finale de la réaction)
Calculer sa valeur sachant qu’à l’équilibre Le taux d’avancement finale f = 0,45.
2. A une température T ' < T, Le taux d’avancement finale 'f = 0,38. Indiquer le caractère
énergétique de la réaction de dissociation d’ammoniac. Justifier la réponse.
3. Quelle est l'influence d'une augmentation de pression, à température constante, sur :
l’équilibre du système chimique
La valeur de f
La valeur de K.
Physique (11 Points) :
EXERCICE N°1 ( 4 pts)
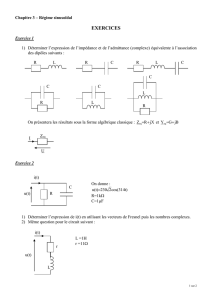
On réalise le circuit électrique représenté par la figure 2 comportant , en série, un générateur idéal de
tension de f.e.m E, une bobine d’inductance L et de résistance r, un interrupteur K et un résistor de
résistance R.
A la date t=0 on ferme l’interrupteur K et à l’aide d’un oscilloscope à mémoire,
on enregistre la tension uB aux bornes de la bobine, on obtient le
chronogramme de la figure 3 .
1- Indiquer le branchement de l’oscilloscope qui permet de visualiser la
tension uB(t) aux bornes de la bobine.
2- Etablir l’équation différentielle régissant les variations de l’intensité du
courant électrique i(t) dans le circuit.
3- Vérifier que i(t) = E
(r+R).(1- e-t/) est une solution de l’équation
différentielle précédemment établie avec = L
(R+r).
4- Prélever du graphe de la figure 3 la fem E du générateur et la constante de temps .
5- Lorsque le régime permanent s’établit, l’intensité du
courant électrique dans le circuit est Ip=0,2A
a- Etablir l’expression de la tension uB lorsque le régime
permanent s’établit. Déduire la valeur de r.
b- Déterminer la valeur de la résistance R.
c- Montrer que l’inductance L de la bobine est égale à
0,15H.
R
L,r
K
E
i
Figure-2-

EXERCICE N°2 ( 5 pts)
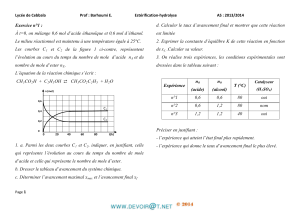
Avec un générateur de tension idéal de f.é.m U0, un condensateur initialement déchargé de capacité
C=2,5μF et une bobine d’inductance L et de résistance r, on réalise le montage électrique schématisé par
la figure 1. L’inverseur k est en position 1.
A une date t=0 on bascule k en position 2. La figure-2 représente l’évolution de uC(t).
1°)
a- Dans quel régime fonctionne le circuit ?
b- Prélever la valeur de la pseudo-période T.
c- Sachant que l’on peut assimiler la pseudo-période des oscillations à la période propre T0 du circuit
oscillant (L,C ), calculer l’inductance L de la bobine.
2°)
a -Etablir l’équation différentielle régissant les variations de la tension uC(t) aux bornes du condensateur.
b- Rappeler l’expression de l’énergie totale de cet oscillateur et montrer qu’elle diminue au cours du
temps.
c- Calculer l’énergie dissipée sous forme thermique pendant la durée ∆t=t2-t1 .
3°) On refait la même expérience en remplaçant la bobine précédente par une autre bobine d’inductance L’
et de résistance négligeable tout en conservant le même condensateur.
a - Etablir l’équation différentielle régissant l’évolution de la charge q(t).
b - Sachant que q(t) = Qm sin(
t
q
)
. En déduire les équations horaires de i(t) et uC(t) en
fonction de Qm, C, t et q.
c - Montrer que l’énergie totale du circuit reste constante au cours du temps.
d - La figure-3 représente les évolutions au cours du temps de uC(t) et i(t).
Montrer que la courbe C1 est celle de uC(t) et C2 est celle de i(t).
En déduire les valeurs numériques de : Qm , et L’.
figure 2
figure 1
figure-3

Etude d’un document scientifique
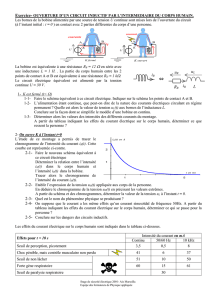
Les plaques de cuisson par induction, ou plaque à induction, ont un fonctionnement
nettement différent des plaques de cuissons classiques malgré qu’elles doivent êtres
branchées à la prise du secteur. La première caractéristique frappante des plaques à
induction c’est qu’en fonctionnement elles sont froides, ou très peu chaude ! A l’inverse
des plaques classiques, ce ne sont pas les plaques qui chauffent dans un système à
induction mais la casserole, elle même.
Ce type de plaque fonctionne donc grâce aux phénomènes d’induction. C’est en 1831
que Michael Faraday découvre qu’un
courant électrique
est créé dans un
conducteur
lorsqu’il
est
soumis
à un
champ magnétique variable.
C’est exactement ce qui se passe
lorsque vous approchez votre casserole de la plaque, le champ magnétique variable, créé
par le générateur (une bobine placé sous la plaque), engendre un courant électrique
dans la paroi de la casserole. Cette dernière étant conductrice, elle s’échauffe par effet
Joule. La chaleur se transmet au contenu de la casserole, et c’est ainsi que les aliments
sont cuits.
Malheureusement ce type de plaque est encore chère, et nécessite d’utiliser des casseroles
compatibles.
D’après : © 2006-2007 BRARD Emmanuel
Questions : 2 points
1/ Qu’est ce qui constitue le circuit où circule le courant induit dans le dispositif d’une
plaque de cuisson Par induction en fonctionnement?
2/ Préciser l’induit et l’inducteur dans le dispositif d’une plaque de cuisson à induction en
fonctionnement?
3/ Pour que la plaque à induction puisse fonctionner on doit la brancher à une prise du
secteur alternatif. Expliquer pourquoi ?
1
/
4
100%