Collège Sadiki
Suivi temporel d’une réaction chimique et vitesse d’une
réaction.
T.P chimie 1
1
http://cherchari.legtux.org/ Obey-Cherchari
1°/ Objectifs :
+ Suivre l’avancement d’une réaction chimique par une méthode chimique(Dosage iodométrique).
+ Déterminer la vitesse moyenne et la vitesse instantanée de la réaction d’oxydation des ions I- par les
ions peroxodisulfate S2O82-.
2°/ Expériences à réaliser
- Noter les couleurs des solutions d’iodure de potassium KI et de peroxodisulfate de potassium
K2S2O8.
- Mélanger ces deux solutions et noter la couleur du mélange. Ecrire les équations des deux demi
réactions et l’équation bilan de la réaction.
- Au mélange précédent, ajouter un peu d’empois d’amidon et noter la nouvelle couleur. (
Remarquer que l’empois d’amidon avec le KI ou avec de K2S2O8 reste incolore).
3°/ Travail demandé :
* Dans un erlenmeyer, introduire un volume V1=40 mL d’une solution aqueuse S1 d’iodure de
potassium KI de concentration molaire C1=0,5 mol.L-1, à l’aide d’une burette graduée ajouter un volume
V0 = 0,5 mL d’une solution aqueuse (S) de thiosulfate de sodium Na2S2O3 de concentration molaire
C0=0,2 mol.L-1, un volume V’= 10 mL d’une solution d’empois d’amidon. Homogénéiser le mélange à
l’aide d’un agitateur magnétique.
* A l’instant t=0 ajouter au mélange un volume V2=10mL d’une solution aqueuse S2 de peroxodisulfate
de potassium K2S2O8 de concentration molaire C2=0,05 mol.L-1 et déclencher simultanément le
chronomètre. Noter la durée t1 au bout de laquelle apparaît la couleur bleue noire dans le mélange. *
A cet instant t1 ajouter, sans arrêter le chronomètre, un second volume V0 =0,5 mL de la solution S et
noter la durée t2 au bout de laquelle apparaît de nouveau la coloration bleue noire dans la solution.
Refaire la même opération n fois. Consigner les résultats dans le tableau suivant :
Opération n°
p=1
2
3
4
5
6
7
8
9
10
V = p.V0 (mL)
0,5
1,0
1,5
2,0
2,5
3,0
3,5
4,0
4,5
5,0
t (min )
x=n(I2 ) (10-4 mol)
3°/ Travail demandé:
a- Dresser le tableau d’avancement de cette réaction.
Déterminer l’avancement maximal ainsi que le réactif
limitant.
b- Ecrire l’équation chimique de la réaction de titrage.
c- Montrer que l’avancement x=pC0V0/2
d- Compléter le tableau précédent.
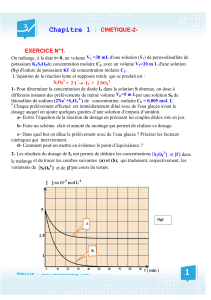
e- Tracer la courbe d’évolution temporelle de x = f(t).
f- Déterminer graphiquement :
- Le temps de demi-réaction t1/2.
- La vitesse moyenne de la réaction entre les instants
t1 = 4 mn et t2 = 8 mn.
- La vitesse instantanée de la réaction à la date t = 0
min
puis à la date t = 6 min.
Chronomètre
S1 + empois d’amidon
d’amidon
Burette
graduée
Sol de thiosulfate de sodium
sodium
S2
2
Agitateur magnétique
1
/
1
100%