Etude du Sinus Transverse et de son implication dans la

1
UNIVERSITE DE NANTES
FACULTE DE MEDECINE
MASTER I SCIENCES BIOLOGIQUES ET MEDICALES
UNITE D’ENSEIGNEMENT OPTIONNEL
MEMOIRE REALISE dans le cadre du CERTIFICAT d’ANATOMIE,
d’IMAGERIE et de MORPHOGENESE
2008-2009
UNIVERSITE DE NANTES
Etude du Sinus Transverse et de son implication dans la
physiopathologie de l’hypertension intra-crânienne
idiopathique
Par
Romain Bourcier
LABORATOIRE D’ANATOMIE DE LA FACULTE DE MEDECINE DE NANTES
Président du jury : Pr. R. ROBERT
Vice-Président : Pr. J.M. ROGEZ
Enseignants : • Pr. O. ARMSTRONG
• Pr. O. BARON
• Pr. G. BERRUT
• Pr. C. BEAUVILLAIN
• Pr. D. CROCHET
• Dr. H. DESAL
• Pr. B. DUPAS
• Dr E. FRAMPAS
• Dr A. HAMEL
• Dr O. HAMEL
• Pr. Y. HELOURY
• Pr A. KERSAINT-GILLY
• Pr. J. LE BORGNE
• Dr M.D. LECLAIR
• Pr. P.A. LEHUR
• Pr. O. RODAT
Laboratoire : S. LAGIER et Y. BLIN - Collaboration Technique

2
UNIVERSITE DE NANTES
FACULTE DE MEDECINE
MASTER I SCIENCES BIOLOGIQUES ET MEDICALES
UNITE D’ENSEIGNEMENT OPTIONNEL
MEMOIRE REALISE dans le cadre du CERTIFICAT d’ANATOMIE,
d’IMAGERIE et de MORPHOGENESE
2008-2009
UNIVERSITE DE NANTES
Etude du Sinus Transverse et de son implication dans la
physiopathologie de l’hypertension intra-crânienne
idiopathique
Par
Romain Bourcier
LABORATOIRE D’ANATOMIE DE LA FACULTE DE MEDECINE DE NANTES
Président du jury : Pr. R. ROBERT
Vice-Président : Pr. J.M. ROGEZ
Enseignants : • Pr. O. ARMSTRONG
• Pr. O. BARON
• Pr. G. BERRUT
• Pr. C. BEAUVILLAIN
• Pr. D. CROCHET
• Dr. H. DESAL
• Pr. B. DUPAS
• Dr E. FRAMPAS
• Dr A. HAMEL
• Dr O. HAMEL
• Pr. Y. HELOURY
• Pr A. KERSAINT-GILLY
• Pr. J. LE BORGNE
• Dr M.D. LECLAIR
• Pr. P.A. LEHUR
• Pr. O. RODAT
Laboratoire : S. LAGIER et Y. BLIN - Collaboration Technique

3
Sommaire :
Introduction p.3
I - Embryologie veineuse cérébrale
Introduction p.4
A- Stade 1 et 2 - 5mm p.5
B- Stade 3 - 6 à 12mm p.7
C- Stade 4 - 12 à 16 mm p.9
D- Stade 5 - 16 à 20 mm p .11
E- Stade 6 - 20 à 26 mm p.13
F- Stade 7- 40 mm p.16
G- Stade 8 - 60 à 80mm p.18
H- De 3 à 7 mois intra-utérin (IU) p.20
Conclusion de l’embryologie p.23
II - Etude anatomique
A- Techniques p.24
B- Projections externes p.25
C- Situation globale du ST p.27
D- Structure externe de la dure-mère voisine du ST p.27
E- Afférences principales p.31
1°) Sinus sagittal supérieur p.32
2°) Sinus tentoriels p.33
a)Sinus tentoriels médiaux
b)Sinus tentoriels latéraux
3°) Veines corticales p.34
4°) Sinus pétreux supérieur p.37

4
F- Vaisseaux d’aval p.40
G- Vascularisation de la paroi durale du ST p.40
I- Innervation de la paroi durale du ST p.40
I – Rapports p.42
Conclusion de l’étude anatomique p.43
III – Etude histologique
Introduction p.44
A – Techniques p.45
B – Résultats p.46
Conclusion de l’étude histologique p.49
IV - Techniques d'imagerie pour la visualisation des veines cérébrales
A – Artériographie cérébrale p.50
B – Phléboscanner p.52
C - Angiographie par résonance magnétique p.54
1°) ARM en contraste de phase
p.55
2°) ARM en temps de vol
p.55
3°) ARM avec injection de gadolinium
p.56
V - Hypothèse d’une compression extrinsèque du ST dans l’IIH
p.60
Conclusion
p.63
Remerciements p.64
Annexes p.65
Bibliographie p.68

5
Introduction
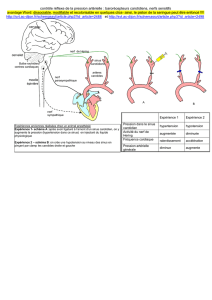
Le sinus transverse (ST) est dans certaines terminologies dénommé sinus latéral (SL)
quand il inclut le sinus sigmoïde (SS). Ce mémoire m’a été proposé car cette zone est
impliquée dans la physiopathologie de l'hypertension intra-crânienne idiopathique (IIH),
affection dont l'incidence semble être en constante augmentation et qui peut conduire à la
cécité dans 10% des cas (1).
L’IIH relève d’une physiopathologie complexe et encore mal élucidée. L’hypothèse
d’une sténose d’un sinus dural veineux retentissant en amont et créant une hypertension
veineuse puis cérébrale globale a été évoquée. Le siège fréquemment observé de ces sténoses
est la jonction ST-SS.
Si cette implication apparaît certaine, de nombreuses publications récentes n'ont
toutefois pas permis de répondre à deux questions importantes :
1 - les sténoses de la jonction ST-SS sont-elles la cause de l'hypertension
intracrânienne ou la conséquence de celle-ci ? Intuitivement, on imagine une sténose
secondaire à l’hypertension intra-cranienne sur une zone de moindre résistance de la paroi
durale. Une sorte de « cercle vicieux » avec l’apparition secondaire d’une hypertension
veineuse en amont de cette sténose participant à l’augmentation de la pression intra-cranienne
(PIC) peut alors être évoquée.
2 – pourquoi les sténoses siègent–t–elles toujours au niveau de cette jonction ST-SS?
La compréhension de ces mécanismes permettrait d'aborder les approches
thérapeutiques de manière plus rationnelle et en particulier de préciser les indications de
prises en charge, non dénuées d'inconvénient, comme les dérivations chirurgicales du LCR,
l'angioplastie et le stenting de cette zone.
Dans ce mémoire nous rappellerons dans un premier temps les caractéristiques de ce
tableau clinico-radiologique.
Puis, afin de tenter de répondre à ces questions, nous étudierons différentes approches:
embryologique, anatomique, histologique et radiologique.
Enfin nous présenterons une ouverture à d'éventuels autres travaux de recherche pour
mieux comprendre cette pathologie.
Cf : annexe pour plus d’éléments sur l’IIH
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
 57
57
 58
58
 59
59
 60
60
 61
61
 62
62
 63
63
 64
64
 65
65
 66
66
 67
67
 68
68
 69
69
1
/
69
100%